Clear Sky Science · zh
滑膜炎性巨噬细胞来源的细胞外囊泡以FMRP选择性分拣方式加剧骨性关节炎中的软骨损伤
为何关节炎症对疼痛膝盖至关重要
许多人把骨关节炎视为简单的“磨损”,与衰老有关,但越来越多的证据表明,关节内部的低度炎症能悄然推动疾病进展。本研究提出了一个关键问题:关节衬里中的免疫细胞如何与软骨细胞通讯?能否打断这一对话以保护关节?研究结果揭示了一种微小的分子递送系统,它会加重损伤——但同时也为诊断和治疗骨关节炎提供了新途径。
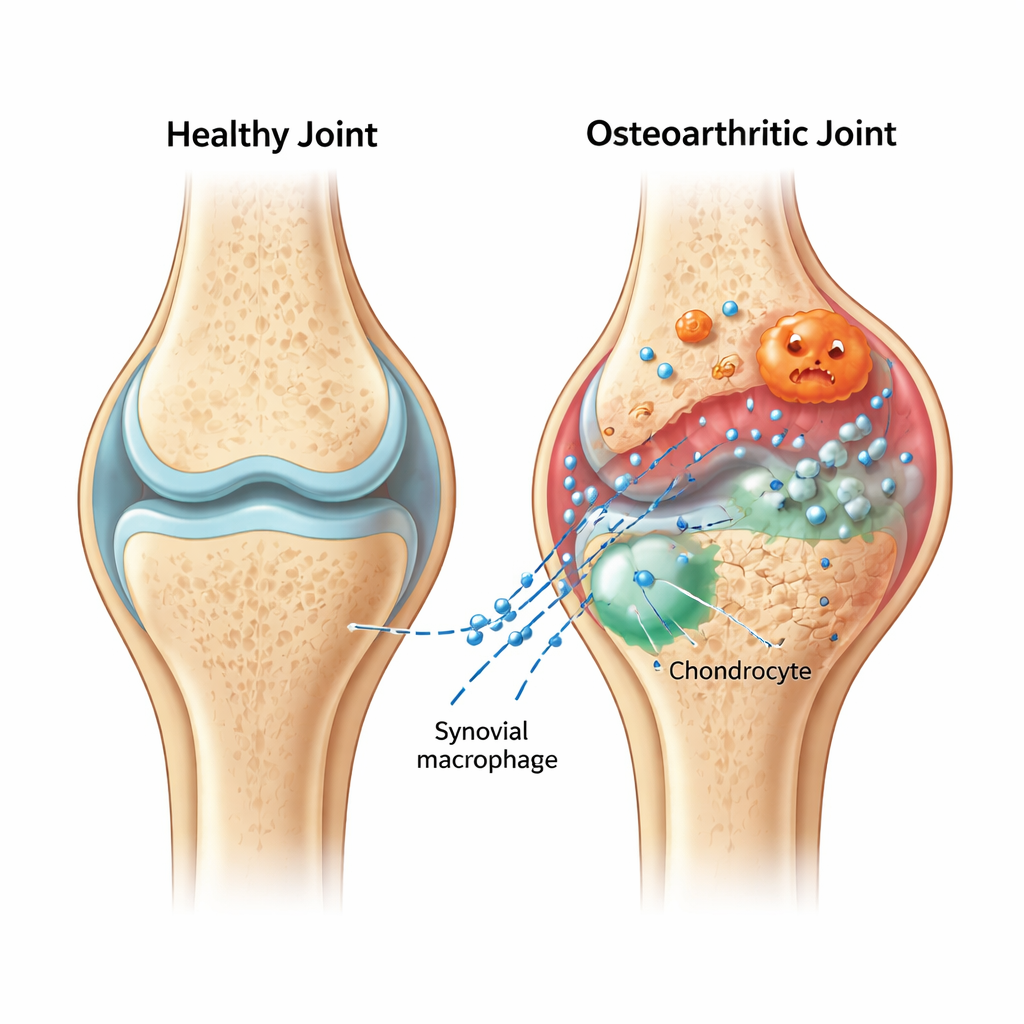
携带坏消息的小包裹
在发生关节炎的膝关节内,柔软的滑膜衬里出现炎症并聚集了称为巨噬细胞的免疫细胞。作者关注的是这些细胞中“易怒”的亚型——促炎巨噬细胞,以及它们释放的微小囊泡,即细胞外囊泡。这些囊泡像密封的包裹,在细胞间运输分子。在外科诱导的骨关节炎大鼠中,研究团队证明来自炎性巨噬细胞的囊泡会定向到软骨并加剧损伤:本来光滑、有缓冲作用的表面变得更粗糙、更薄,关键的软骨蛋白减少而降解酶增加。
炎症如何关闭软骨的自我清理机制
软骨细胞(软骨细胞)依赖一种称为自噬的清理机制来回收损耗的成分,维持长期健康。当研究者比较暴露于炎性囊泡的软骨与暴露于生理盐水的软骨时,发现自噬通路强烈被抑制的迹象。在电子显微镜下,接受囊泡处理的关节软骨中典型的回收囊泡显著减少。在细胞培养中,暴露于巨噬细胞囊泡的软骨细胞形成的自噬小体和自噬溶酶体也更少,证实它们的自我清理机制在损伤积累时被关闭。
单一微小RNA翻转关键开关
进一步深入研究时,团队检查了封装在巨噬细胞囊泡内的微小RNA调控分子。其中一种分子,miR-155-5p,格外突出:在骨关节炎动物的囊泡中以及人类骨关节炎的关节组织中(尤以滑膜为甚)富集。实验显示,囊泡递送的miR-155-5p进入软骨细胞并直接靶向一种称为GSK-3β的蛋白,该蛋白通常有助于抑制称为mTORC1的生长控制通路。当GSK-3β被抑制,mTORC1变得过度活跃,自噬下降,软骨细胞应对压力的能力减弱。在大鼠中用设计性的“antagomiR”阻断miR-155-5p可恢复自噬、保护软骨结构并减轻骨关节炎表现;而在其巨噬细胞中缺失miR-155的基因工程小鼠,则表现为较轻的疾病和较少的滑膜炎。
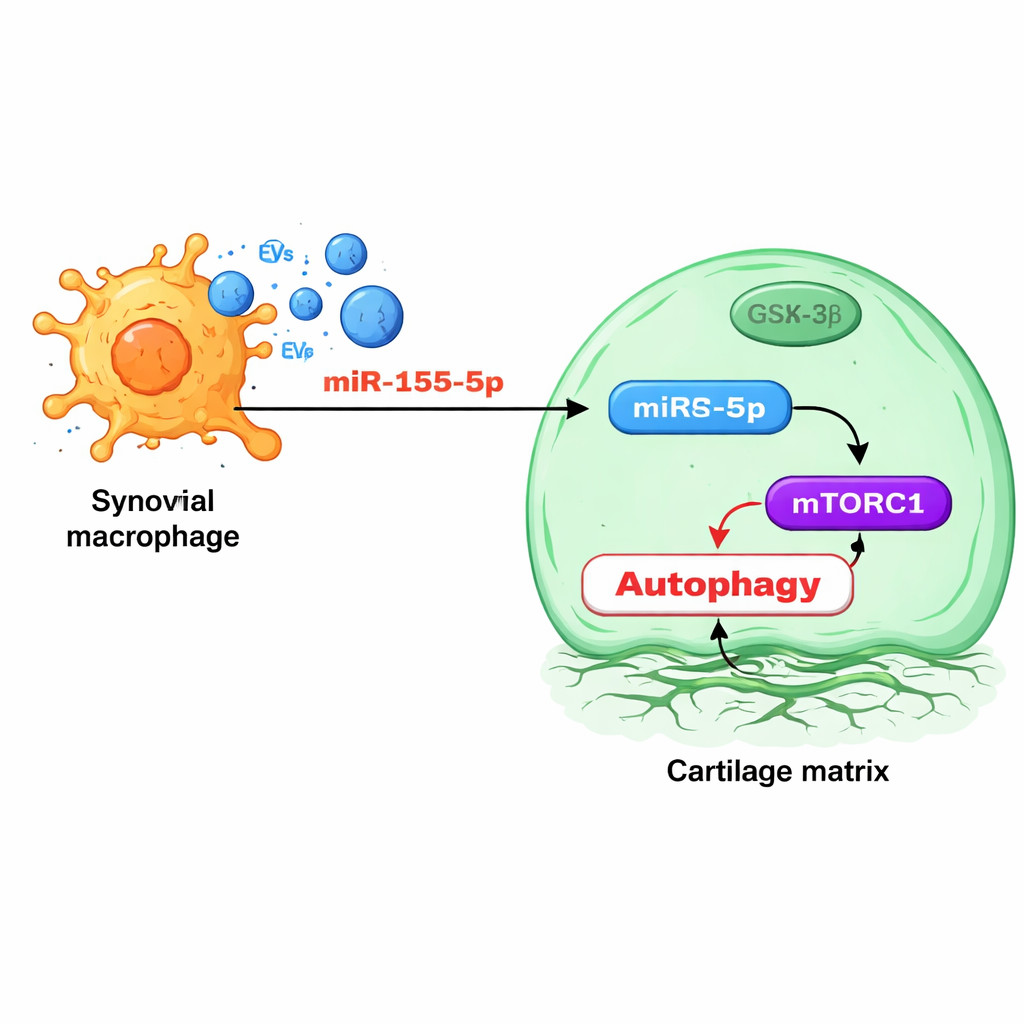
对有害信号的分拣与定位
有趣的是,研究发现巨噬细胞使用一种特定的RNA结合蛋白FMRP来选择性地将miR-155-5p装入囊泡。当FMRP水平增加时,囊泡携带更多miR-155-5p并对软骨细胞造成更大伤害;当FMRP减少时,囊泡毒性降低,软骨细胞自噬反弹。循环于血液中的囊泡中FMRP水平在大鼠和人类患者的骨关节炎进展中上升,这表明该蛋白或携带它的囊泡可作为一种基于血液的疾病活动性标志,免去了影像学或侵入性检查。
一种定位到目标细胞的无细胞疗法
基于这些机制性发现,研究人员构建了一种潜在疗法:使用来自脂肪衍生间充质细胞(一种存在于脂肪组织的类干细胞)的囊泡。他们在这些囊泡表面连接了一个能作为促炎巨噬细胞“归巢”装置的小肽,并装载了antagomiR-155-5p。在骨关节炎大鼠中,反复注入这些靶向囊泡减少了滑膜炎,促使巨噬细胞向更“修复性”状态转变,降低了关节内的miR-155-5p水平,恢复了GSK-3β,并比非靶向囊泡更强烈地改善了软骨结构和成分。在体外对人类滑膜组织样本的应用中,这些工程化囊泡也降低了炎性标志并增强了抗炎信号。
这对骨关节炎患者意味着什么
这项工作将骨关节炎重新定位为不仅由力学磨损驱动的疾病,而是由炎性关节衬里细胞与软骨之间的分子对话所推动。促炎巨噬细胞释放含有miR-155-5p的囊泡,透过GSK-3β/mTORC1通路关闭软骨细胞的自我修复系统,加速组织分解。通过以基因方式或使用靶向治疗囊泡阻断该信号,研究者在动物模型和人体组织中都能缓解炎症与软骨损伤。尽管在这些策略进入临床之前仍需大量工作,但研究凸显了新的可能性:基于囊泡货物的血液检测用于追踪疾病,以及能抑制有害炎症同时帮助软骨自我保护的精确无细胞疗法。
引用: Zhao, S., Wang, J., Xue, M. et al. Synovial inflammatory macrophage-derived extracellular vesicles exacerbate cartilage lesions with a FMRP-selectively sorted manner in osteoarthritis. Bone Res 14, 26 (2026). https://doi.org/10.1038/s41413-025-00502-4
关键词: 骨关节炎, 细胞外囊泡, 巨噬细胞, 软骨, 微小RNA-155