Clear Sky Science · zh
MicroRNA-132/212 通过靶向腹侧被盖区的多巴胺转运蛋白负向调节阿片类药物的奖赏作用
这项研究与日常生活的重要性
阿片类镇痛药和相关药物可以缓解疼痛,但也带来严重的成瘾风险。本研究深入大脑奖赏系统,识别出影响阿片类药物奖赏强度的小型基因开关。通过了解这些开关,科学家希望设计更聪明的治疗方法,在缓解疼痛或控制依赖的同时,不致劫持大脑的愉悦回路。
小分子却影响巨大
我们的大脑依赖一种叫多巴胺的化学物质来传递愉悦信号并驱动我们追求奖励体验,从美味食物到致瘾性药物。该信号的强度和持续时间部分由多巴胺转运蛋白控制,该蛋白像吸尘器一样将多巴胺吸回神经细胞。作者关注两段非常小的遗传物质——microRNA-132 和 microRNA-212,它们可以下调特定蛋白的产生。早期研究将这些 microRNA 与可卡因使用和应激联系起来。本研究团队探讨它们是否也影响大脑对阿片类药物,尤其是吗啡的反应。
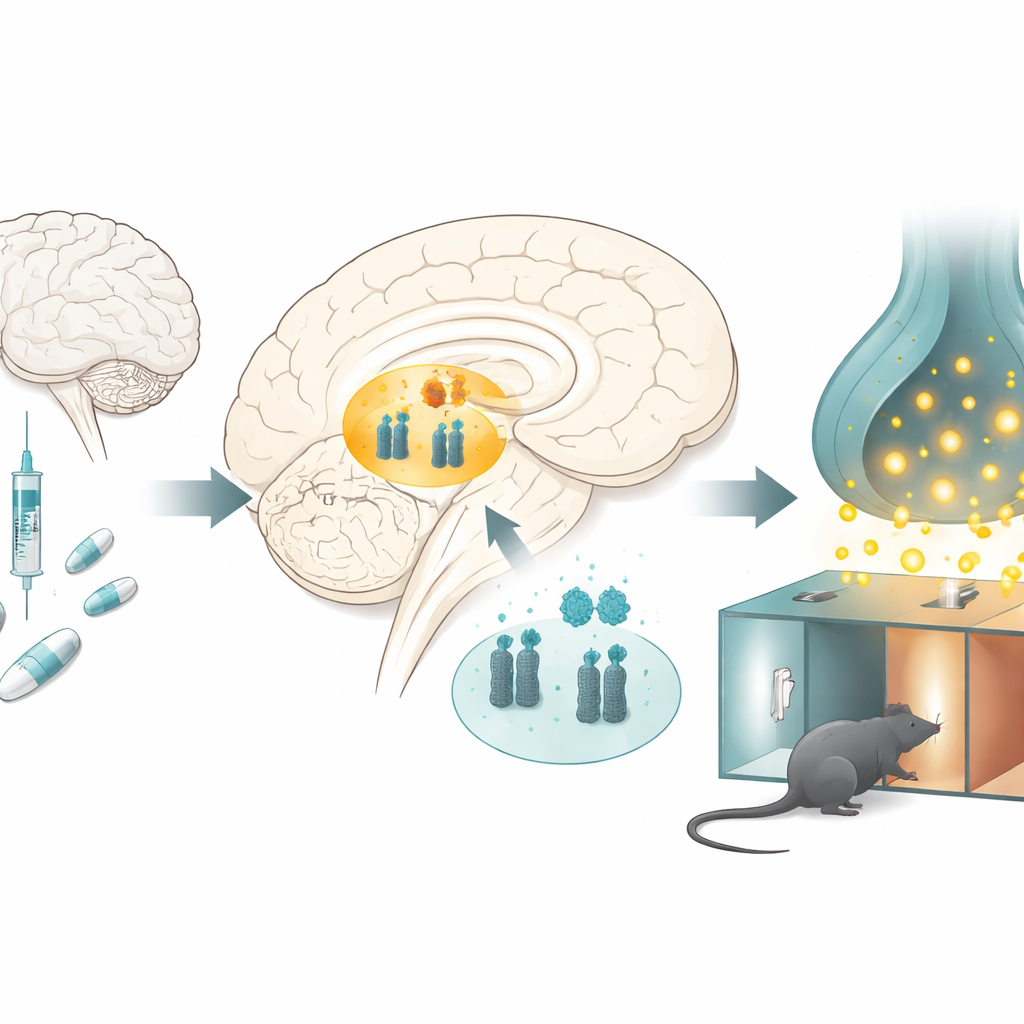
阿片类如何改变大脑的奖赏中心
研究者在大鼠身上反复给予吗啡,使用经典的药物奖赏测试——动物学会偏好与药物相关联的房间。几天后,接受吗啡的大鼠在与吗啡配对的舱室中停留时间更长,表明药物具有奖赏性。检查大脑深处的关键奖赏区域——腹侧被盖区时,研究者发现了明显的模式:microRNA-132 和 microRNA-212 水平下降,而多巴胺转运蛋白水平上升。当大鼠仅接受吗啡而不进行位置学习任务时也出现类似变化,表明慢性药物暴露本身就会改变这种分子平衡。
精准定位直接的分子联系
为确认这些 microRNA 是否真正控制多巴胺转运蛋白,研究团队转而在体外的人类神经样细胞中进行实验。通过人为提高 microRNA-132 或 microRNA-212 的水平,他们观察到转运蛋白的mRNA和蛋白质水平均下降。阻断这些 microRNA 则产生相反效应。他们随后构建了一个报告基因,将发光酶与转运蛋白的调控尾部连接起来。加入 microRNA 会减弱光信号,但当结合位点的几个关键碱基被突变时,这种效应消失。综合这些实验表明,microRNA-132 和 microRNA-212 直接结合转运蛋白的mRNA并抑制其表达。
从分子到多巴胺水平与行为的链路
接下来研究者考察这种分子调控在活体神经细胞中的表现。在培养的神经细胞中,增加这些 microRNA 会减少多巴胺的再摄取,而阻断它们则增强多巴胺清除。当他们人为上调或下调多巴胺转运蛋白水平时,microRNA 的影响相应增强或减弱,证实转运蛋白是主要中介。在活体大鼠中,提升腹侧被盖区的 microRNA-132 会增加流向连接区域的多巴胺水平,反映出转运蛋白活性减弱。在行为层面,使用病毒工具在该脑区“海绵吸收”microRNA-132 或 microRNA-212 使大鼠对吗啡形成更强的偏好,同时转运蛋白水平升高。相反,在同一区域强制表达额外的 microRNA-132 则降低了转运蛋白水平并减弱了雄性、雌性和青少年动物对吗啡的偏好,而不影响运动或对天然奖励(如糖水)的喜好。
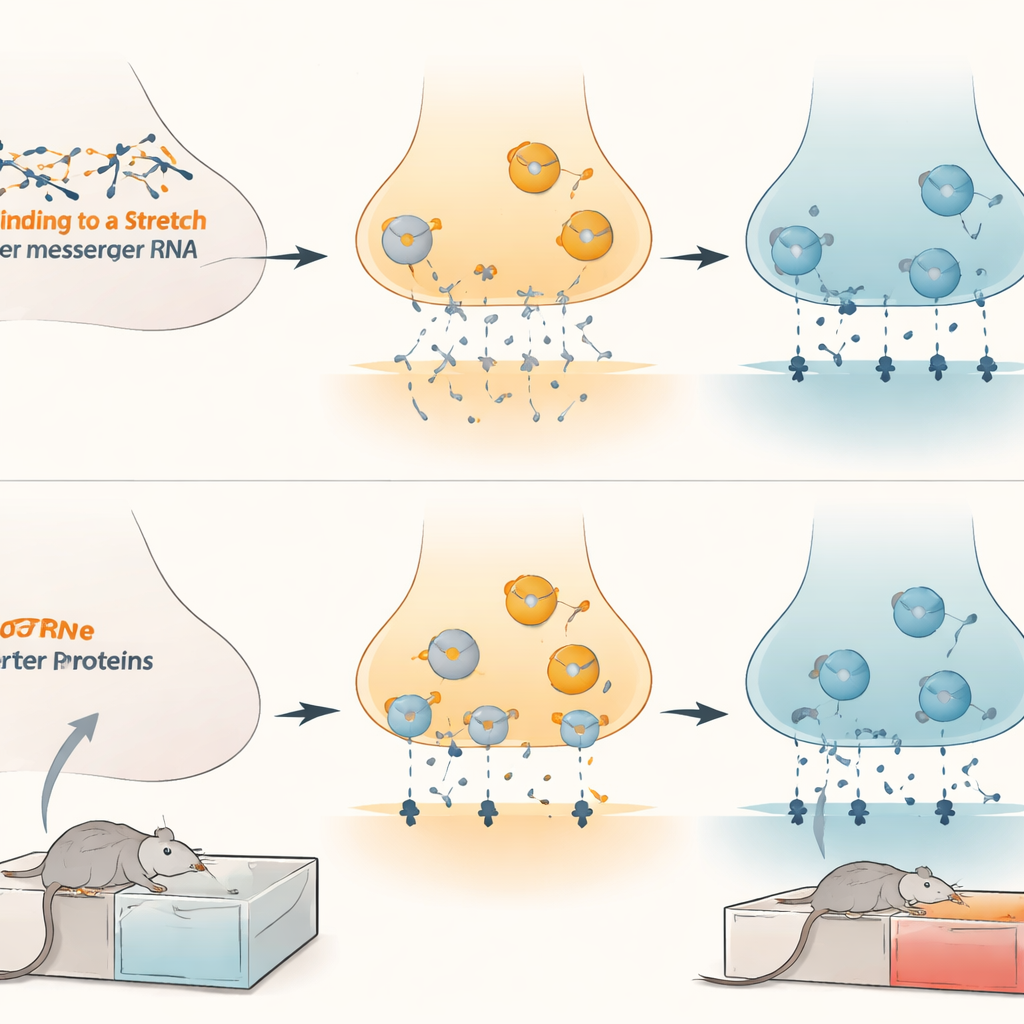
对治疗阿片类成瘾的启示
这些发现揭示了大脑奖赏回路中的精细制动系统:microRNA-132 和 microRNA-212 控制多巴胺转运蛋白的水平,从而影响阿片类药物的奖赏强度。慢性吗啡似乎通过降低这些 microRNA 来解除该制动,使转运蛋白水平上升并帮助巩固与药物相关的奖赏信号。通过在腹侧被盖区特异性恢复或模拟这些 microRNA 的作用,或许可以减弱阿片类药物的奖赏吸引力,而不会广泛压抑愉悦或运动功能。虽然要在人体中测试此类策略仍需大量工作,但本研究指出了一条新的、高度靶向的路径,未来有望在大脑自身的分子调节层面上应对成瘾问题。
引用: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
关键词: 阿片类成瘾, 多巴胺转运蛋白, microRNA-132, 腹侧被盖区, 吗啡奖赏