Clear Sky Science · zh
孕期免疫激活通过表观遗传机制对突触与神经发育通路的产前和产后影响
母亲的免疫系统如何塑造孩子的大脑
妊娠期感染长期以来被认为与子代患精神分裂症、自闭症和注意力缺陷多动障碍等疾病的风险增加相关,但将生病的母体与易感成年大脑连接起来的生物学“桥梁”一直不清楚。这项小鼠研究展示了母体在妊娠期对流感的免疫反应如何在发育中的大脑上留下长期的化学印记,改变脑细胞的通信方式,并可能增加未来精神健康与神经学问题的风险。
妊娠期疾病与终生大脑风险
人群流行病学研究显示,当孕妇发生感染时,其子代在成年后更可能出现多种精神和神经发育障碍。作者关注母体免疫激活——即机体抗感染时释放的一系列免疫信号。这些信号可以穿过或影响胎盘,并在神经回路正在建立的关键时期与发育中的大脑相互作用。额叶皮质对计划、决策与情绪控制至关重要,其发育期长,对早期干扰尤其敏感。
剖析产前与产后影响
为将子宫内发生的效应与产后效应区分开,研究者在妊娠早期(相当于人类第一孕 trimester 末期)感染了孕鼠一种温和且不致死的流感病毒。部分幼鼠由出生母鼠抚育,另一些在出生后24小时内被交由代养母鼠照顾。这样形成四组:既无产前也无产后暴露的后代、仅产前暴露、仅产后暴露以及两期均暴露的后代。当这些后代成年后,团队检查了额叶皮层的神经元,分析了基因活性以及“表观遗传”标记——附着在DNA包装蛋白上的化学标签,这些标签帮助控制基因的开启与关闭。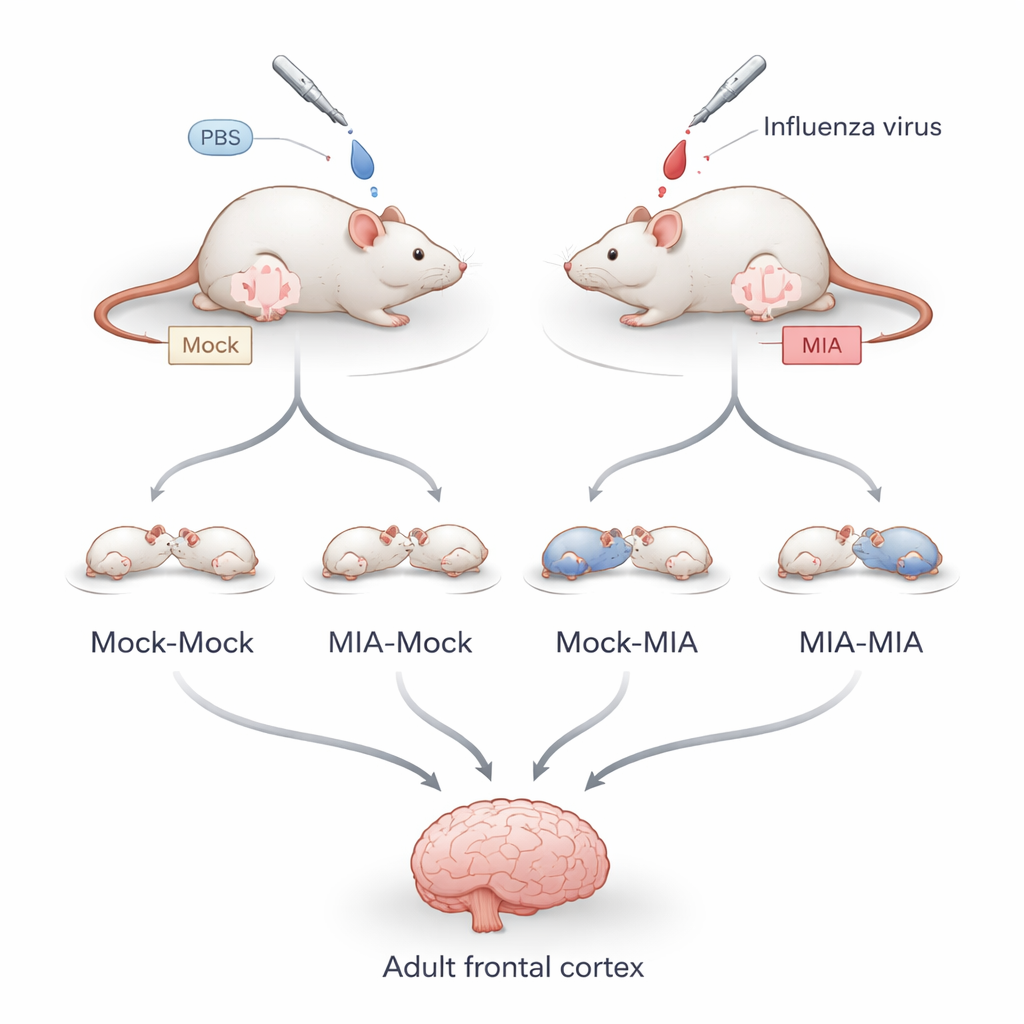
大脑DNA上持久的化学印记
研究集中于两种组蛋白修饰H3K27ac和H3K4me3,它们分别标记活跃的增强子位点和基因启动点。利用灵敏的测序方法,作者绘制了数以万计的这些调控区域,并测量了各组中哪些基因表达增高或降低。他们发现,产前的母体免疫激活在增强子区域产生了广泛且持久的变化——这些区域作为基因活性的控制旋钮。受影响的基因尤其富集于前脑构建、轴突生长引导以及早期神经元通讯点的建立等过程。同样的基因在产后由免疫激活母亲抚育的幼鼠中也表现出表达改变,表明这是在发育过程中持续的调控轨迹,而非短暂的冲击。
从表观遗传改变到突触与回路的调整
产前和产后暴露均影响了调控神经元相互信号传递的分子通路。与谷氨酸(主要的兴奋性递质)、GABA(主要抑制性递质)和多巴胺(与动机与奖赏相关)有关的基因在其调控元件与表达水平上都出现了协调性变化。这些系统在精神分裂症、抑郁症、自闭症和成瘾等疾病中多次被牵涉。作者还发现参与突触组织、轴突生长和回路精细化的基因受影响,尤其是产后暴露影响显著,提示母亲的行为以及产后持续的免疫相关变化共同塑造了神经网络的布线与调谐。网络分析突出了一组核心转录因子——基因活动的主调控者,在两个时间窗口均受到干扰。
与人类精神疾病风险的关联
为了检验这些小鼠变化与人类疾病的相关性,团队将小鼠的增强子和启动子位点转换为最接近的人类对应位点,并与大型精神疾病遗传学研究进行比较。受母体免疫激活影响的区域在精神分裂症、双相障碍、抑郁症、神经质倾向和注意力缺陷多动障碍的人类风险位点中呈强烈富集,但在大多数非精神类疾病中则不显著。这一模式表明,承载遗传易感性的同类调控DNA区域也对妊娠期与早期生命的免疫挑战敏感,成为基因与环境交汇的关键点。
对人类健康的意义
对非专业读者而言,关键信息是:母体的免疫反应——而不仅仅是感染本身——可以在发育中大脑的“说明书”边缘留下持久的“注释”。这些在产前与产后写下的表观遗传注释,能微妙地改变脑细胞的生长方式以及它们在控制思维、情绪与行为的回路中的交流。尽管大多数生病母亲的孩子不会发展为精神疾病,这项工作有助于解释为何有些个体更易感,并强调在妊娠期与早期生命阶段预防和管理感染与炎症对长期大脑健康的重要性。
引用: Zhu, B., Li, G., Saunders, J.M. et al. Prenatal and postnatal effects of gestational immune activation on synaptic and neurodevelopmental pathways via epigenetic mechanisms. Transl Psychiatry 16, 82 (2026). https://doi.org/10.1038/s41398-026-03884-z
关键词: 母体免疫激活, 表观遗传学, 神经发育, 突触信号传导, 精神病学风险