Clear Sky Science · zh
应激后皮质酮对海马可兴奋性和涉及超极化激活阳离子通道1功能的行为的影响
当应激记忆出问题时
大多数人在惊恐经历后能够恢复,但对某些人来说,事件的提示会在数月甚至数年内引发强烈的恐惧和生动的记忆。这种被称为创伤后应激障碍(PTSD)的状况,与大脑如何存储和更新危险记忆密切相关。海马——一个对形成和回忆情境及事件至关重要的海马状脑区——在PTSD患者中常表现为萎缩和异常活动。本研究用小鼠探讨一个简单但有重大意义的问题:创伤后立即释放的应激激素如何改变海马细胞,使之固定不良恐惧并干扰正常记忆?
在小鼠中构建更好的创伤模型
研究者常用一种称为单次持续应激(SPS)的方案来模拟啮齿动物的PTSD特征。该方案结合了若干强烈应激源——如限制、强制游泳和短暂麻醉——并在大鼠中产生了可靠的类PTSD效应。然而在小鼠中,结果并不一致:某些品系表现出明显的恐惧与记忆改变,另一些则没有,这表明存在一种仅在特定条件下显现的潜在脆弱性。作者怀疑,应激激素本身,尤其是皮质酮(啮齿动物中的皮质醇对应物),可能就是缺失的因素之一。他们设计了一个模型,使成年雄性小鼠在接受SPS后立即注射皮质酮,旨在更贴近人类创伤后激素激增的情形。
应激激素暴露出潜在的记忆问题 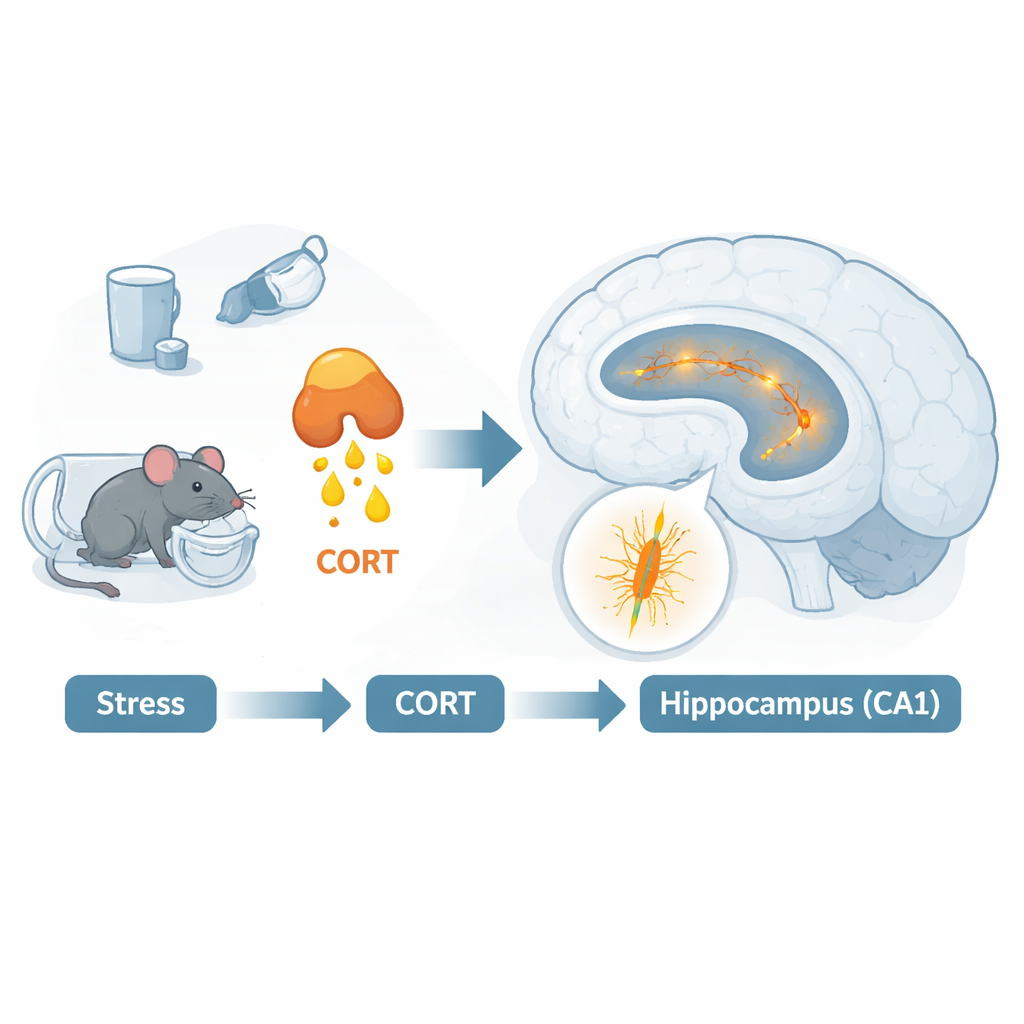
Figure 1.

SPS处理并经过10天恢复期后,小鼠接受了一系列行为测试。在开放场地中,受应激的小鼠无论是否额外注射激素,运动正常且未显示明显的焦虑样行为增加。但在用于检测短时空间工作记忆的Y形迷宫中,接受SPS加皮质酮的小鼠表现更差:它们较少以灵活的模式在臂间交替,更倾向于重复进入同一臂。随后,动物在情境性恐惧任务中接受训练——在该任务中是环境而非音调预示轻微电击。所有组都学会了这一关联,但只有SPS加皮质酮组随后出现“情境性失忆”:当返回与电击相关的环境时,它们的冻结反应减少,仿佛该环境不再强烈提示危险。与此同时,这些动物在重复安全重新暴露中难以消退恐惧,这是类PTSD行为的一个标志。
一个通道如何抑制记忆神经元 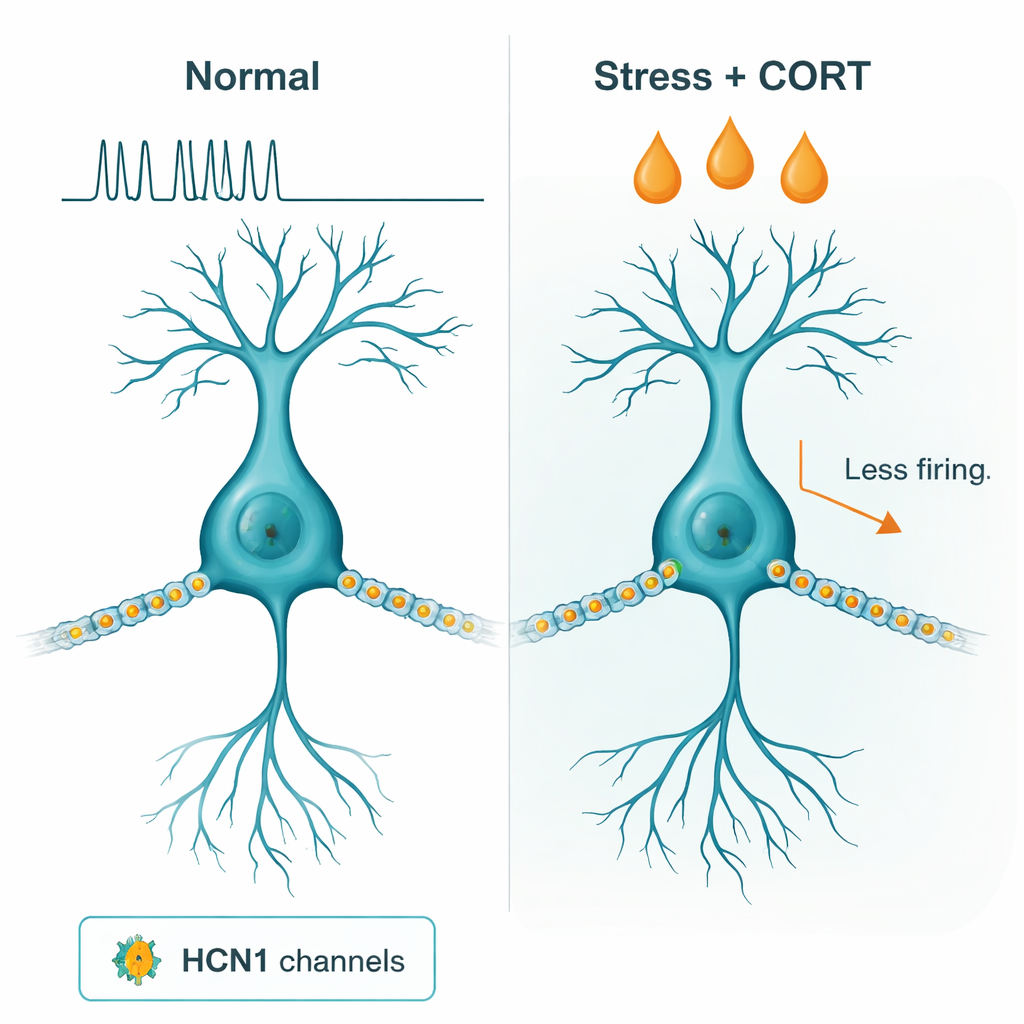
Figure 2.

为了解海马内部发生了什么,研究团队制备了薄的脑片,并记录了背侧CA1区单个神经元的电活动,该区对空间和情境记忆至关重要。在经历SPS加皮质酮的小鼠中,这些细胞更难被激活:其输入阻抗降低,对电流刺激的动作电位发放减少。研究者将这一变化追溯到一种特定的电流——Ih,该电流通过被称为HCN1的蛋白形成的通道流动。在SPS加皮质酮的小鼠中,Ih增大且更易被激活,意味着这些通道在较少负电位时就开放,像强有力的泄漏通道一样分流进入的信号。当科学家应用阻断HCN通道的药物时,神经元的电学特性恢复正常,应对输入的发放能力也得以恢复。
用基因改造证明因果关系
仅有相关性不足以说明问题;作者想确认HCN1是否真正在驱动行为改变。他们使用病毒工具在背侧CA1锥体神经元中特异性地增强或删除HCN1。即便在没有额外激素的情况下,在受应激小鼠中过表达HCN1也足以复制SPS加皮质酮动物的关键特征:空间工作记忆下降、对与恐惧相关情境的回忆减弱以及难以消退恐惧。电生理记录证实这些神经元类似于激素处理组,表现为兴奋性降低和Ih升高。相反,当在SPS加皮质酮小鼠的CA1神经元中选择性去除HCN1时,它们的记忆表现得到改善,神经元兴奋性恢复。换句话说,该通道既能单独产生缺陷(充分性),又是这些缺陷出现所必需的(必要性)。
这对创伤与治疗意味着什么
对非专业读者来说,关键结论是:这项研究将记忆细胞中的一种特定分子“阀门”——HCN1通道——与创伤应激及应激激素共同扭曲记忆的方式联系了起来。在这个小鼠模型中,单独的SPS并不能可靠地产生类PTSD问题,但加入一阵皮质酮激增揭示了海马的持续弱点:其神经元变得过于“安静”,无法恰当地编码和更新情境性恐惧。通过证明上调或下调HCN1可以恶化或拯救这些缺陷,该研究为未来旨在缓解PTSD相关记忆症状的药物明确了一个具体靶点。尽管还需在不同年龄、性别和脑区进行更多验证,这些发现提示,精细调控海马可兴奋性——而不是单纯抑制恐惧反应——可能是创伤后更精确治疗的一条有前景的途径。
引用: Kim, C.S., Kim, J. & Michael, S. Effects of post-stress corticosterone on hippocampal excitability and behavior involving hyperpolarization-activated cation channel 1 function. Transl Psychiatry 16, 74 (2026). https://doi.org/10.1038/s41398-026-03871-4
关键词: PTSD, 海马, 应激激素, HCN1 通道, 记忆消退