Clear Sky Science · zh
GABA能中间神经元功能障碍导致PPT1缺陷小鼠癫痫样活动相关的神经网络振荡改变
当脑节律出错时
癫痫发作不仅是大脑活动的突发风暴;它们常常源于神经元之间交流方式的细微变化。本研究考察了一种罕见的儿童脑疾病——CLN1病,并提出了一个看似简单却意义深远的问题:当一种名为PPT1的酶缺失时,大脑的“节律守护者”会发生什么?通过随时间追踪这些变化,研究者揭示了抑制机制早期的小故障如何逐渐累积,最终导致癫痫发作和广泛的脑损伤。
维持大脑平衡的守护者
我们的大脑依赖两大类神经元。兴奋性细胞,例如海马的金字塔状神经元,推动活动向前;抑制性细胞,称为中间神经元,则像刹车一样控制这种活动并塑造大脑的电节律。在这些中,两个重要群体是钙结合蛋白阳性(PV+)中间神经元和生长抑素阳性(SST+)中间神经元。它们有助于产生和协调节律性脑波,如theta和gamma振荡,这些振荡支持学习和记忆等功能。在CLN1病中,儿童失去PPT1酶,该酶通常负责去除蛋白上的脂基。作者使用携带与患者相同突变的小鼠模型,观察这种酶的缺失如何影响中间神经元及其调控的脑节律。
抑制系统的早期裂缝
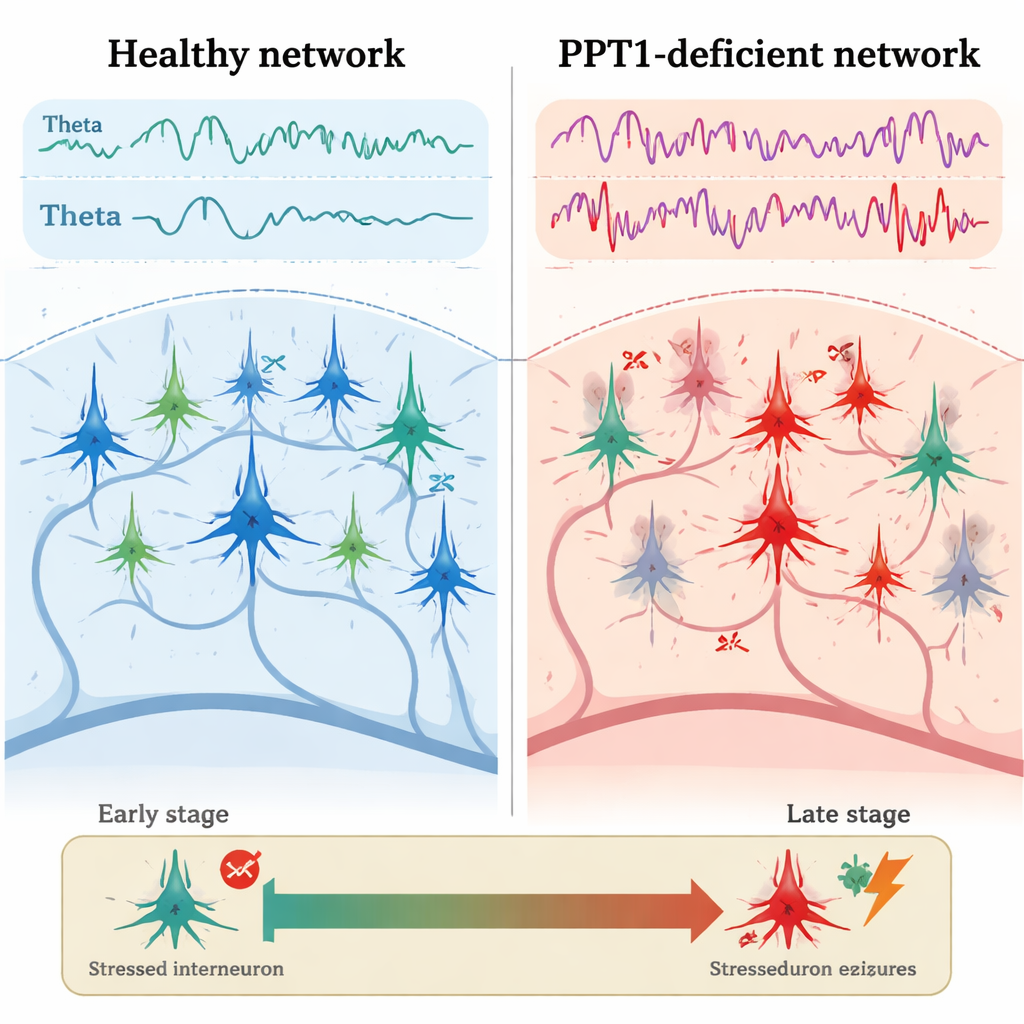
在约三到四个月大的青年突变小鼠中,首个明显问题出现在PV+中间神经元。来自海马的电生理记录显示,这些抑制性细胞的发放频率低于健康小鼠,而邻近的金字塔状神经元发放更快、峰间间隔更短。显微镜观察发现,许多PV+中间神经元出现了caspase-3的激活——这是程序性细胞死亡的关键执行者——尽管它们的总数尚未下降。与此同时,theta和gamma脑波的能量增强,钙成像显示动物活动时海马神经元的活动更强。关键是,theta和gamma节律之间的正常“相互作用”——较慢的波帮助组织较快的波——减弱了,这提示网络活动精细时序在早期就开始失常。
从节律紊乱到癫痫性放电爆发
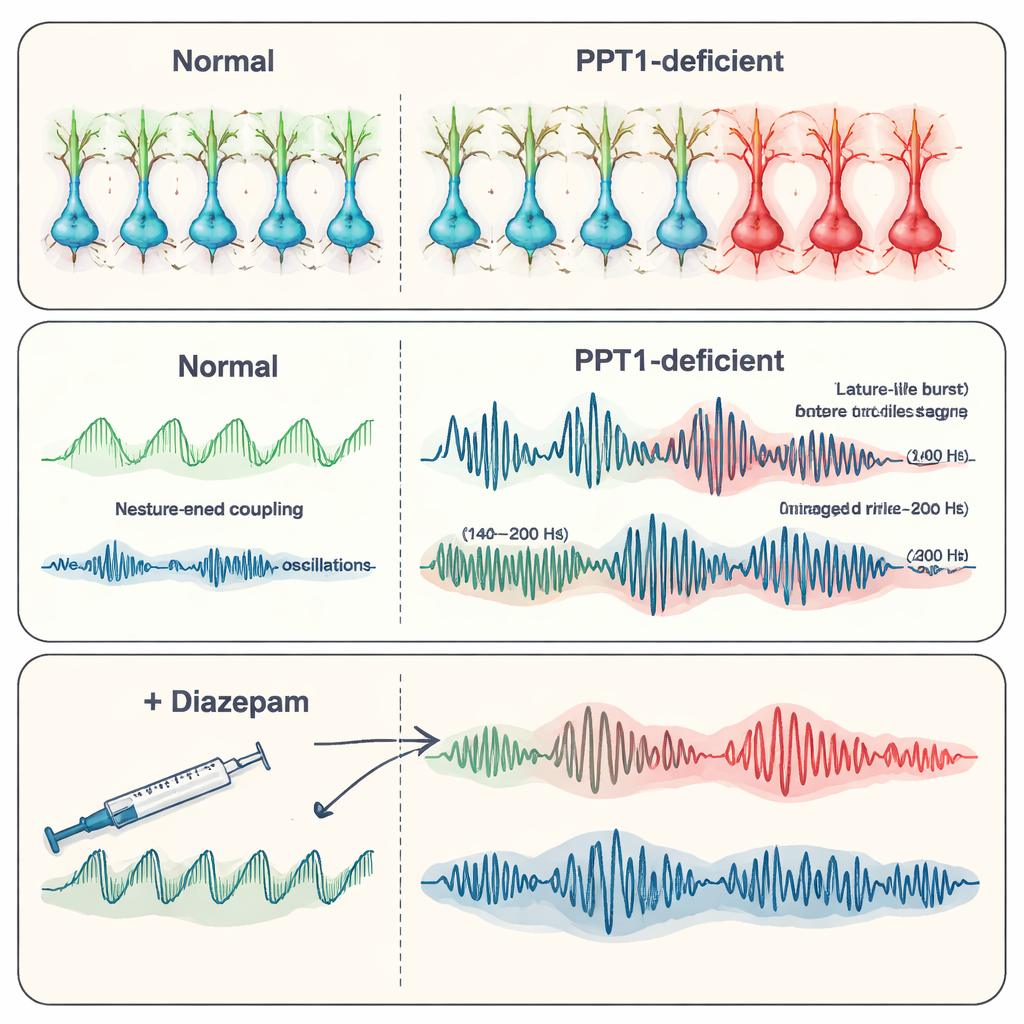
到六到七个月时,情况进一步恶化。许多PV+中间神经元丧失,SST+中间神经元也出现了caspase-3激活的迹象。来自海马的记录显示自发的癫痫样放电——与癫痫相关的短暂异常爆发性活动。团队关注高频“涟漪”现象,这是通常有助于记忆存储的快速振荡。在突变小鼠中,生理性涟漪(约140–200赫兹)变得不那么频繁但振幅更大,而更快的“病理性”涟漪(200–500赫兹),与癫痫紧密相关,则变得更强且更常见。这些变化共同表明,随着抑制控制的失败,组织良好的记忆相关节律正向混乱、易发作的模式转变。
神经元衰竭与地西泮的介入
随病情进展,海马本身开始退化。神经元的钙信号下降,戈尔基染色显示树突更细且分支减少,形成突触的小棘突也变少。对关键海马区域(CA1和CA3)神经元计数证实了广泛的细胞丧失,电生理记录中可检测到的活跃单位也减少。研究者随后测试了地西泮——一种常用的抗癫痫药,可增强抑制性神经递质GABA的作用。在年长的突变小鼠中,地西泮降低了癫痫放电的频率,并部分恢复了更正常的振荡模式,包括涟漪行为,尽管它并不能修复基础的受体损失。这提示即便在抑制性成分受损时,加强剩余的抑制信号仍能在一定程度上平息网络活动。
这些发现为何重要
对非专业读者而言,核心信息是CLN1病不仅仅是脑细胞内废物积累的问题。PPT1的丧失触发了一连串反应:首先,专门的抑制性中间神经元承受压力并开始功能衰竭,这释放出过度活跃的金字塔状神经元并扭曲大脑节律。随着时间推移,这种失衡导致癫痫发作并最终引发大规模的神经元和连接丧失。研究指出了疾病早期的一个干预窗口:保护或挽救PV+中间神经元——例如通过阻断caspase激活——可能有助于防止后期的癫痫和退变。尽管地西泮不能治愈CLN1,其在该模型中抑制异常节律的能力强调了一个更广泛的观点:恢复抑制功能可能是治疗癫痫及相关脑疾病的有力策略。
引用: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
关键词: 癫痫, 中间神经元, 海马, 脑振荡, 溶酶体贮积病