Clear Sky Science · zh
由常见与罕见自闭谱系障碍变异提供信息的基因在组织特异性通路与基因网络中的会聚与分歧
为何自闭症的遗传拼图重要
家庭和临床医生长期以来都知道自闭谱系障碍(ASD)差异很大:有些人需要终生支持,而另一些人虽能独立生活但在社交方面遇到困难。这种多样性很大程度上被认为源自遗传学,但风险分布在成千上万的DNA变异上,每个变异都以微妙方式影响大脑和身体。本研究提出了一个简单但重要的问题:罕见且影响强大的突变与众多常见但效应较小的DNA变异在不同组织中如何协同或各自作用以塑造自闭症——这对理解和治疗该病意味着什么?
两类遗传线索
研究者将罕见变异与常见变异区分开来:罕见变异能强烈破坏基因,但仅见于相对少数人;常见变异在人群中频繁出现,但通常效应较小。罕见变异更容易在个别家庭中与自闭症关联,但它们仅能解释整体遗传风险的一小部分。常见变异合并起来能解释自闭症较大比例的遗传成分,但单个变异的影响微弱、易被忽视。本文作者旨在整合罕见与常见的信号,探问它们是否会在相同生物系统上会聚,或指向身体不同部位与不同的致病机制。
将DNA信号映射到组织与网络
为此,团队使用了一种名为 Mergeomics 的分析框架,将大规模遗传研究与基因在特定组织中如何开关的信息相结合。他们以来自超过9百万个常见DNA变异的全基因组关联数据为起点,这些数据来自逾1.8万名自闭症个体和约2.8万名非自闭症对照。随后,他们利用关于近50种组织中基因活动的详细参考数据,将这些变异映射到基因上,所涉组织包括多个脑区以及消化、免疫、生殖和其他外周器官。通过将同一组织中同时被激活的基因分组,并检验这些基因组与自闭症相关变异的一致性,研究者识别出似乎与ASD重要相关的组织特异性“模块”和调控网络。
脑与身体均有贡献
分析确认了大脑的核心作用——尤其是如前扣带皮层、杏仁核、额叶皮层、小脑和更广泛的皮质区等区域,这些区域已知与情感、社交行为、认知与协调相关。这些脑区的基因网络富含常见与罕见的自闭症相关变异,并与突触信号传导、神经发育及脑内免疫调控有关。然而,图景并未止于颅内。令人惊讶的是,许多外周组织,特别是消化、免疫、内分泌和生殖系统,也包含受自闭症相关常见变异强烈影响的基因模块。这些模块与免疫反应、细胞生长与分裂、能量产生、mRNA 剪接以及被称为 mTOR 的重要控制通路等过程相关,而这些过程都与脑发育和行为有关联。
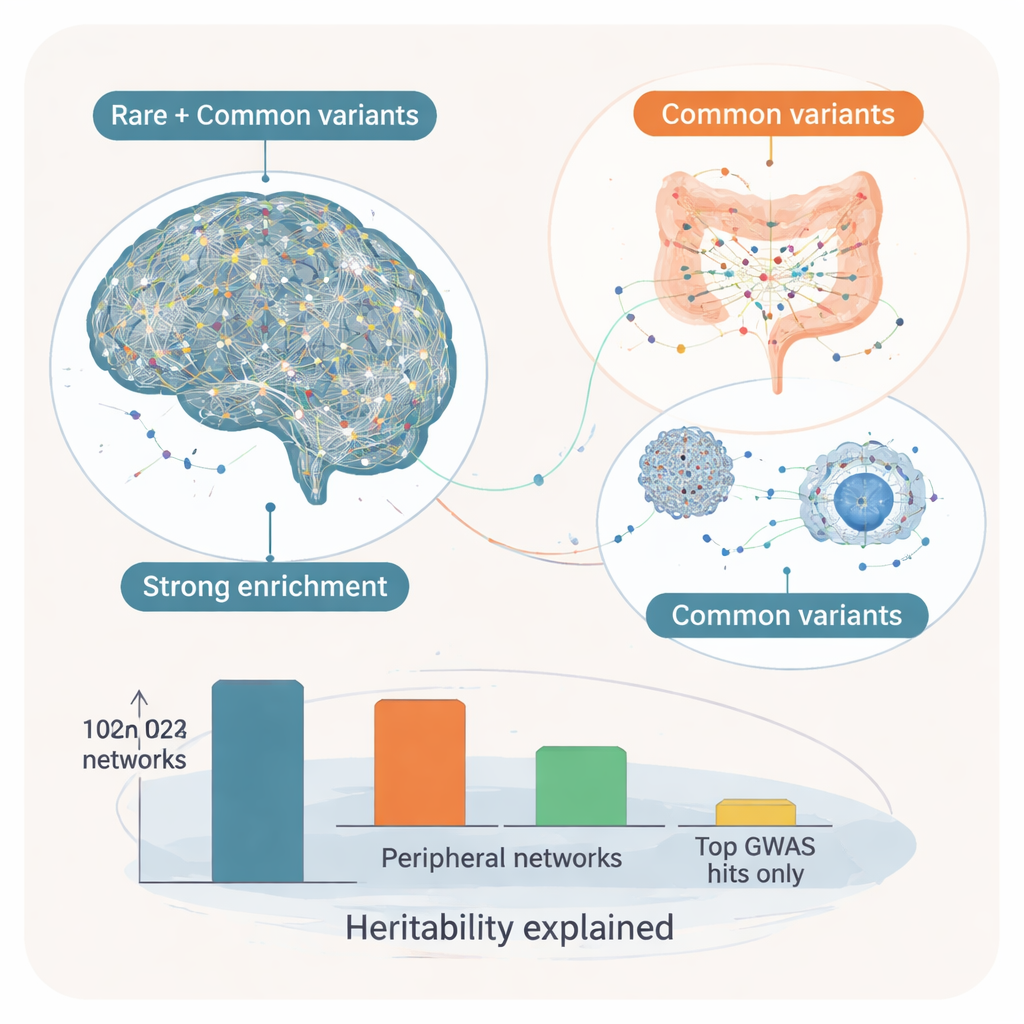
关键调控基因与“核心—修饰子”观点
通过将这些模块置入有方向性的基因调控网络中,研究者进一步询问哪些基因位于枢纽位置——所谓的“关键驱动因子”,它们影响许多其他基因。在脑网络中,这些关键驱动因子对罕见高影响力自闭症变异和常见变异都表现出显著富集,表明它们构成了一个两类风险会聚的“核心”基因集合。示例包括控制突触处神经递质释放的 SYT1,以及参与塑造神经元结构与连通性的 ADD2。其周边网络包含已知的罕见自闭症基因与涉及突触通信和神经元兴奋性的常见变异靶点的混合体。相比之下,外周组织(尤其是消化和内分泌器官)中的关键驱动因子更多地受单独的常见变异影响。这些基因更像“修饰子”,调节免疫、代谢和信号传导通路,可能影响核心脑易感性如何在症状上表现。
对个体与未来治疗的意义
当作者估算这些网络能够解释多少自闭症的遗传风险时,基于大脑的模块解释了约7%的可遗传成分,外周模块另约3%,合计捕获了原始研究中观察到的大部分常见变异遗传力——远多于仅由最强单个DNA信号解释的微小部分。对非专业读者来说,结论是自闭症的遗传遵循分层模式:罕见与常见变异在一个以大脑为中心的核心网络上会聚,这些网络对神经发育至关重要;而广泛存在于肠道、免疫与激素组织中的常见变异很可能作为修饰子,塑造疾病的进程与表型。这个核心—修饰子框架有助于解释为何自闭症在不同个体间差异巨大,并暗示未来的治疗或需同时针对大脑与与之相互作用的更广泛身体系统。
引用: Gill, C., Zuo, Y., Ha, D.Sm. et al. Convergence and divergence of genes informed by common and rare variants of autism spectrum disorders in tissue-specific pathways and gene networks. Transl Psychiatry 16, 98 (2026). https://doi.org/10.1038/s41398-026-03824-x
关键词: 自闭症遗传学, 罕见变异, 常见变异, 脑网络, 肠–脑轴