Clear Sky Science · zh
围产期高雄激素化与免疫激活在啮齿动物模型中再现自闭症亚型
妊娠如何塑造发育中的大脑
为什么有些儿童会发展为自闭谱系障碍而其他人则不会,即便他们共享基因和环境?本研究使用小鼠来探讨两种与人类自闭症风险升高相关的情况:妊娠期雄性类激素增高和母体强烈的免疫反应。研究者从妊娠晚期追踪到幼年,显示这两种影响都可以导致类似自闭症的特征,但在社交行为、大脑结构和免疫变化上呈现不同的模式。
两种不同的妊娠风险受检
团队聚焦两种现实世界的风险因素。其一,模拟高雄激素暴露,类似多囊卵巢综合征患者中可能出现的睾酮增高。其二,模拟母体免疫激活,以再现妊娠期对感染的强烈免疫反应。孕鼠被给予额外的睾酮、促免疫的化合物、两者同时给予或都不给予。随后研究者追踪幼鼠的早期“婴儿叫声”、少年期社交行为、重复行为和脑解剖,同时检查胎盘、胎儿及新生儿大脑,以及与应激和生长相关的分子。
通往类似自闭症行为的不同路径
两种模型都诱发了类似自闭症的特征,但方式并不相同。暴露于过量雄激素的幼鼠在社交交流方面变化尤为显著。新生期时,它们发出的超声叫声更少且更短——这种高频声音是幼鼠吸引母鼠注意的手段——但这些叫声的音高高于正常水平。少年期时,这些小鼠在与其他小鼠相遇时叫声更少,也不太愿意与社交伙伴共处。有趣的是,当在熟悉小鼠和陌生小鼠之间做选择时,它们更倾向于靠近陌生小鼠,表明其社交探索的基本驱动力发生了改变,而不仅仅是减少。相比之下,来自免疫激活母鼠的后代表现出较轻微的社交改变,但重复行为明显增加:在标准的掩埋弹珠实验中,它们掩埋的弹珠更多,这一实验反映重复性、强迫样的挖掘行为。
变化中的大脑与免疫系统内部情况
脑成像显示,雄激素暴露的雄鼠总体脑体积较小——约减少4%——但某些与动机和社交行为相关的关键区域相对增大,例如伏隔核和邻近的与应激、情绪相关的条状终纹床核(bed nucleus of the stria terminalis)。相比之下,母体免疫激活并未改变整体脑体积,但选择性地增大了皮层的部分区域,包括常与自闭症患者重复行为相关的扣带回。在细胞层面,雄激素暴露的少年鼠显示出持续的神经炎症迹象:海马中的免疫细胞——小胶质细胞表现出更高的激活状态并且树突分支减少,这种状态会影响神经回路的修剪与精细化。两种模型在胎盘和新生儿脑中的免疫分子也显示出不同的特征,并且在两种重要脑蛋白上出现相反变化——支持神经生长的BDNF与帮助调节动机和奖赏的多巴胺D2受体。
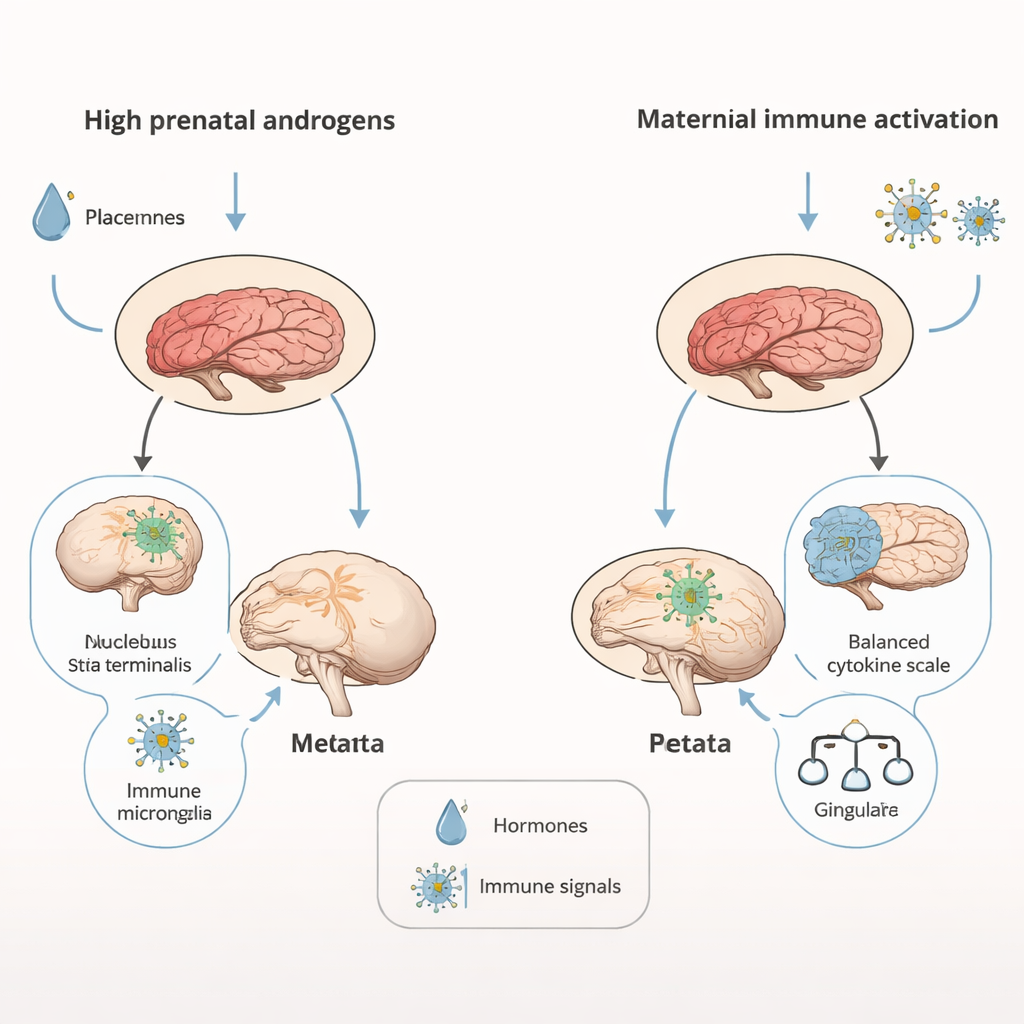
对自闭症亚型与性别差异的线索
将行为与生物学发现综合起来看,这两种小鼠模型似乎分别反映了人类观察到的不同自闭症亚型。雄激素暴露主要破坏社交交流,而对重复行为的影响相对较小——类似于那些社交困难多于重复倾向的人群。母体免疫激活则呈相反模式,重复行为更强烈而社交变化较为微妙。由于男性胎儿天生经历比女性更高的雄激素水平,研究支持这样一种观点:即便是这些激素的适度增加——或大脑对其反应方式的差异——也可能促成男孩中自闭症发病率较高,尤其是以社交交流障碍为主的亚型。
这对理解自闭症意味着什么
对非专业读者来说,关键的信息是“自闭症”并非单一路径或单一的大脑模式。在这些小鼠中,额外的雄性类激素和强烈的母体免疫反应各自将发育推向类似自闭症的结局,但通过不同的生物学通路并伴随不同的行为谱。这有助于解释为何自闭症患者在表现上差异巨大。它还提示未来的治疗或预防措施可能需要针对潜在原因进行定制——无论这些原因更偏向激素相关、免疫相关,还是二者混合——而不能假定所有自闭症都有相同的生物学基础。
引用: Burke, F.F., Randell, A.M., Sparkes, K.M. et al. Perinatal hyperandrogenization and immune activation in rodents model subtypes of autism. Transl Psychiatry 16, 97 (2026). https://doi.org/10.1038/s41398-026-03821-0
关键词: 自闭症亚型, 产前激素, 母体免疫激活, 神经发育, 啮齿动物模型