Clear Sky Science · zh
组胺 H3 受体作为酒精使用障碍的靶点:挑战动物模型在药物开发临床转化中的可预测性
这项研究与日常生活的关系
酒精使用障碍影响着全球数以百万计的人,但现有药物只能帮助其中的一小部分。本文追踪了一个有前景的新药候选物 BP1.3656B 从实验室到人体试验的整个过程,展示了在动物身上效果显著的想法为何仍可能在人类身上失败——以及这一差距为何对希望获得更好问题饮酒治疗的人来说至关重要。
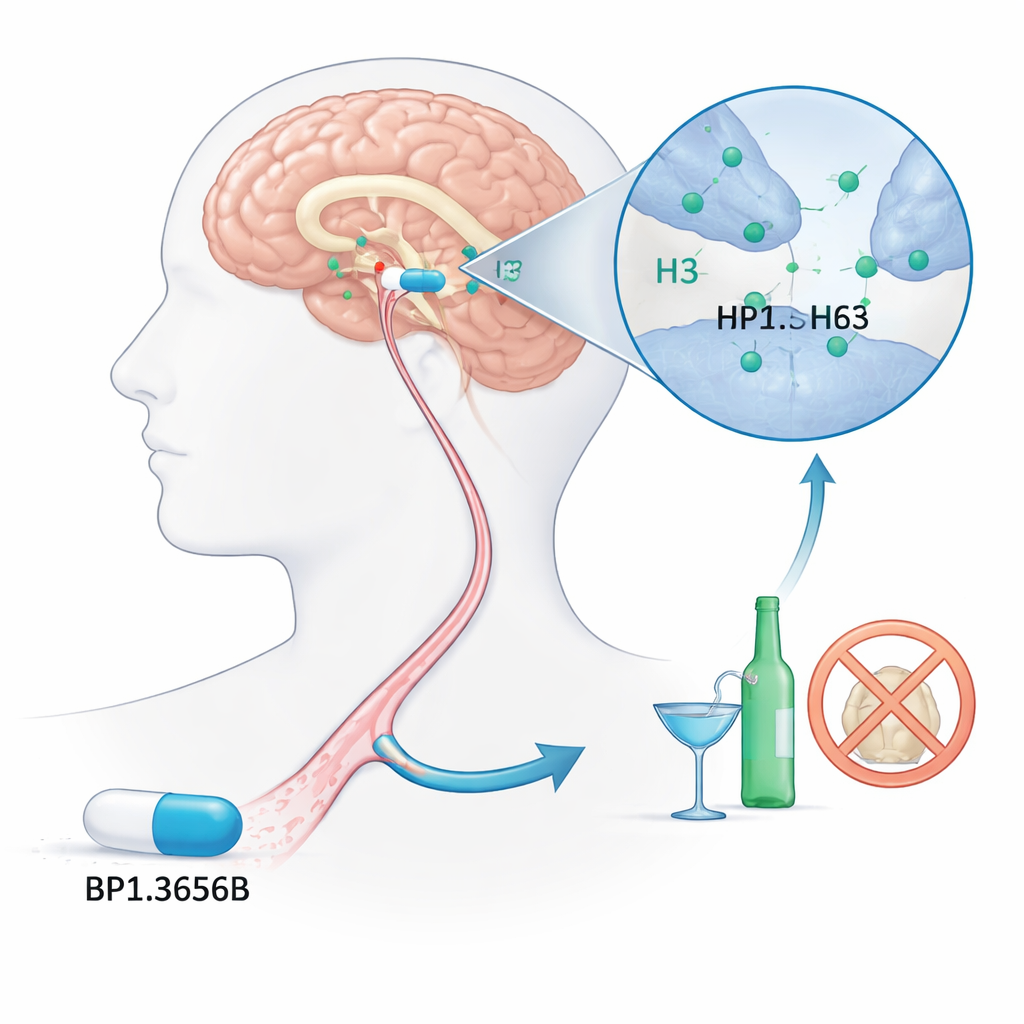
针对问题饮酒的新的大脑靶点
研究人员将注意力集中在一种较少为人知的大脑开关——组胺 H3 受体。组胺最为人知的是在过敏反应中的作用,但在大脑中它帮助调节警觉性和神经细胞之间的通讯。H3 受体像一个调光器,降低组胺及若干参与奖赏与动机的其他神经递质的释放。因为酒精与这些大脑系统有强烈的相互作用,科学家长期以来推测阻断 H3 受体可能降低饮酒冲动。BP1.3656B 被设计为一种强效的 H3 阻断剂,期望能减弱酒精对大脑奖赏回路的吸引力。
从化学到动物成功故事
在早期测试中,BP1.3656B 展现了药物开发者梦寐以求的特性。它对 H3 受体结合紧密且选择性高,能良好进入大脑,并在标准实验筛查中显示安全。在小鼠中,该药减少了通常在酒精注射后出现的活动激增,并在“黑暗中饮酒”试验中在一定程度上降低了暴饮样行为。在受训为按杠杆获取酒精的大鼠中,BP1.3656B 大幅减少了它们的饮酒量以及为获得酒精所付出的努力,无论是在单纯的嗜酒动物还是在被诱导产生身体依赖的动物中。它还减弱了类似复发的饮酒行为并缓解了与戒断相关的焦虑。综述这些结果表明,该药可能降低对酒精的动机并有助于防止重度饮酒的复发。
早期人体试验:药物能到达其靶点吗?
接下来是对健康志愿者的 I 期研究。单次和重复给药至多 90 微克总体耐受良好,主要出现与睡眠相关的轻微副作用,这与 H3 阻断剂的唤醒促进效应相符。血液测定显示了药物吸收和清除的清晰、可预测的模式。为了确认它在活体人脑中是否到达预期靶点,团队使用了正电子发射断层扫描,这是一种可以显示药物占据多少受体的脑部扫描方式。即使是相对较低剂量的 BP1.3656B 也在多个与动机和奖赏相关的重要脑区阻断了大部分 H3 受体,证实了至少在生物学层面上,该药在发挥其设计目的。
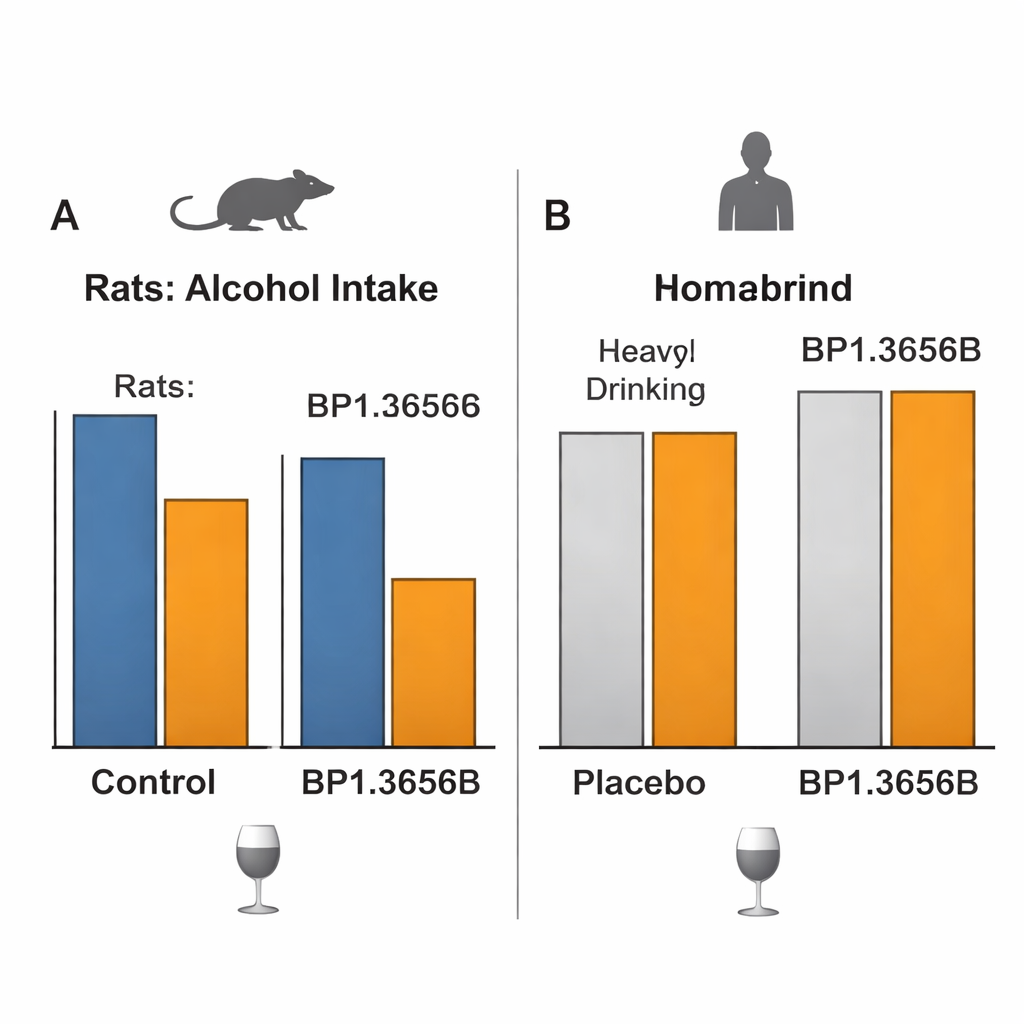
动物研究有前景却未能转化为人类效果
关键问题是,所有这些能否转化为对酒精使用障碍患者饮酒行为的有意义改变。在一项精心控制的实验室研究中,非寻求治疗的有酒精问题的成年人接受了 BP1.3656B 或安慰剂,然后完成了可通过按按钮自我输注静脉酒精的环节,条件设计用于测量享受程度和动机。该药对他们选择接收的酒精量没有可检测的影响。随后一项规模更大、为期 12 周、跨国的临床试验在寻求治疗的患者中测试了三种每日剂量的 BP1.3656B 与安慰剂的比较。包括安慰剂组在内的所有组随时间均显著减少了重度饮酒日和总体酒精摄入量,但尽管安全性良好且明确占据了靶点,该药在任何主要的饮酒或渴求指标上均未优于安慰剂。
这对未来治疗意味着什么
对非专业读者而言,结论令人清醒但重要:一种在细胞、小鼠和大鼠中表现出色并且明确到达人脑靶点的药物,仍未能帮助人们减少饮酒。这并不意味着科学本身是错误的,但它突出了仅依赖动物模型来预测人类结果的不确定性。作者们主张应更常规地使用规模较小的早期人体实验室研究,直接检验药物对酒精使用的影响,以在大型昂贵试验之前降低开发风险。换句话说,这项工作表明我们不仅需要新的药物思路,还需要更好的方法来判定哪些想法真正有可能帮助正在与酒精使用障碍作斗争的人们。
引用: Le Foll, B., Naassila, M., Jeanblanc, J. et al. Histamine H3 Receptor as a target for alcohol use disorder: challenging the predictability of animal models for clinical translation in drug development. Transl Psychiatry 16, 55 (2026). https://doi.org/10.1038/s41398-026-03807-y
关键词: 酒精使用障碍, 组胺 H3 受体, BP1.3656B, 成瘾治疗, 转化研究