Clear Sky Science · zh
光合细菌铜蓝蛋白肽抑制线粒体能量生成以阻断肿瘤生长
将细菌变为抗癌武器
癌细胞极度需要能量。它们依赖名为线粒体的小型“发电站”来产生生长、扩散并抵抗治疗所需的能量。本研究探讨了一种出人意料的抗癌盟友:来源于光合细菌的一段短蛋白片段。研究者表明,这种设计肽能渗入癌细胞,在能量来源处关闭其供应,并显著增强放疗效果——同时在很大程度上不损伤正常细胞。
小肽,大使命
研究团队从早期发现出发:一种称为azurin的细菌蛋白可通过作用于著名的肿瘤抑制因子p53来减缓肿瘤生长。随后他们考察了生活在人体肿瘤周围的细菌,重点关注利用光产生能量的光合微生物。这些细菌携带一类相关的蛋白——铜蓝蛋白。通过比较结构与进化历史,研究者锁定了其中一种铜蓝蛋白auracyanin B,并截取出一段28个氨基酸的短区段,命名为aurB。该片段可溶于水,能穿过细胞膜,且构象暗示它可能与细胞内关键的能量产生装置发生相互作用。
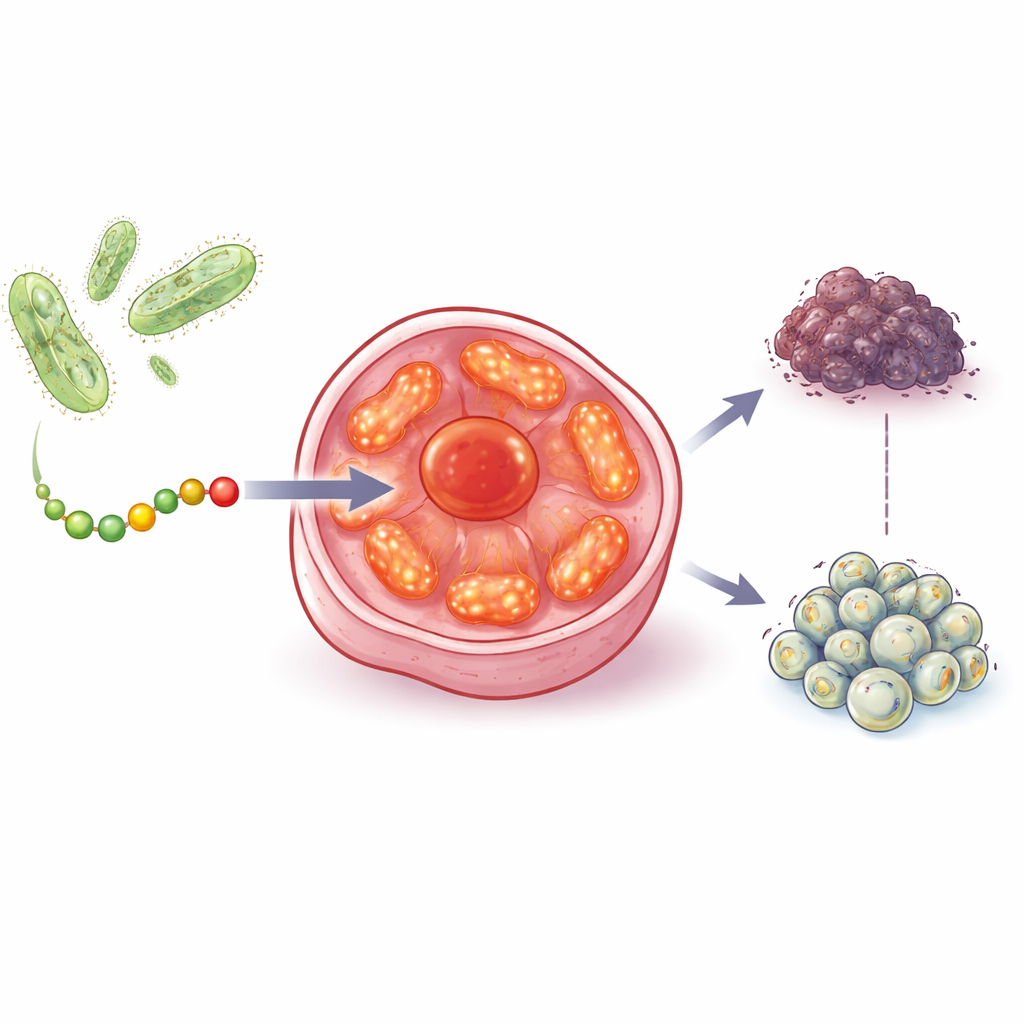
寻找并打击癌细胞的能量工厂
在体外实验中,aurB降低了乳腺癌、前列腺癌、结肠癌和卵巢癌细胞系的存活率,即便这些细胞缺失功能性p53或许多现有药物所依赖的激素受体。重要的是,aurB对富含线粒体的正常前列腺、心脏和肌肉细胞的影响要弱得多。成像实验显示,aurB更易进入癌细胞并在其线粒体内富集。借助将aurB连接到微小金棒作为可视化把手的电子显微镜观察,证实该肽确实在这些细胞器内积累。
切断能量供应
一旦进入线粒体,aurB与ATP合酶的一个特定成分结合——ATP合成的分子涡轮是产生细胞主要能量货币ATP的装置。生化拉下(pull-down)实验和质谱鉴定出该结合伙伴为ATP5C,属于酶的核心成分。表面等离子体共振测量显示,aurB与ATP5C以中等结合力且释放缓慢的方式结合,符合稳定相互作用。功能性检测进一步揭示了这种结合的后果:aurB显著降低了前列腺癌细胞的线粒体ATP水平,减缓了其耗氧速率,并阻断了呼吸以及作为后备的糖酵解通路。随着能量生成崩溃,癌细胞表现出由关键执行蛋白酶caspase-3驱动的程序性细胞死亡特征。
阻断肿瘤并增强放疗效果
研究者接着在攻击性前列腺癌的小鼠模型中测试了aurB。在皮下异种移植有人类前列腺肿瘤的动物体内,定期注射aurB使肿瘤生长缩小约三分之二,可与或优于化疗药物紫杉醇的效果,同时没有明显的体重下降或痛苦迹象。来自处理组小鼠的肿瘤样本显示增殖细胞减少而死亡细胞增多。在第二个模拟骨转移(前列腺癌常见且致命的转移位点)的模型中,单用aurB也减缓了腿骨内肿瘤扩展并减少了肺转移数量。然而,当与适度剂量的放疗联合使用时,效果惊人:受治疗肢体内的肿瘤几乎被消灭,且与对照组相比肺转移减少超过90%。
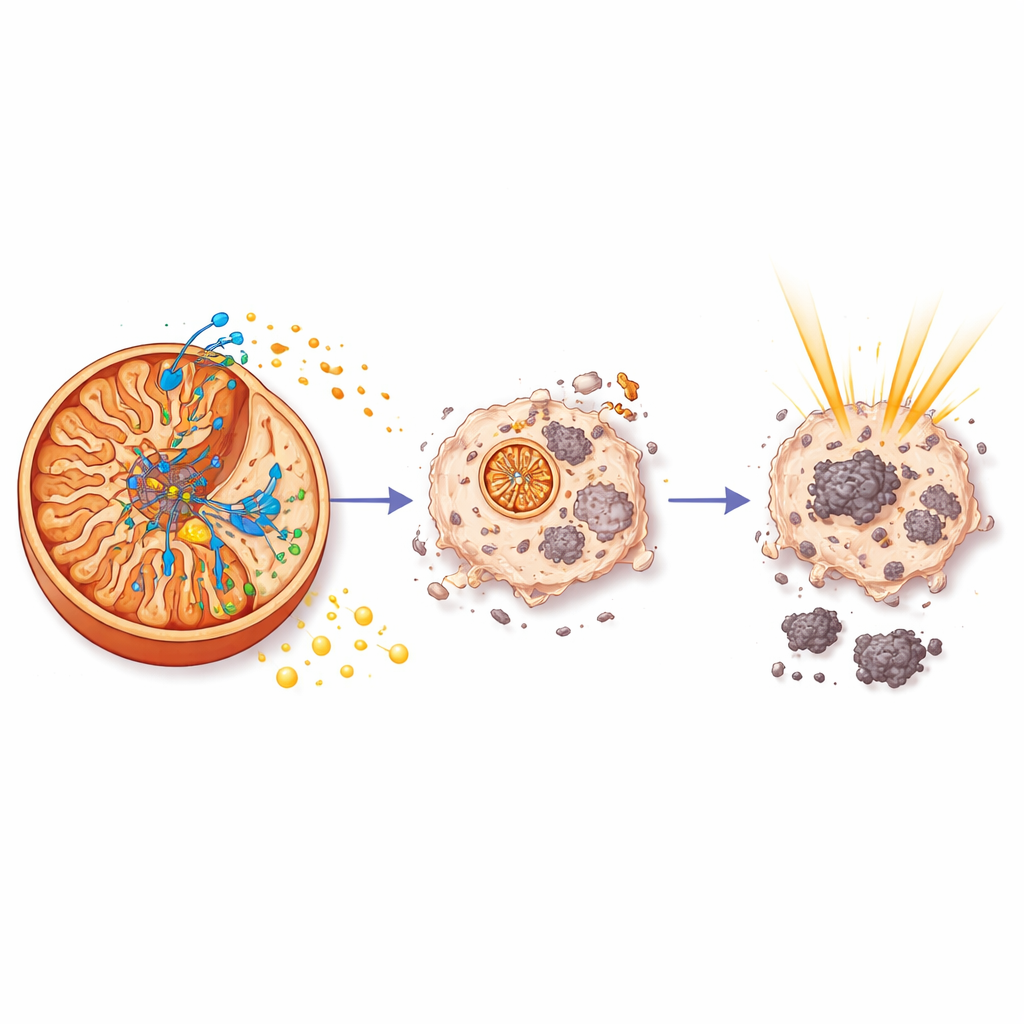
为何能量对放疗至关重要
为理解aurB为何能增强放疗,团队检查了处理后小鼠肿瘤的基因活性。他们发现aurB(而非单独放疗)抑制了一组由HIF-1控制的基因网络,HIF-1是帮助癌细胞适应低氧并促进治疗抗性的主控因子。在aurB制造的能量匮乏条件下,由PI3K和c-Myc驱动的关键生长与存活通路被下调,支持肿瘤在恶劣环境中生存的糖酵解机制也被抑制。实质上,通过在线粒体涡轮处直接破坏ATP产生,aurB将癌细胞推入能源危机,使其对放射损伤更加脆弱。
一种新型的精确能量阻断剂类别
这项工作提出了一种新的癌症治疗策略:设计受细菌启发的小型肽,靶向肿瘤中被改变的线粒体能量系统。源自光合细菌蛋白的aurB选择性地作用于ATP合酶的一个成分,该成分在前列腺、乳腺、卵巢和脑肿瘤等癌症中常呈过度活跃状态。通过直接使癌细胞断粮并削弱其防御,尤其是对放疗的防御,这类肽可以补充现有治疗,并为免疫疗法效果有限的情况提供选择。尽管在转入临床之前仍需大量工作,这项研究表明,古老的细菌能量蛋白可以被改造为现代、高度靶向的抗癌工具。
引用: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
关键词: 线粒体ATP合酶, 癌症代谢, 治疗性肽类, 前列腺癌, 放射增敏