Clear Sky Science · zh
神经生长因子信号激活限制了乐伐替尼在肝细胞癌中的疗效
为什么这个癌症研究重要
肝癌是全球致死率很高的癌症之一,即便有现代药物,许多患者在一段时间获益后仍会出现疗效丧失。该研究探究了为何一种广泛使用的药物——乐伐替尼——在晚期肝瘤中常常失去作用。研究人员发现了一个来自神经生物学领域的意外“同谋”——神经生长因子(NGF),并展示了阻断这一信号如何可能帮助现有治疗延长并提高疗效。
当有效药物失去动力时
乐伐替尼是一种口服药,通过切断生长信号和血供来减缓肿瘤生长,已成为无法手术切除肝癌患者的主要治疗手段。然而,大多数肿瘤最终会“学会”与药物共存,患者生存期并未达到期望的改善。为在更真实的条件下研究这一问题,团队在小鼠体内培养了人体肝肿瘤,给予乐伐替尼治疗,然后将存活的肿瘤细胞在动物与培养皿之间反复传代。经过数个循环,他们获得了对该药极难杀灭的细胞群体,逼真地模拟了临床中观察到的耐药性。
一个暗中喂养肿瘤的神经信号
研究人员利用这些耐药细胞周围的培养液线索,寻找细胞分泌到环境中的蛋白质。其中一个分子尤为突出:神经生长因子(NGF),它以指导神经元生长与存活而闻名。随着细胞变得更耐药,它们稳定地分泌更多NGF。当将这种富含NGF的培养液加入先前敏感的细胞时,这些细胞也变得更难以被乐伐替尼杀灭。单独加入纯化的NGF就足以削弱药物效应,而其它生长因子并未产生相同影响。在耐药细胞中敲除NGF能恢复其对治疗的敏感性并在小鼠中减缓肿瘤生长,尤其是在联用乐伐替尼时更明显。在患者样本中,曾在乐伐替尼治疗后持续存在或复发的肿瘤显示出比未治疗肿瘤更高的NGF水平,且肿瘤NGF高的患者生存较差。
肿瘤细胞如何重接其内在机器
研究团队接着探究肝癌细胞如何在不改变基因序列或减慢蛋白降解的情况下提高NGF产量。他们在NGF的RNA剪接与组装中找到了答案。NGF基因可以被处理成长或短两种信使RNA版本。在对药物敏感的细胞中,长型占主导;而在耐药细胞中,短型占上风且被翻译成蛋白的效率更高。一个名为SRSF1的剪接蛋白特异性结合定义短型的RNA区域。而SRSF1的活性又受到一种激酶SRPK1的增强,SRPK1通过添加磷酸基并促进SRSF1进入细胞核来帮助剪接过程。在耐药细胞中,SRPK1上调,SRSF1在细胞核内更为活跃,NGF的高产RNA版本被偏向产生,从而驱动NGF蛋白大量分泌。
一种躲避药物的信号开关
NGF通过结合肿瘤细胞表面的受体TrkA发挥作用。当耐药细胞中的TrkA被激活时,它会重新导向细胞内的生长信号流向。在正常情况下,肝癌细胞主要依赖一条经典的蛋白级联通路——通常称为ERK1/2途径——来驱动生长。乐伐替尼擅长破坏这条主要通路。但在被NGF充斥的耐药细胞中,TrkA偏向激活一条平行通路,终点是名为ERK5的蛋白。随着乐伐替尼关闭常规通路,肿瘤悄然将依赖转向ERK5路线,维持生长和存活信号。与乐伐替尼联合阻断TrkA或ERK5,在长期生长实验中能显著提高对耐药细胞的杀伤力,而对药物敏感细胞影响不大。在耐药的早期阶段,像EGF受体等其他信号更为重要,但随着耐药加深,NGF–TrkA–ERK5通路成为主导的逃逸通道。
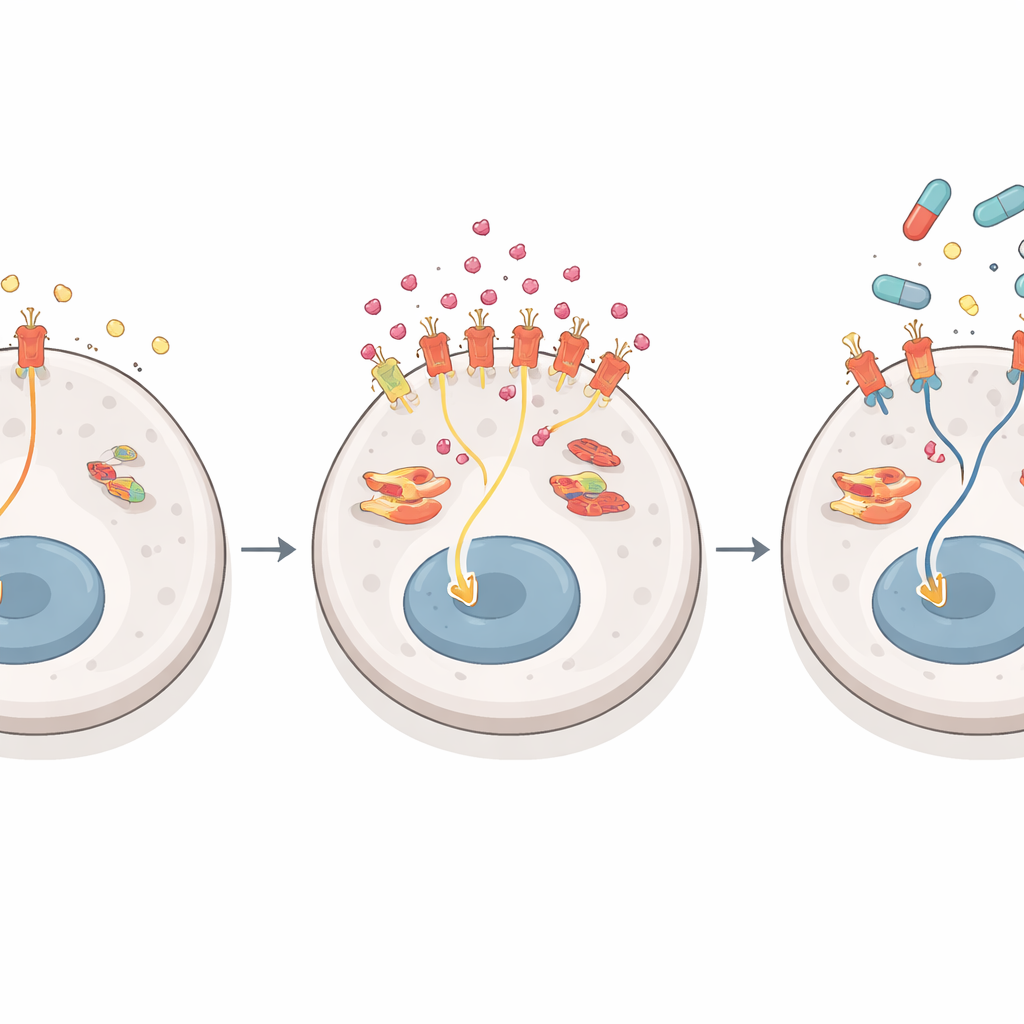
将一个弱点转化为新的治疗方案
由于SRPK1在健康细胞中有多种作用,作者将注意力集中在更实际的靶点TrkA上。他们测试了larotrectinib(一种已获批用于某些由TRK基因融合驱动肿瘤的药物)。在肝脏中过表达SRPK1的鼠模型中,一旦NGF水平上升,单用乐伐替尼几乎无法抑制肿瘤,而单用larotrectinib的疗效也仅属温和。但两药联合能强烈缩小肿瘤且未见明显额外毒性。在来自患者的肿瘤移植模型和来自那些对乐伐替尼产生耐药且肿瘤NGF高的个体培养的迷你肿瘤中,larotrectinib恢复了对乐伐替尼的敏感性,两药联用的效果远优于单药。相比之下,NGF低的肿瘤仍可被单用乐伐替尼良好控制,加入larotrectinib带来的益处有限。
这对患者意味着什么
这项工作表明,一些肝癌通过开启类似神经的生长回路来逃避乐伐替尼:SRPK1和SRSF1重塑NGF的RNA,提升NGF产量;NGF进而激活TrkA并将肿瘤的内部线路切换到乐伐替尼难以阻断的备用通路。令人鼓舞的是,这种重接也暴露出一个新的脆弱点。将现有的TrkA抑制药与乐伐替尼联合使用——特别是针对肿瘤显示NGF高或TrkA活性高的患者——可能在安全可控的范围内重新使耐药癌恢复敏感。如果这一策略在临床试验中得到验证,一项简单的组织检测NGF或TrkA活性就能指导医生为晚期肝癌患者制定更个体化的联合治疗方案。
引用: Xu, M., Zheng, Y., Zhao, L. et al. Activation of Nerve Growth Factor signaling limits the response to lenvatinib in hepatocellular carcinoma. Sig Transduct Target Ther 11, 120 (2026). https://doi.org/10.1038/s41392-026-02649-w
关键词: 肝细胞癌, 药物耐受, 神经生长因子, 靶向治疗, 乐伐替尼