Clear Sky Science · zh
前列腺素E2驱动的施旺细胞去分化导致胰腺导管腺癌的神经周侵袭
当癌症沿着神经蔓延
胰腺癌以致命著称,部分原因在于它不仅以肿块形式生长——常通过沿邻近神经爬行的方式扩散,这一过程称为神经周侵袭。这个隐蔽的通路与疼痛、早期转移和更差的生存率相关,但临床上仍缺乏良好的预测或阻断手段。本文所述研究揭示了胰腺肿瘤如何化学性地“重编程”包裹神经的支持细胞,使其成为帮助癌细胞侵袭的活跃共犯。理解这种神经—肿瘤的协作关系,可能为缓解疼痛和延缓疾病提供新思路。
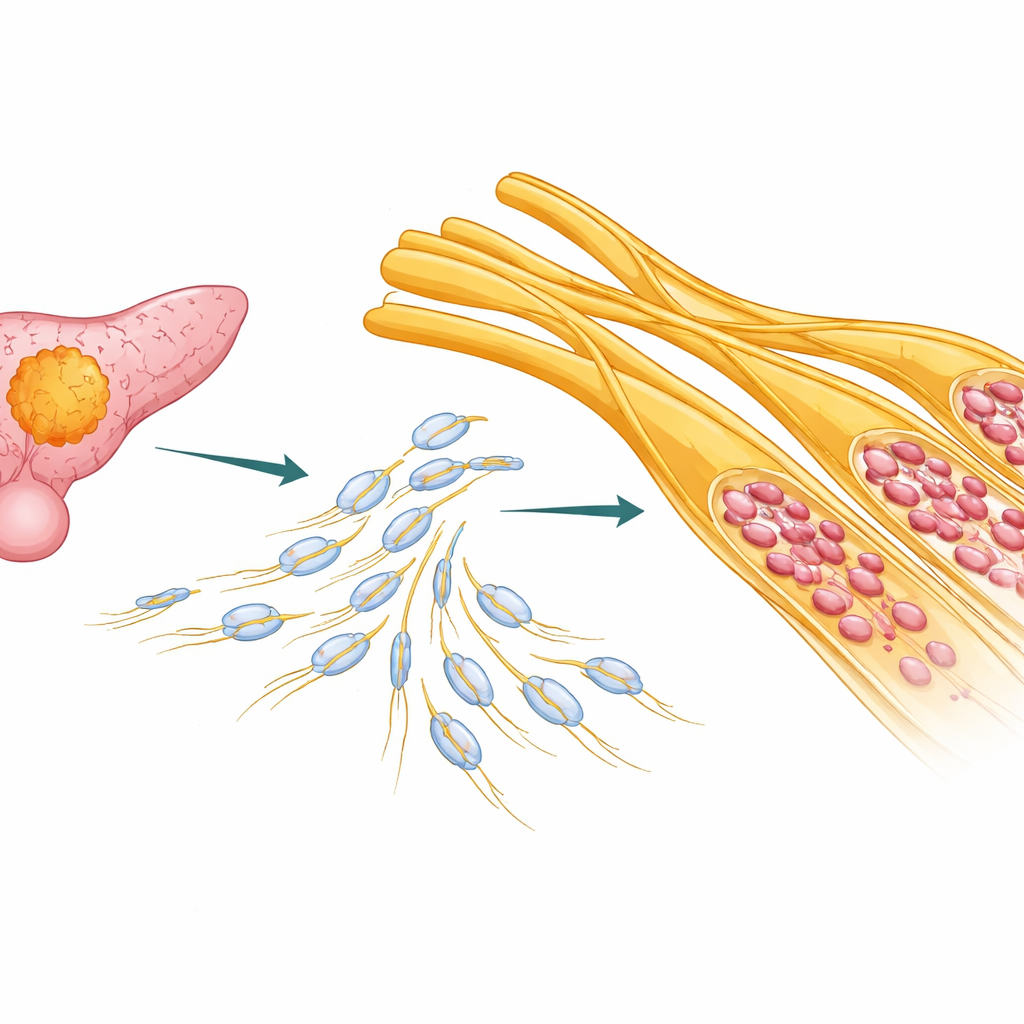
胰腺内部的隐秘高速公路
在许多胰腺导管腺癌患者中,癌细胞并非只是侵入邻近组织;它们环绕并沿着神经移动。作者分析了来自一百多名患者的肿瘤样本和公开的癌症数据库,发现神经侵袭更严重的患者往往预后更差,尤其是在分子亚型较不侵袭性的患者中更为明显。这提示神经周侵袭并非单纯的副作用,而是推动病程进展的重要因素,应影响患者的风险分层和治疗决策。
倒戈的支持细胞
体内神经由施旺细胞包裹和保护,施旺细胞也是损伤后帮助神经修复的一类支持细胞。在胰腺癌组织中,研究者使用先进的RNA测序、空间转录组学和单细胞分析绘制了不同细胞类型的位置分布及其基因表达。他们发现一种类似于损伤后“修复”状态的施旺细胞恰好集中于被肿瘤侵袭的神经区域。这些细胞表现出去分化的特征:失去了正常的绝缘功能,变得细长、可迁移且高度活跃,表达诸如p75NTR、SOX2和c‑Jun等标志物。
来自肿瘤到神经的化学信号
为弄清促使施旺细胞进入这种修复样、促侵袭状态的驱动因子,研究团队在体外共培养体系中将胰腺癌细胞与施旺细胞共同培养。他们发现癌细胞增强了施旺细胞的运动性、改变其形态并激活去分化相关基因。多层次的遗传学分析指向了一个肿瘤酶作为关键元凶:PTGES,它产生脂类信使前列腺素E2(PGE2)。PTGES在靠近被侵袭神经的肿瘤区域特别高表达,且在癌细胞与施旺细胞共培养时PGE2水平上升。当研究者用小分子抑制剂阻断PTGES或通过基因敲除时,PGE2水平下降,施旺细胞激活与迁移显著减少。

被重编程的细胞如何打开通路
将纯化的PGE2直接加入施旺细胞培养中,会使它们呈现出修复状态典型的细长双极形态并上调去分化标志物。在三维培养中,这些改变后的细胞朝向胰腺癌簇和类似神经的结构伸展,实质上构建出引导肿瘤细胞的细胞“轨道”。进一步放大观察发现,经PGE2刺激的施旺细胞分泌出高水平的两种关键蛋白:促神经生长与重塑的白血病抑制因子(LIF)和有助于分解周围细胞外基质的酶ADAMTS‑1。这些分泌因子共同削薄了包绕神经的物理屏障并促进新的神经萌发,创造出柔软、重塑的通道,便于癌细胞沿其移动。
将机制转化为治疗构想
动物实验支持了这一图景:当胰腺癌细胞先被施旺细胞“预激活”后,肿瘤在小鼠体内生长得更大,并导致更多的神经损伤与肢体无力。阻断PTGES或中和LIF的治疗减少了肿瘤负担、降低了神经侵袭并改善了神经功能,同时在显微镜下也保留了神经的髓鞘结构。由此形成的总体模型是一个旁分泌回路:胰腺肿瘤释放PGE2,将施旺细胞重编程为修复样、易于侵袭的状态;这些细胞继而分泌LIF和ADAMTS‑1,重塑神经及周围组织,为癌细胞沿神经扩散铺平道路。对患者而言,这项工作提示针对PTGES–PGE2–施旺细胞轴或阻断LIF的药物,未来可能有助于减轻神经侵袭、缓解疼痛并减缓胰腺癌进展。
引用: Wang, L., Liu, Q., Zhang, Z. et al. Prostaglandin E2-driven dedifferentiation of Schwann cells leads to perineural invasion in pancreatic ductal adenocarcinoma. Sig Transduct Target Ther 11, 122 (2026). https://doi.org/10.1038/s41392-026-02648-x
关键词: 胰腺癌, 神经周侵袭, 施旺细胞, 前列腺素E2, 肿瘤微环境