Clear Sky Science · zh
不可逆电穿孔与CAR-NK细胞疗法对肝细胞癌的协同免疫治疗作用
用电与免疫细胞共同对抗肝癌
肝癌,尤其是肝细胞癌,是全球致死率很高的一类癌症,且治疗难度大。许多患者不适合手术治疗,即使局部消融肿瘤,肿瘤也常常复发。本研究探讨了一种新策略,将一种用短电脉冲袭击肿瘤的医疗装置与下一代免疫细胞疗法相结合,旨在赋予机体防御系统对抗癌症的持久优势。
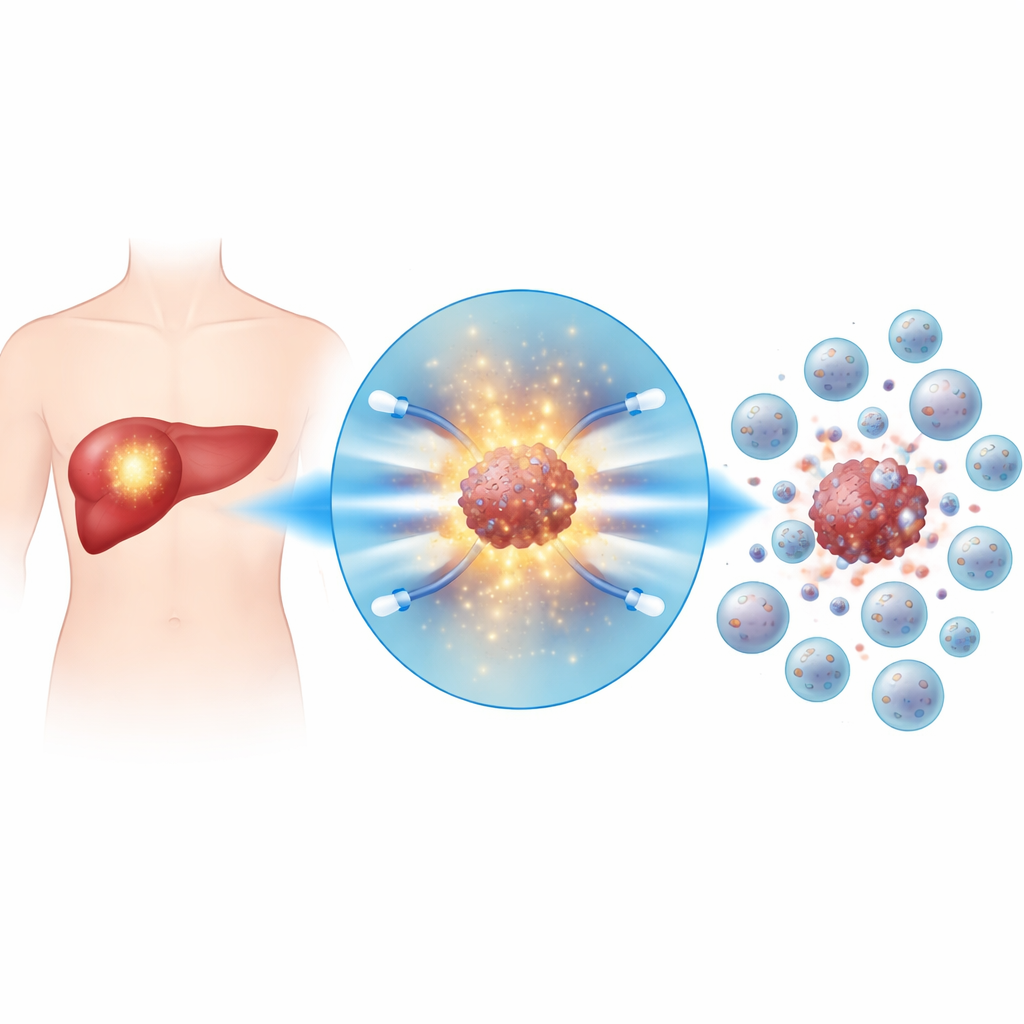
为什么肝脏肿瘤难以对付
肝脏肿瘤并非仅作为孤立的肿块生长;它们还会改造周围环境,使之成为免疫不利区。在这种环境中,有益的免疫细胞(例如自然杀伤细胞,NK细胞)难以进入并发挥功能。NK细胞是机体对异常细胞的快速反应防线,但在肝癌中常常数量不足且功能受损。热消融或化疗等常规治疗虽能缩小肿瘤,却很少能修复这种不利的免疫微环境,这也是复发频繁的原因之一。
用电脉冲唤醒免疫系统
研究人员关注了一种称为不可逆电穿孔的技术,该技术将极短的高压脉冲直接施加到肿瘤组织中。与热灼不同,这些脉冲在癌细胞膜上打出微小且永久的孔洞,使细胞以一种释放警示信号的方式死亡。在肝癌小鼠模型中,该操作引发肿瘤内趋化因子大量涌现,并在数小时内吸引了免疫细胞浪潮,尤其是NK细胞。同时,电脉冲提高了幸存癌细胞内的活性氧水平(高反应性分子),使其更易被NK细胞清除。
打造更聪明的杀伤细胞
为进一步增强此效应,研究团队制造了携带嵌合抗原受体(CAR)的强化NK细胞,该CAR识别糖蛋白3(glypican-3),这是一种常在肝癌细胞上高表达的蛋白。他们没有使用病毒载体来转入基因指令,而是采用特制的脂质纳米颗粒——带正电修饰的小型脂质递送载体——高效将信使RNA运入NK细胞。这种方法能够相对快速且安全地生产CAR-NK细胞。在体外培养和来源于患者的肝癌类器官中,这些工程化NK细胞在遇到先经电脉冲处理的肿瘤细胞时表现出特别强的杀伤力,导致的细胞死亡多于任一单独方法。
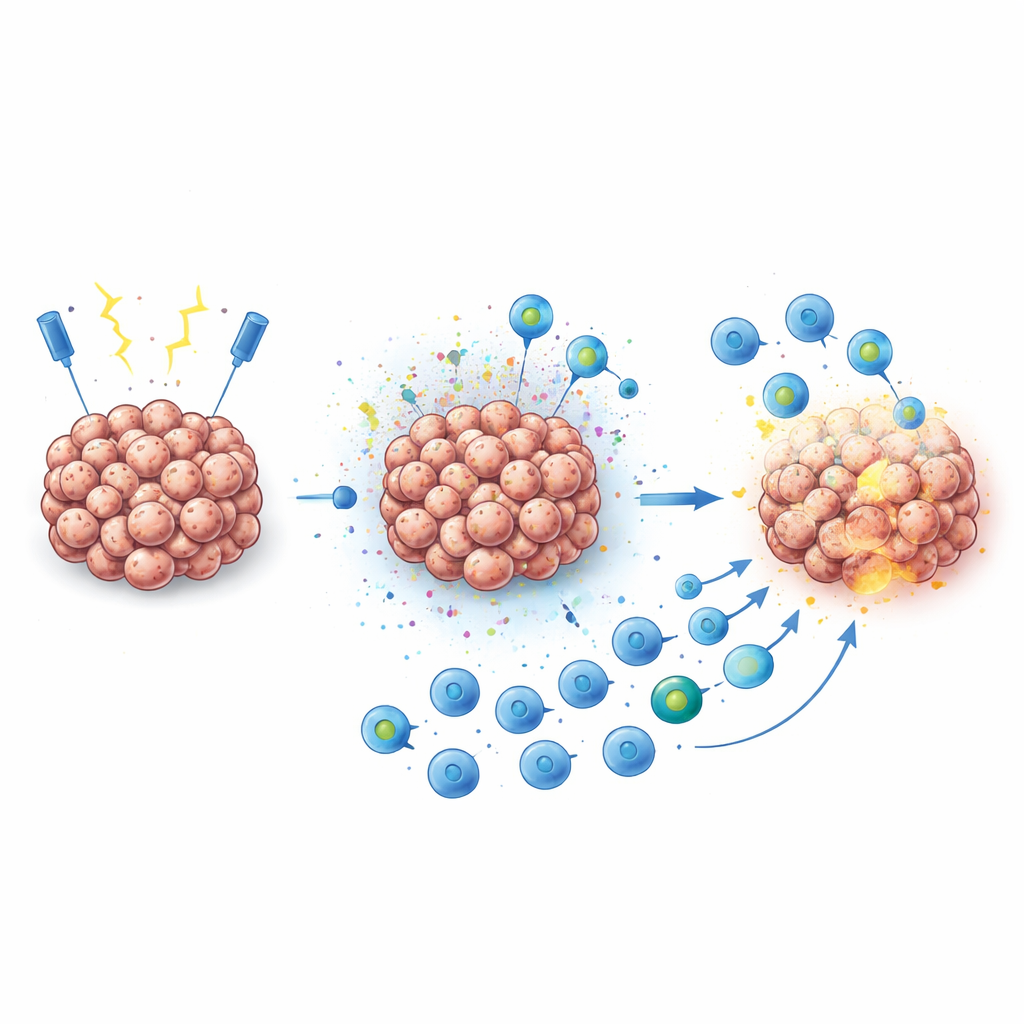
活体模型中更强的肿瘤控制
接着在多种小鼠模型中检测了联合疗法,包括生长在肝脏内的肿瘤和移植于皮下的人源肝肿瘤。单独使用不可逆电穿孔仅能有限延缓肿瘤生长,单独给与CAR-NK细胞在这些实体瘤中效果也有限。然而,当两者结合时,肿瘤收缩更显著,部分小鼠达到无肿瘤状态,且生存期延长,同时未见对健康器官的明显损伤或显著体重下降。血液检测显示,常被癌症扰动的肝功能指标在联合治疗后趋向正常。
建立持久的免疫记忆
除了即时的肿瘤缩小,研究者还考察了该策略是否能训练更广泛的免疫系统。在免疫健全的小鼠中,电脉冲与CAR-NK细胞的联合提高了树突状细胞的数量和活化水平(树突状细胞是T细胞的“教师”),并在肿瘤内增加了辅助性和杀伤性T细胞的存在。在脾脏中,更多的杀伤性T细胞对肿瘤抗原产生了特异性应答,表明该治疗有助于机体学习并记住肿瘤特征。这种协调的免疫反应暗示出可能更持久的防御,有助于防止肿瘤再生长。
这对未来患者意味着什么
总体而言,研究表明将肿瘤电穿孔与精确制导的NK细胞组合,既能裂解肝肿瘤又能动员免疫系统。电脉冲重塑肿瘤微环境并削弱癌细胞,而工程化NK细胞则识别独特的肿瘤标志并实施定向攻击。鉴于该装置治疗和NK细胞平台都已有临床基础,这一策略有望被切实转化为未来的治疗手段。对于难治性肝癌患者,这种联合方法或许有朝一日不仅提供局部肿瘤控制,还能建立更强、更持久的免疫防护。
引用: Park, J.D., Shin, H.E., Jang, H.J. et al. Synergistic immunotherapeutic effects of irreversible electroporation and CAR-NK cell therapy against hepatocellular carcinoma. Sig Transduct Target Ther 11, 86 (2026). https://doi.org/10.1038/s41392-026-02627-2
关键词: 肝细胞癌, 不可逆电穿孔, CAR-NK细胞, 肿瘤免疫治疗, 脂质纳米颗粒