Clear Sky Science · zh
糖皮质激素通过抑制 H4K12 乳酸化提高透明细胞肾细胞癌对 HIF-2α 抑制剂的敏感性
这项肾癌研究为何重要
透明细胞肾癌是最常见且致死率最高的肾癌类型,许多患者仍会复发或对现有药物无反应。本研究揭示了这些肿瘤对一种特定糖代谢方式及其产物乳酸的“依赖”:乳酸被用于维持驱动癌症的基因持续开启。更重要的是,研究表明一种常见药物类别——糖皮质激素(如地塞米松)——可被重新定位,用来削弱这种依赖,从而增强一种新型靶向药物 HIF-2α 抑制剂 belzutifan 的疗效。
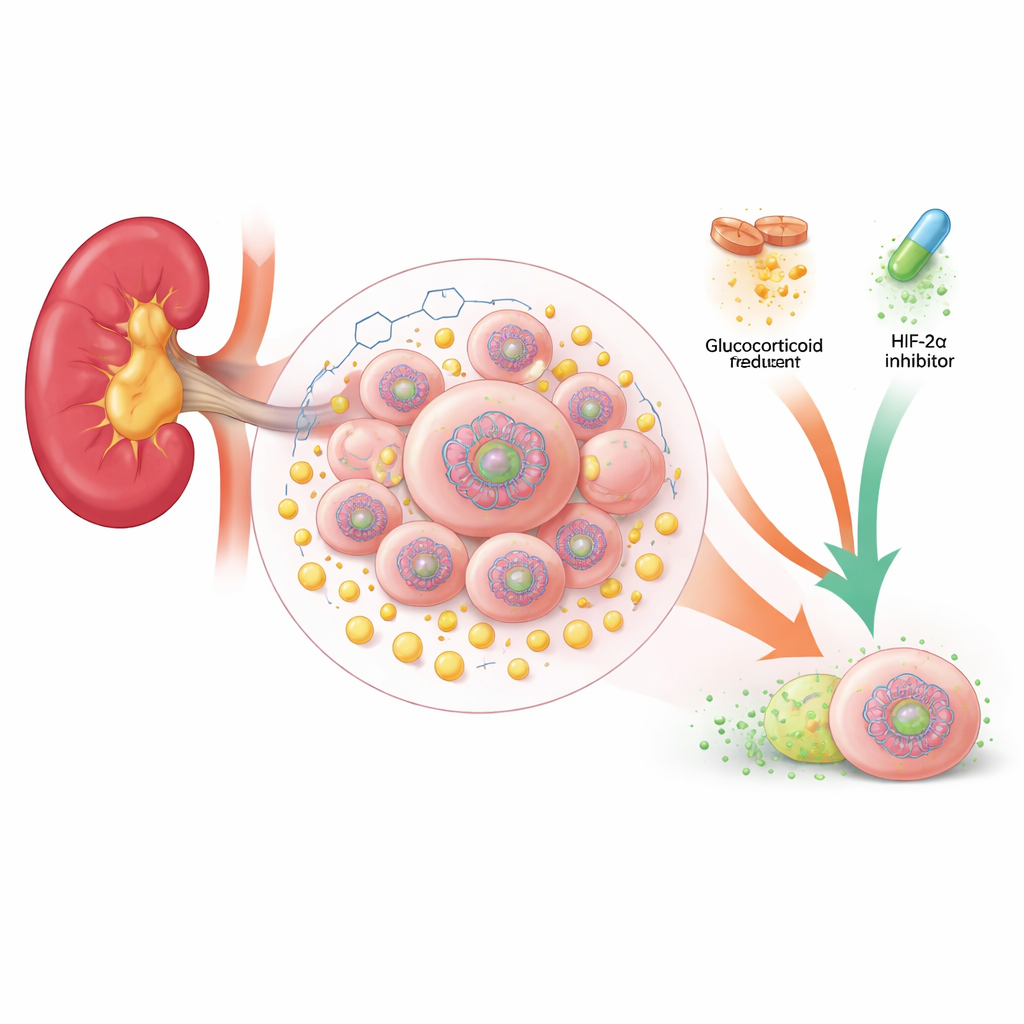
肾脏肿瘤内的糖驱动循环
许多透明细胞肾癌丧失了一个名为 VHL 的关键保护基因。没有 VHL,细胞即使在有氧的情况下也表现得像缺氧一样。它们将代谢从线粒体内的高效能量产生转向一种快速且粗放的过程——糖酵解,产生能量的同时大量生成乳酸。作者发现,在缺乏 VHL 的肾脏肿瘤中,乳酸不仅作为代谢废物积累:它进入细胞核并化学修饰包装 DNA 的蛋白质。尤其是称为 H4K12 乳酸化的标记在患者肿瘤中显著升高,并与更大、更具侵袭性的肿瘤及较差的生存相关联。
乳酸如何帮助癌基因持续开启
通过绘制这种基于乳酸的标记在癌细胞 DNA 上的位置,团队发现它大量集中在驱动肿瘤生长和糖代谢的基因“开启开关”(启动子)处。其中一个突出基因是 PGK1,该酶有助于推动糖通过糖酵解通路生成乳酸。在 VHL 缺失的细胞和小鼠模型中,PGK1 水平升高带来更多乳酸,进而在 PGK1 及其他促生长基因的染色质上产生更多 H4K12 乳酸化。这形成了自我强化的循环:PGK1 增加乳酸;乳酸在染色质上产生 H4K12 标记;该标记维持 PGK1 及其他促肿瘤基因的高活性,使癌细胞被锁定在高度糖酵解的状态。
用现有药物打破该循环
研究者接着探问是否有获批药物能削弱这一乳酸—染色质循环。在对 2,468 种 FDA 批准的化合物对肾癌细胞进行筛选时,出现了一个令人惊讶的命中名单:若干糖皮质激素显著降低了 H4K12 标记。地塞米松效力最强,即使在低剂量下也能降低 H4K12 乳酸化。这些激素通过糖皮质激素受体发挥作用,该受体在药物存在时进入细胞核并结合 DNA。在癌细胞中,糖皮质激素受体在糖酵解基因启动子的结合与 H4K12 标记的丧失以及 PGK1 等糖代谢基因活性的下降同时发生。因此,细胞产生的乳酸减少,代谢又向更接近正常的、有氧方式转变。
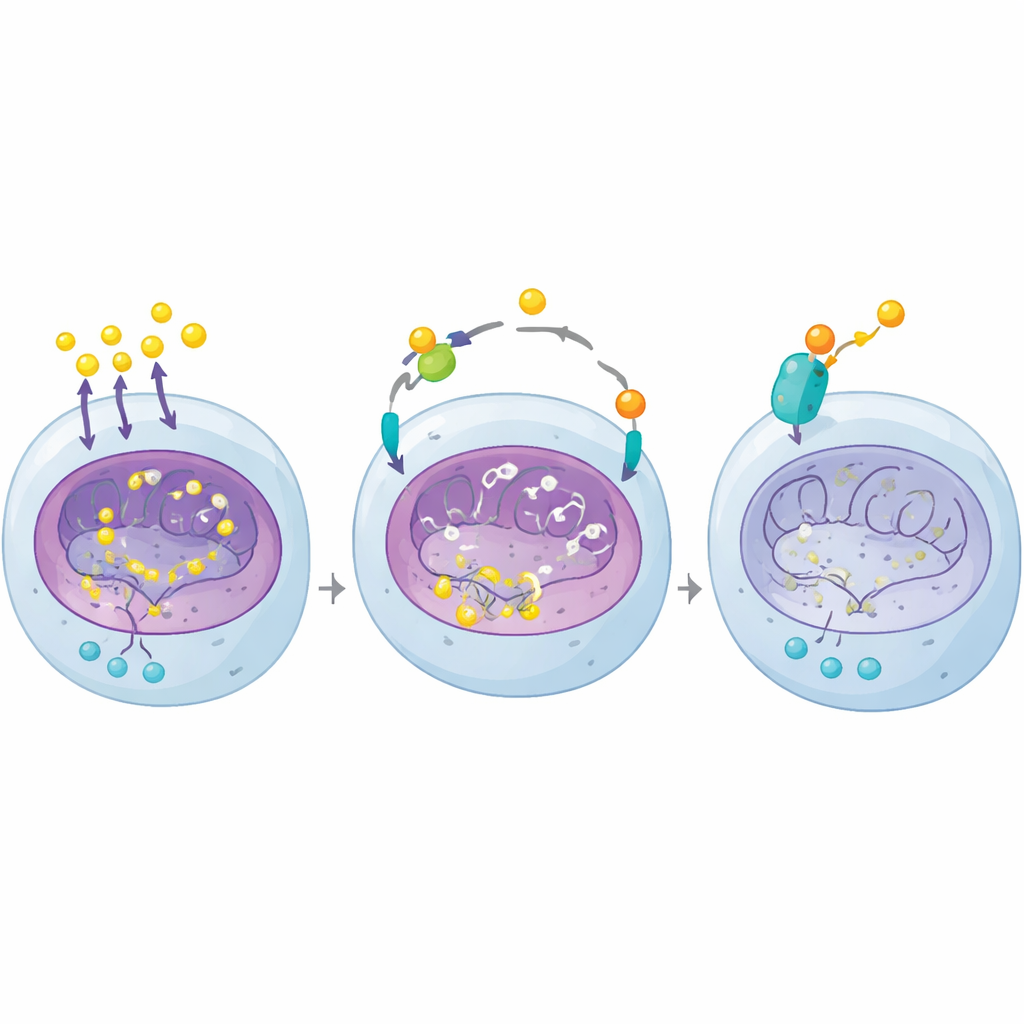
让靶向抗癌药更有效
Belzutifan 是最近获批的 HIF-2α 抑制剂,直接阻断 VHL 缺失的主要下游效应子之一,并已在晚期透明细胞肾癌患者中显示出益处。然而,疗效并不完全且常常持续时间有限。由于地塞米松从不同角度攻击癌细胞的乳酸驱动染色质程序,作者在小鼠模型中测试了两药联合。无论是来自细胞系还是患者组织的肿瘤,糖皮质激素与 belzutifan 联用比单用任一药物使 VHL 缺失肿瘤缩小得更多。该组合降低了 H4K12 乳酸化并减少了与肿瘤生长相关的关键糖酵解基因和肾系谱基因的水平,同时在动物研究中对正常组织影响较小。
对患者和未来治疗的意义
这项工作揭示,许多透明细胞肾癌被困在一个恶性循环中:VHL 缺陷驱动饥渴糖代谢,产生乳酸;乳酸化学修饰染色质,使同一组促进生长和代谢的基因持续活跃。研究表明,长期用于抗炎的糖皮质激素也可作为有针对性的表观遗传学药物,抑制这一由乳酸驱动的循环并使肿瘤对 HIF-2α 阻断更为敏感。尽管需要谨慎的临床测试——尤其是考虑到糖皮质激素可能抑制免疫系统——这些发现指向一种基于机制的可行联合策略,可能使现有靶向疗法对这种难治肾癌患者更有效。
引用: Zhang, K., He, L., Wang, Y. et al. Glucocorticoids elevate clear cell renal cell carcinoma sensitivity to HIF-2α inhibitors by suppressing H4K12 lactylation. Sig Transduct Target Ther 11, 117 (2026). https://doi.org/10.1038/s41392-026-02622-7
关键词: 透明细胞肾细胞癌, 肿瘤代谢, 组蛋白乳酸化, 糖皮质激素, HIF-2α 抑制剂 belzutifan