Clear Sky Science · zh
少突胶质细胞前体——小胶质细胞通过 BMP4 的相互作用驱动小胶质细胞的神经保护反应并缓解阿尔茨海默病
大脑自身的支持细胞如何可能有助于对抗阿尔茨海默病
阿尔茨海默病常被描述为记忆和思维的缓慢、不可阻挡的丧失。但在大脑内部,某些细胞并非旁观者——它们会主动尝试保护神经元免受损伤。本研究揭示了两类此类细胞之间出人意料的合作,并显示增强它们之间的自然对话可能有助于大脑更长时间地抵御阿尔茨海默病。
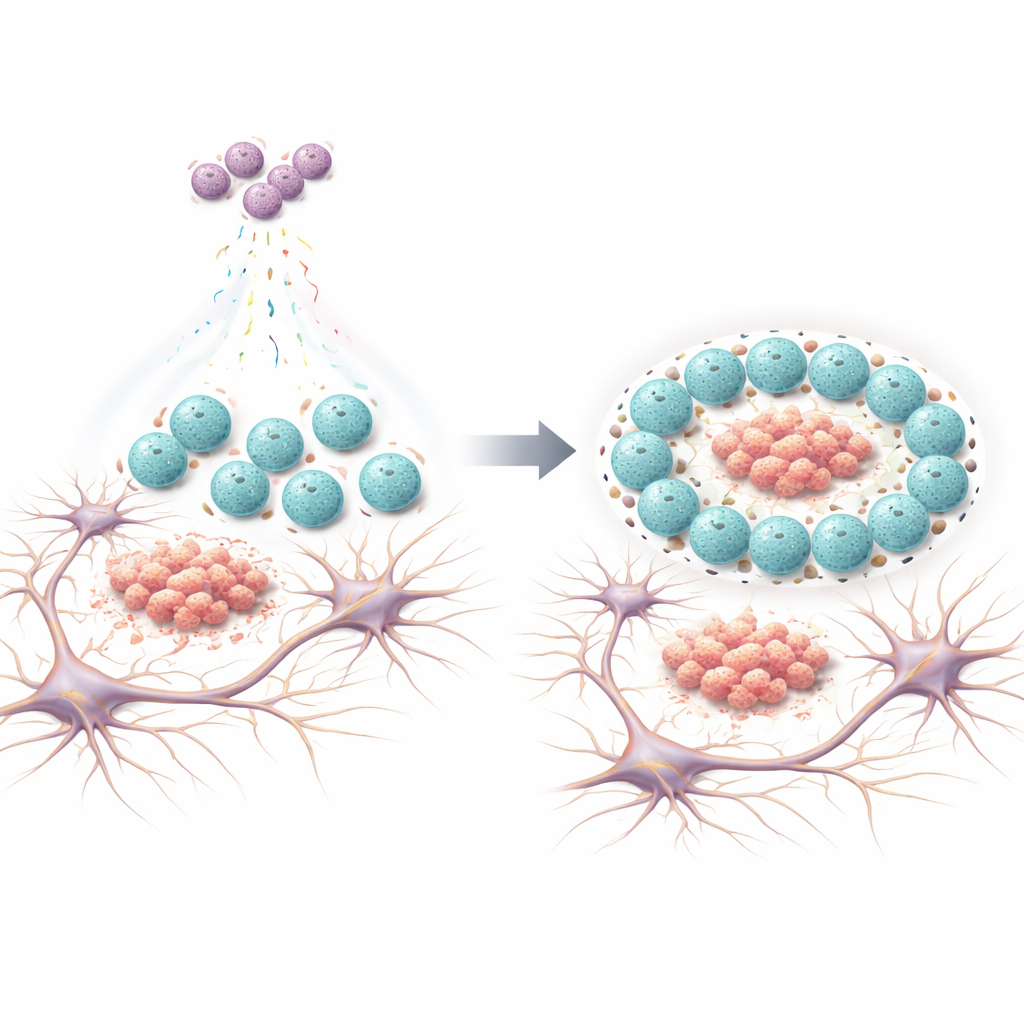
病变大脑内部的一场隐秘对话
我们的大脑包含远不止神经元。其间有少突胶质细胞前体(OPC),它们通常分化为用髓鞘包裹神经纤维的细胞,帮助信号快速传导。小胶质细胞是另一类关键细胞,像驻留的免疫巡逻者一样巡视大脑,清理垃圾并对损伤做出反应。在阿尔茨海默病早期,小胶质细胞可以采用一种“疾病相关”的保护性状态,聚集在β-淀粉样蛋白团块(斑块)周围以致密并限制它们。然而,是什么促使小胶质细胞进入这种有益状态一直不明。该研究的作者怀疑,一类特殊的 OPC 亚群——称为已承诺的少突胶质细胞前体(COPs)——可能正在发送关键的信号。
一种名为 BMP4 的保护性信号
通过研究阿尔茨海默病小鼠模型和人类脑组织,研究人员发现靠近淀粉样斑块的 COPs 会产生大量名为 BMP4 的信号分子。当斑块开始出现时,COPs 会提高 BMP4 的产生并将其释放到周围脑组织和小的膜包裹囊泡中。附近的小胶质细胞带有匹配的受体 BMPR1A,并显示对 BMP 信号特异响应的内部通路(SMAD1/5/8)被激活。随着疾病进展,产生 BMP4 的 COPs 数量下降而炎症上升,这表明这种 COP–小胶质细胞的通讯是一种早期、时限性的保护反应,随时间被耗尽。
当该信号被切断会发生什么?
为测试 COP 来源的 BMP4 是否确实对保护重要,研究团队在阿尔茨海默病模型小鼠中选择性地从 OPCs 中删除了 Bmp4 基因。这些动物最初显示出轻微改善的髓鞘覆盖,但随时间发展,它们出现了更多且更大的淀粉样斑块,以及更差的记忆表现。细胞层面的详细分析显示,这些小鼠的小胶质细胞在斑块周围聚集较少,携带的吞噬(清除)囊室减少,分支更为简单、探索性较低。关键是,决定保护性疾病相关小胶质细胞状态的基因和蛋白质——包括一个关键受体 Trem2——明显减少。斑块变得不那么致密、危害性增加,神经纤维出现更多肿胀,维持神经元间通讯的突触蛋白丧失。
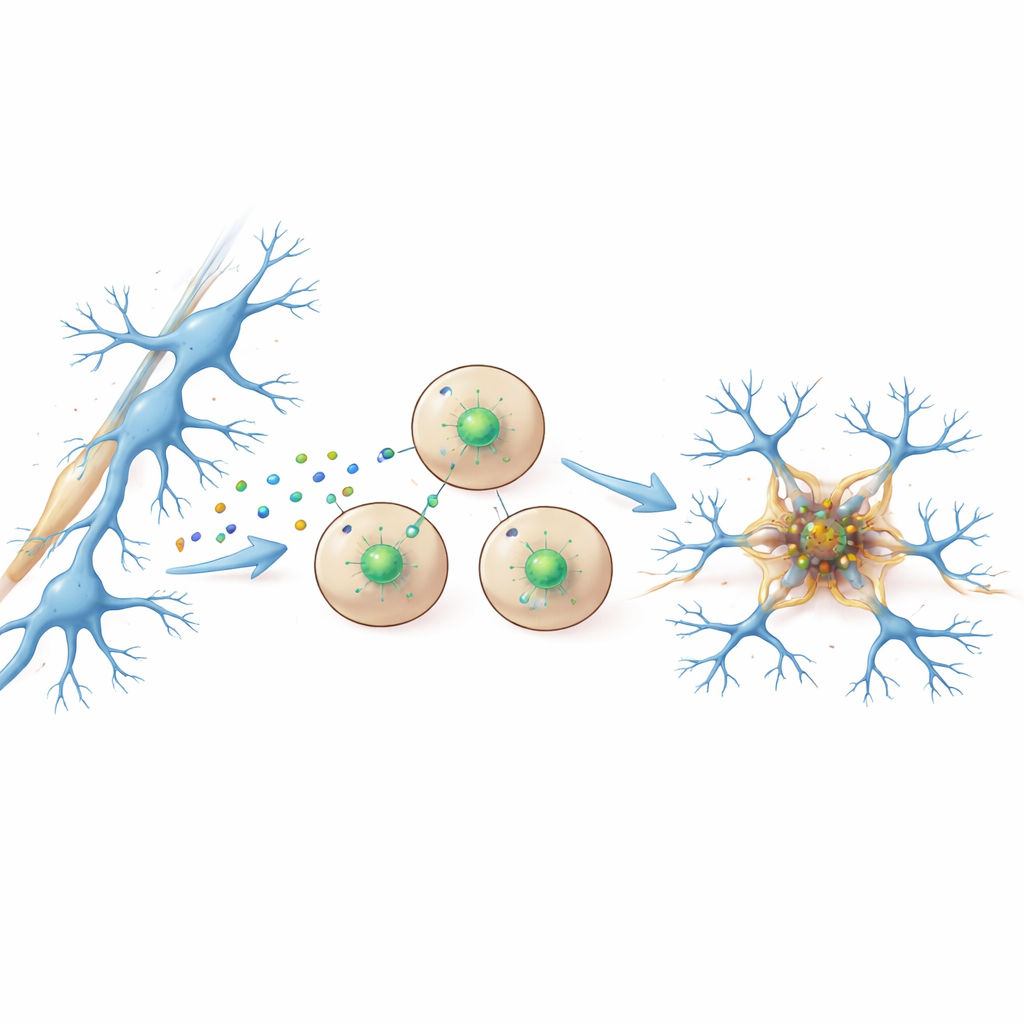
BMP4 如何将小胶质细胞调为防御者
作者随后聚焦 BMP4 如何改变小胶质细胞。在类人和小鼠小胶质细胞培养中,加入 BMP4 激活了 SMAD1/5/8 通路、提升了 Trem2 表达,并增强了小胶质细胞向淀粉样蛋白移动与吞噬的能力。阻断 BMP 受体会抹去这些益处。进一步的实验表明,SMAD 蛋白直接结合到 Trem2 基因的调控区,像手指翻开“开”关一样。当缺乏 BMPR1A 的小胶质细胞被移植到小鼠大脑时,它们未能采用保护性状态,不形成围绕斑块的紧密屏障,导致斑块更松散、更具危害性。综合这些结果揭示了一条逐步链条:COPs 感知淀粉样蛋白、分泌 BMP4、BMP4 激活小胶质细胞中的 BMPR1A–SMAD1/5/8,从而提升 Trem2 与其他基因,使小胶质细胞能够包围、致密化并清除斑块。
唤醒大脑的早期防御
由于 COPs 寿命短,研究人员探讨是否补充 BMP4 可以延长或恢复这一保护窗口。当他们向阿尔茨海默小鼠移植额外的 BMP4 产生 COPs,或使用基因治疗病毒专门在 COP 样细胞中驱动 BMP4 产生时,小胶质细胞在斑块周围变得更活跃,Trem2 水平上升,淀粉样沉积缩小并变得更致密,神经和突触损伤的迹象减少。被治疗的小鼠在记忆测试中表现更好,长期治疗也减少了随后发生的髓鞘丧失。这些发现提示,从 COPs 到小胶质细胞的 BMP4 信号通路增强,可能是一种加强大脑自身早期防御系统以对抗阿尔茨海默病病理的方法,有望推迟损伤压倒修复的时间点。
引用: Baek, S., Jang, J., Yeo, S. et al. Oligodendrocyte precursor cells–microglia crosstalk via BMP4 drives microglial neuroprotective response and mitigates Alzheimer’s disease. Sig Transduct Target Ther 11, 109 (2026). https://doi.org/10.1038/s41392-026-02620-9
关键词: 阿尔茨海默病, 小胶质细胞, 少突胶质细胞前体, BMP4 信号传导, 神经炎症