Clear Sky Science · zh
经M6A修饰的circArhgap26通过抑制plakophilin‑1棕榈酰化减轻心脏缺血–再灌注损伤
为什么在心梗后保护心脏很重要
当一个人发生心肌梗死时,医生会迅速重开阻塞的动脉以恢复血流。这一步可挽救生命,但也有负面效应:血流的突然恢复可能进一步损伤心脏,这就是所谓的缺血–再灌注损伤。本文概述的研究发现在心肌细胞内存在一种意想不到的天然保护因子—一种称为circArhgap26的环状RNA—它有助于抵御这一次生损伤波。理解这一微小分子的作用方式,可能为心脏病患者带来新的治疗方法和血液检测思路。
心脏基因脚本中的隐秘环形
我们大多数人把基因想象成线状的DNA或RNA,但细胞也会产生环状RNA,这类分子呈闭合环状,异常稳定,并能微调多种细胞过程。研究者在小鼠心脏中筛查在损伤期间表达变化的环状RNA,聚焦于一种名为circArhgap26的分子,其水平在血流中断并恢复后显著下降。他们证实该环状RNA形成闭合环,主要分布于细胞质,不作为蛋白质合成的模板。相反,它更像一种调节因子,通过与其他分子相互作用影响心肌细胞在应激后是生存还是死亡。 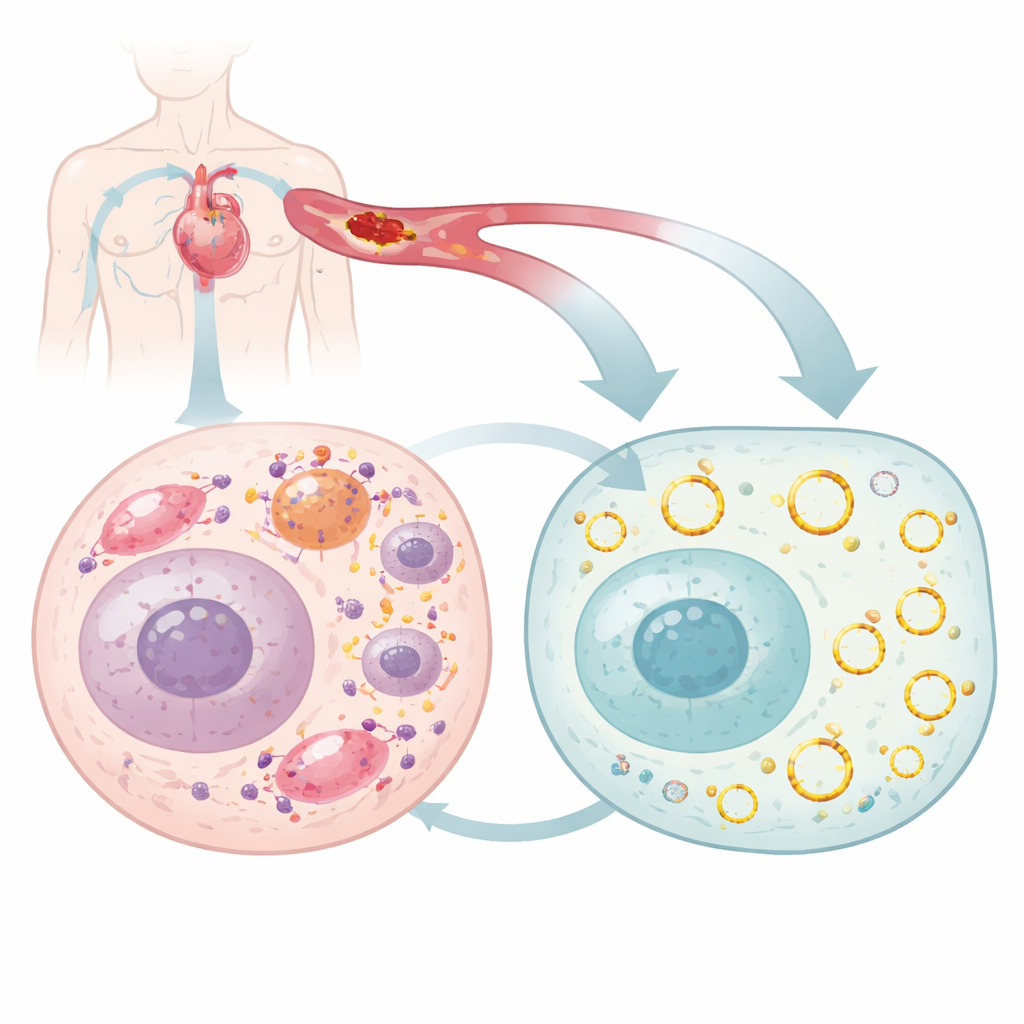
证实该环状RNA对心脏具有保护作用
为了弄清circArhgap26的实际作用,研究团队在小鼠心脏中增强或降低其表达。当他们用病毒载体在心肌细胞中特异性提高circArhgap26时,经历短暂冠状动脉阻塞并恢复血流的动物表现出更强的心脏泵功能、更小的受损区域以及更少的细胞死亡。血液和心肌组织中的经典损伤标志物也更低。相反,当该环状RNA被沉默时,即便没有人为诱导心梗,心功能也恶化、细胞死亡增加,而加入缺血–再灌注后问题更加严重。在体外的人类类心肌细胞中也出现了类似的保护效果,提示该机制在小鼠与人之间是保守的。
被约束的有害伙伴蛋白
进一步探究时,研究者询问circArhgap26如何发挥保护作用。通过生化“捕鱼”技术,他们发现它直接结合一种结构蛋白plakophilin‑1(PKP1),该蛋白能影响细胞粘附强度并调节程序性死亡的易感性。在受伤的心脏和受压的心肌细胞中,PKP1水平上升并与更严重的损伤相关。沉默PKP1可减轻心脏损伤和细胞死亡,而强制表达PKP1则使结局更差。当增加circArhgap26时,PKP1蛋白量下降,但其基因转录并未改变,表明控制发生在RNA信息传递之后。实验显示,circArhgap26通过干扰一种称为棕榈酰化的脂肪修饰过程来加速PKP1蛋白的降解,而该修饰通常能稳定PKP1。
围绕细胞死亡信号的分子拉锯战
棕榈酰化由一类酶执行;其中一种,ZDHHC1,被发现能向PKP1添加脂肪基团,从而延长其寿命。CircArhgap26在PKP1上结合的位置与ZDHHC1使用的位置重叠,形成分子层面的拉锯战。当环状RNA占上风时,PKP1获得的脂肪标记减少、稳定性下降并更快被清除。这会产生连锁反应:PKP1通常通过与另一种RNA的调控区相互作用,促进APAF1蛋白的生成。APAF1是激活caspase‑9和caspase‑3这两种细胞死亡执行酶的关键部件。随着PKP1稳定性降低,APAF1蛋白的产生减少,死亡信号级联被抑制,心肌细胞在血流恢复的应激下更有可能存活。 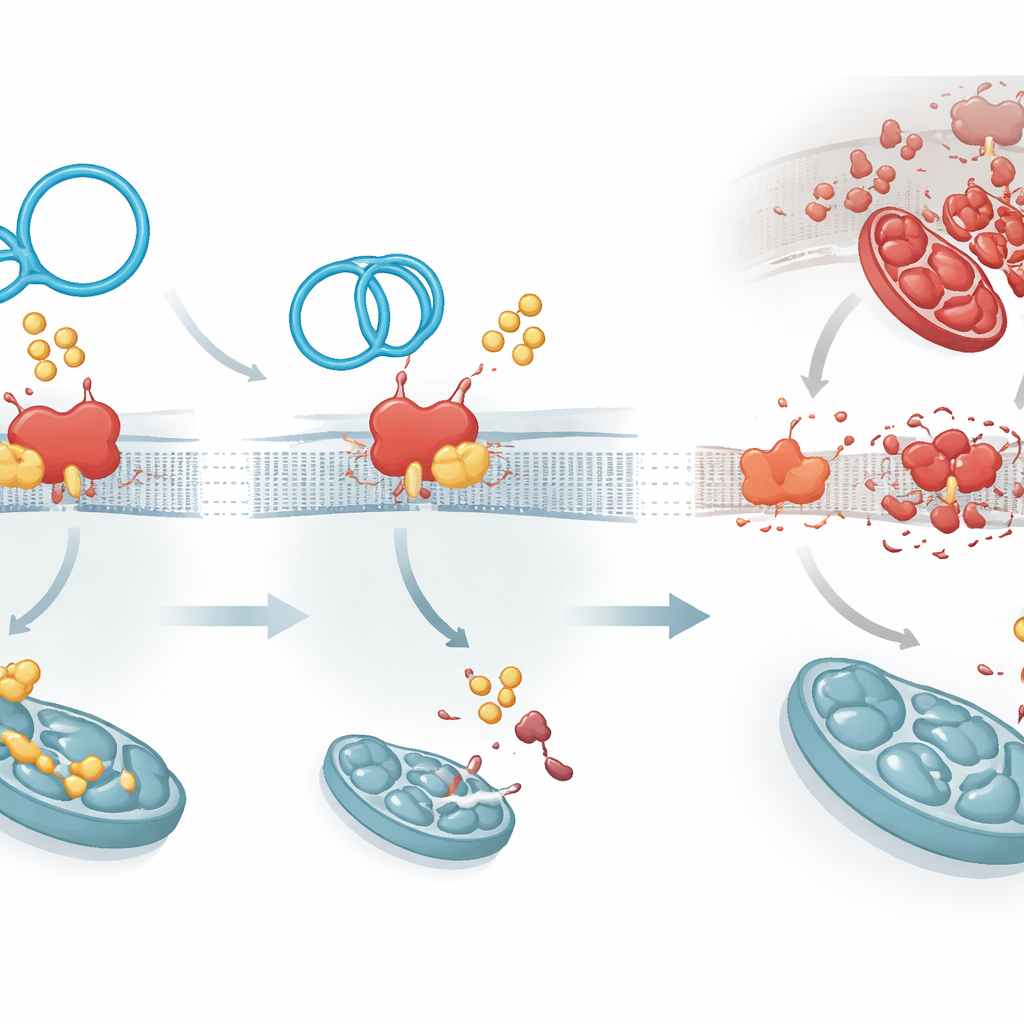
对环状RNA的精细调控及其对患者的意义
该研究还揭示了circArhgap26在损伤期间为何被下调。RNA上的一种常见化学标记m6A在受压心脏的该环状RNA上积累。一个名为YTHDF2的识读蛋白识别这一标记并促进circArhgap26的降解,这在心脏最需要防御时削弱了其天然保护作用。重要的是,人类对应的环状RNA与小鼠高度相似,并且在接受血管开通手术的患者血液中明显低于健康志愿者。综上,这些发现表明恢复或模拟circArhgap26既可作为基于血液的风险标志物,也可能成为一种新型疗法。通俗地说,这项工作揭示了一种小而闭合的分子,它通过解除心肌细胞内致命连锁反应,从而作为抵御再灌注损伤的“守护者”。
引用: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
关键词: 缺血再灌注损伤, 环状RNA, 心肌梗死, 心肌细胞凋亡, 基于RNA的治疗