Clear Sky Science · zh
化学‑光热协同通过铁死亡点燃抗肿瘤免疫
把体内的热与光转化为对抗癌症的武器
化疗药物可以使肿瘤缩小,但常伴随严重副作用,且并不总能阻止癌症复发。本研究探索了一种新方法,通过将已有药物多西他赛封装进对热敏感的小颗粒并用近红外光激活,使其更高效、更智能地发挥作用。目标不仅是更精确地杀死肿瘤细胞,还要唤醒免疫系统,使其识别并在全身范围内追踪消灭癌细胞,防止未来复发。 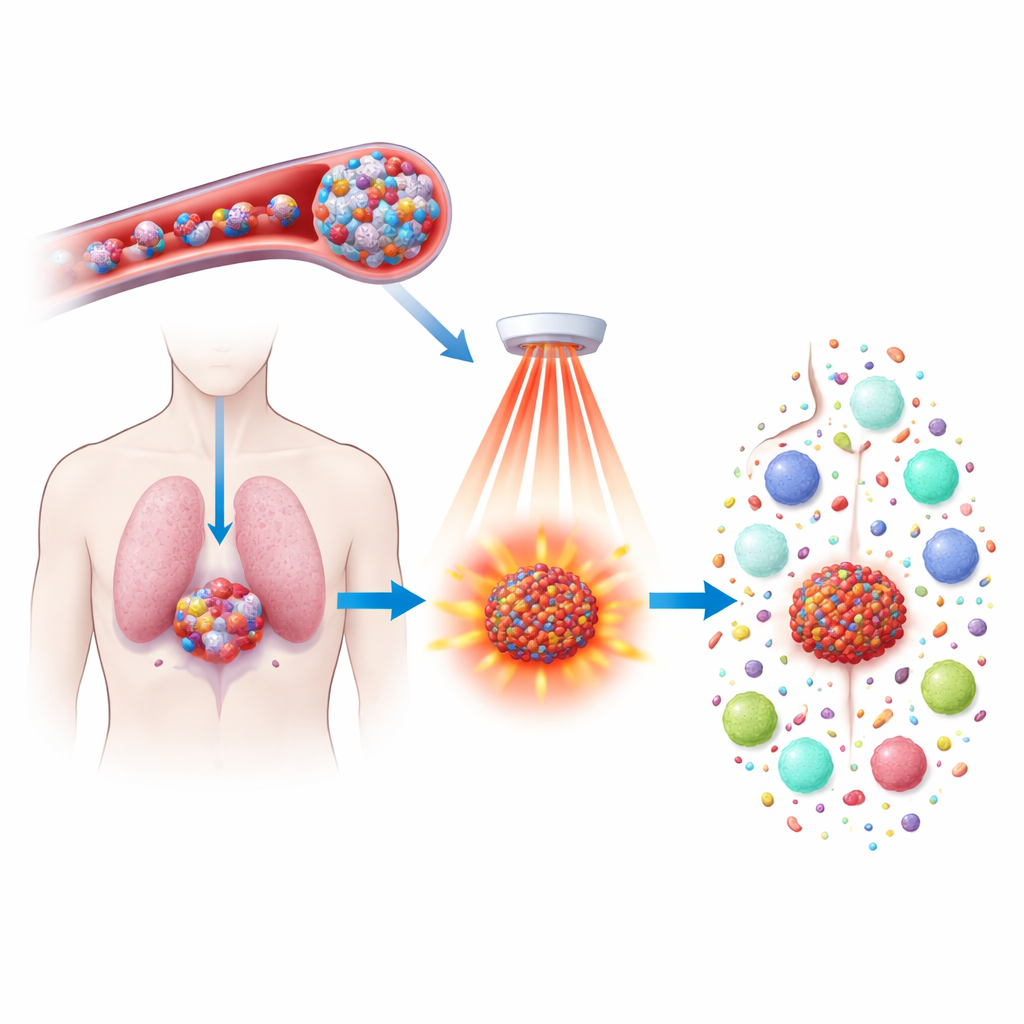
知道去向的小小快递员
研究者构建了一种新型纳米颗粒,基于含有茚基铁(ferrocene)的聚合物——这是一种含铁分子,会与过氧化氢发生强烈反应。肿瘤组织中比正常组织含有更高水平的过氧化氢。这些聚合物自组装成亲水的球形结构,能同时携带多西他赛和一种名为IR808的吸光染料。注入血液后,颗粒足够小且稳定以循环球状循环并渗漏进入肿瘤;在肿瘤中,通透性高的血管和高水平的过氧化氢开始削弱颗粒,并缓慢释放其负载。该设计将治疗集中于肿瘤,同时限制对健康器官的损伤。
用光使局部损伤倍增
随后用可安全穿透组织的近红外光照射肿瘤区域。纳米颗粒内的IR808吸收光能并将其转化为热,同时产生化学活性的氧物种。肿瘤产生的过氧化氢与光驱动的氧化剂共同作用,使颗粒更快崩解并在所需部位释放药物。同时,茚基铁部分的铁有助于将这些氧化剂转化为更具攻击性的形式,专门攻击细胞膜的脂质成分。这种靶向的化学与热学联合作用,比单纯使用多西他赛或仅光照治疗显著增强了杀伤效果。 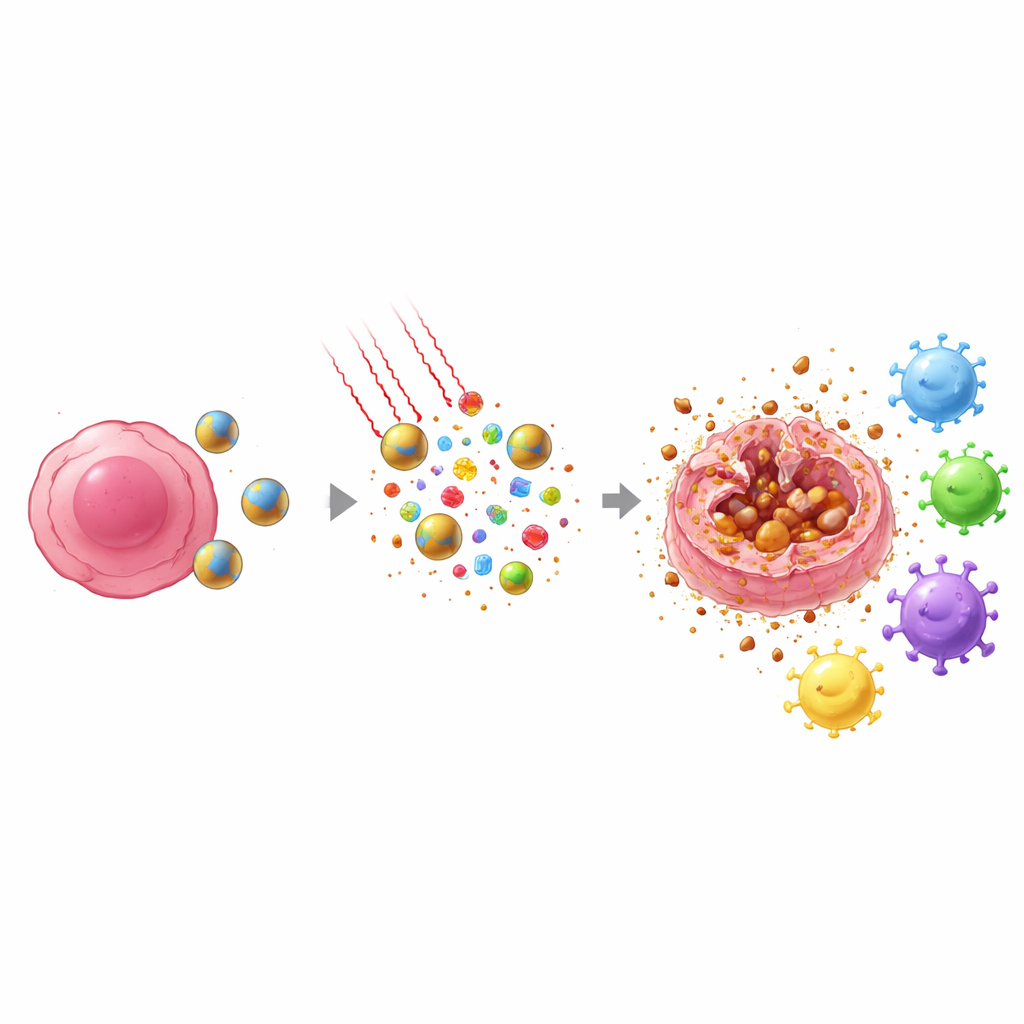
受控的“燃烧”向免疫系统发出信号
重要的是,这种治疗下肿瘤细胞的死亡方式不同于常规化疗。许多细胞并非安静地分解成整齐的碎片,而是经历称为铁死亡的过程——一种铁依赖、损伤脂质的细胞死亡形式,常伴随细胞外膜破裂。当发生这种情况时,细胞会将内部的警报信号和肿瘤特异性片段泄漏到周围环境。同时,多西他赛促使一种关键的核蛋白HMGB1向细胞边缘移动,准备被释放。热、氧化剂和药物作用共同产生了一阵危险信号和抗原信号,附近的免疫哨兵——树突状细胞能够检测到这些信号并将信息带到淋巴结。
从局部攻击到全身防御
在小鼠肿瘤模型中,这种化学‑光热联合治疗不仅比任何单一成分更有效地缩小了直接加热的肿瘤,还改变了免疫微环境。肿瘤中以及引流淋巴结中出现了更多成熟的树突状细胞和数量增加的杀伤性T细胞。在一些免疫功能正常的小鼠中,经两次治疗周期后原发肿瘤消失。当研究者随后在远端或对侧皮下再次植入新肿瘤时,这些继发性生长被延缓或抑制,表明动物形成了一种肿瘤特异性的免疫记忆。加入阻断免疫检查点、防止T细胞衰竭的抗体可进一步减少肺转移并延长存活时间,提示这种局部治疗可以与现代免疫疗法联合使用。
这对未来癌症护理的重要意义
对非专业读者而言,关键要点是这种方法将多西他赛从一种粗放的全身毒物转变为智能、多步骤的抗癌策略的一部分。通过将药物封装在对光触发、含铁的纳米颗粒中,并利用肿瘤自身的化学环境响应,疗法在肿瘤内部造成更多损伤同时尽量保护健康组织。它诱导的特殊细胞死亡模式像是一种来自肿瘤内部的疫苗,教会免疫系统识别并记住癌细胞。如果这些发现能转化到人类临床,这类化学‑光热系统可能帮助将耐药的“冷”肿瘤转变为对免疫疗法更敏感的“热”肿瘤,从而降低复发率并改善长期控制效果。
引用: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
关键词: 癌症纳米药物, 光热疗法, 铁死亡, 癌症免疫治疗, 多西他赛递送