Clear Sky Science · zh
导电配位纳米酶前药在原位精准触发焦亡、铜死亡和铁死亡以实现癌症疫苗化
将肿瘤变成自身的疫苗
传统癌症治疗通常直接旨在杀死肿瘤细胞,但如果能把肿瘤本身变成针对它的疫苗呢?这项研究描述了一种智能纳米颗粒“前药”,它在体内安全运输,仅在肿瘤内被激活,从而迫使癌细胞以一种强烈激发免疫系统的方式死亡。结果不仅是缩小原发肿瘤,还能训练机体识别并消灭远处的肿瘤和转移灶。
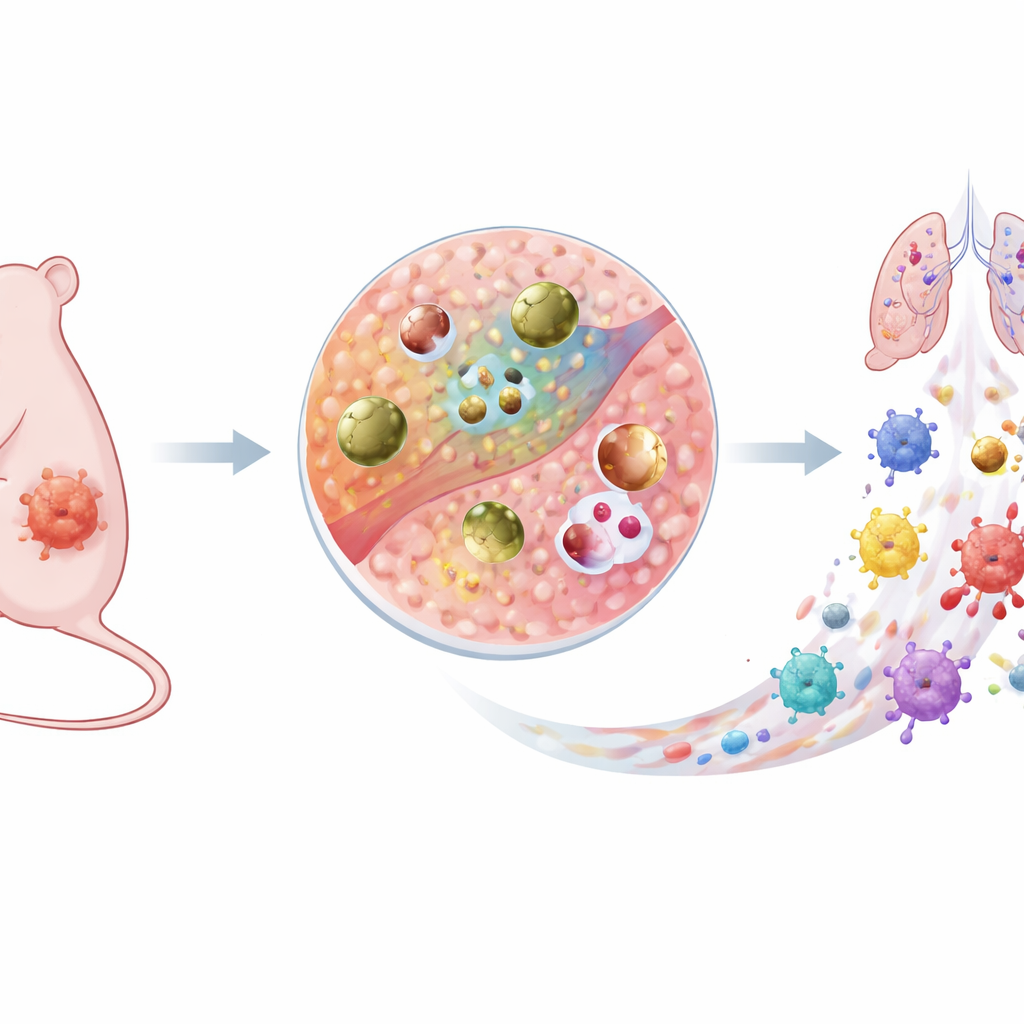
一种新型智能抗癌武器
研究者构建了一种基于铜的微小颗粒,称为Cu–DHN,在循环过程中表现为休眠状态的药物,而到达肿瘤后则成为强效的抗癌因子。它由铜离子、无害的前体分子(1,5-二羟基萘,DHN)和氨基酸半胱氨酸组装而成。三者共同形成了一个导电配位网络,意味着电子可以在颗粒内自由移动。这条内部“电子高速公路”使整个纳米颗粒而不仅是其表面都能参与化学反应。关键在于,Cu–DHN被设计成只响应肿瘤微环境中异常的化学特征——谷胱甘肽和过氧化氢同时异常升高的情况。
肿瘤化学如何打开开关
在肿瘤内部,Cu–DHN表现得像一种人工酶。在谷胱甘肽和过氧化氢共同存在时,它首先利用谷胱甘肽将铜离子重置为高度反应性的状态,然后利用过氧化氢持续产生具有强氧化性的自由基(羟基自由基)。这些氧化物发挥双重作用:损伤细胞成分并将被封存在颗粒内的无害DHN转化为强效抗癌化合物胡桃醌。胡桃醌反过来抑制肿瘤自身的抗氧化防御并进一步提高过氧化氢水平,形成一个自我放大的氧化应激循环,并且该循环被限制在肿瘤内,因为只有肿瘤提供启动该循环所需的特定化学输入。
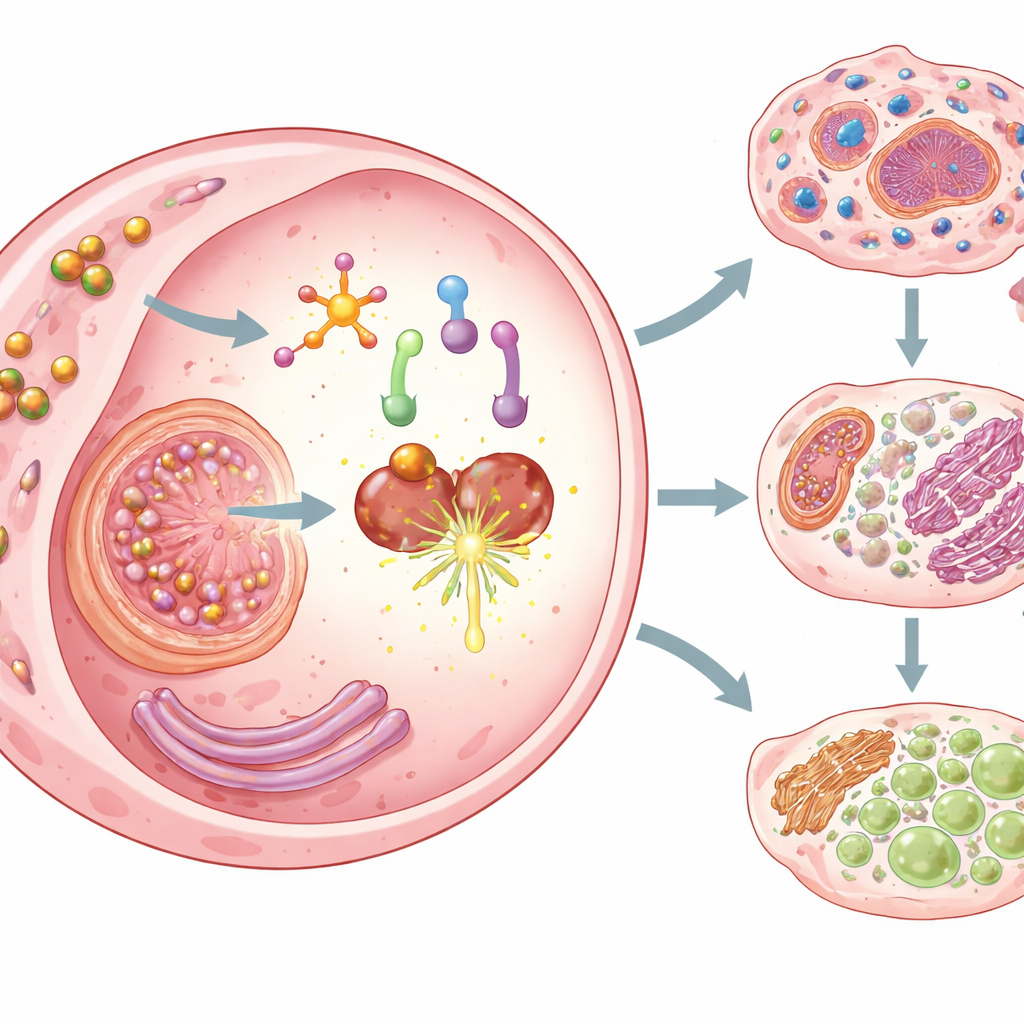
触发三种形式的癌细胞死亡
一旦被激活,Cu–DHN的作用不仅仅是毒杀癌细胞。它触发了三种受调控的细胞死亡形式,这些死亡方式对免疫系统尤其可见。首先,胡桃醌逆转了一种形成孔洞蛋白(gasdermin D)的表观遗传沉默并激活炎症感应复合体,使细胞经历焦亡——一种戏剧性、呈水泡状的死亡,导致细胞膜破裂并泄露内部成分。其次,纳米颗粒携带的铜被癌细胞高效摄取,驱动铜死亡(cuproptosis),这是一种与关键代谢装置中铜毒性积累相关的死亡方式。第三,通过耗竭谷胱甘肽并抑制保护性酶GPX4,Cu–DHN促进了铁死亡(ferroptosis),一种由脂质过氧化驱动的死亡。三种模式协同作用,确保癌细胞不仅被高效杀灭,而且以特别具有免疫原性的方式死亡。
从局部攻击到全身防御
焦亡及伴随的氧化损伤促使肿瘤细胞释放大量警报信号:肿瘤相关抗原、诸如ATP和HMGB1的危险分子,以及表面的应激标志。在侵袭性乳腺癌小鼠模型中,将Cu–DHN单次注入原发肿瘤可在邻近淋巴结中强烈激活树突状细胞,并引发肿瘤特异性CD8 T细胞的激增。这些免疫细胞随后迁移到身体另一侧未治疗的肿瘤和肺部,在那里减缓或几乎阻止了新肿瘤和转移结节的生长。阻断CD8 T细胞会大幅消除这种保护作用,证实Cu–DHN将原发肿瘤转化为一种原位疫苗,教会免疫系统识别并消灭其他部位的癌细胞。
有效且具有更安全的特性
基于焦亡的疗法一个重要的担忧是可能损伤正常组织,因为正常组织也携带相同的成孔蛋白。当胡桃醌以其活性形式直接给药时,小鼠会出现明显的肝、肾和血液毒性。相比之下,Cu–DHN在健康组织中保持惰性,因为它们缺乏激活颗粒所需的化学触发组合。在小鼠中,Cu–DHN在避免器官损伤、血液异常和体重下降的同时,呈现出与活性胡桃醌相当的肿瘤杀灭和抗转移能力。简言之,这项工作展示了一种智能的、具有电导性的纳米颗粒如何在体内保持静默,仅在肿瘤内唤醒,使癌细胞以能刺激免疫的方式死亡,从而作为一种精确、自包含的癌症疫苗平台发挥作用。
引用: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
关键词: 癌症免疫疗法, 纳米医学, 焦亡, 癌症疫苗, 肿瘤微环境