Clear Sky Science · zh
泛素介导的KDM5B稳定性通过抑制双特异性磷酸酶4驱动卵巢癌化疗耐药性
为何部分卵巢癌对化疗失去反应
很多卵巢癌患者起初对顺铂等铂类药物反应良好,但随后往往面临肿瘤复发且不再对治疗产生反应的沉重打击。本研究揭示了癌细胞内部的一条隐秘分子回路,帮助它们获得药物耐受性。通过阐明某一特定“表观遗传开关”如何被打开和关闭,研究者指出了新的方法来预测哪些肿瘤会耐药,以及如何使其重新对现有药物敏感。
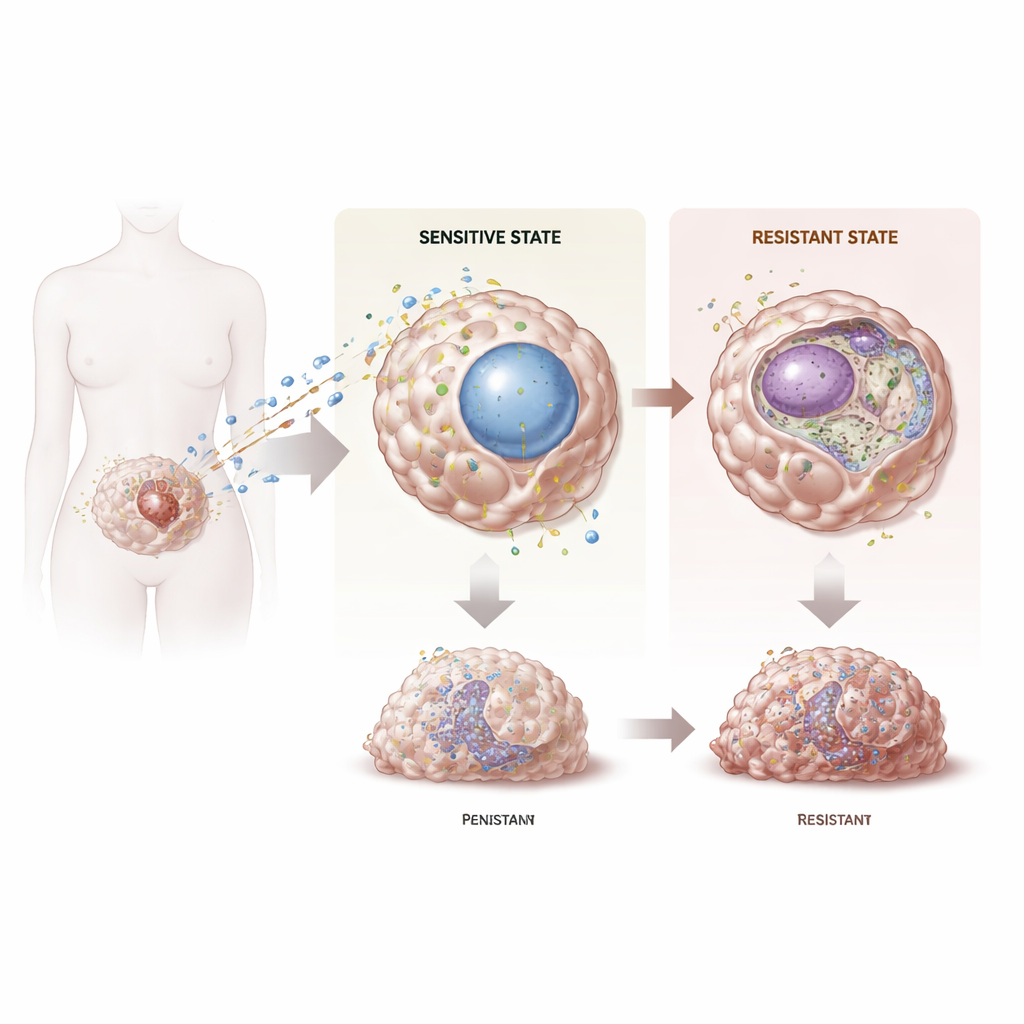
致命癌症的顽固卷土重来
卵巢癌是妇科恶性肿瘤中致死率较高的一种,部分原因在于常常发现较晚且易发生化疗耐药。尽管多达80%的患者最初从铂类化疗中获益,但大多数患者会复发且肿瘤不再敏感,剩余的治疗选择有限、预后不良。近期研究表明,DNA的包装和读取方式的变化——即表观遗传改变——可以帮助癌细胞适应治疗。作者聚焦于一类称为KDM5的酶,这些酶通过去除组蛋白上的化学标记来微调基因活性。他们探讨了该家族中是否有特定成员是卵巢癌铂耐药的关键。
一种酶将平衡推向耐药
通过挖掘大型癌症基因组数据库并测试多种卵巢癌细胞系,研究团队发现KDM5家族中的一员KDM5B在耐药肿瘤中尤为突出。复发性卵巢癌、转移灶和对顺铂不再敏感的细胞系中其表达更高,而其近缘成员KDM5A并未呈现相同模式。当研究者有选择性地去除耐药细胞中的KDM5B时,这些细胞再次对顺铂变得易感并表现出更多的程序性细胞死亡。向原本敏感的细胞中额外加入KDM5B则产生相反效果,使其更难被化疗杀死。这些结果在多个独立细胞模型和携带人源卵巢肿瘤的小鼠体内均得到验证,明确表明KDM5B是化疗耐药的驱动因子。
被沉默的生长信号刹车
深入研究时,作者探讨了KDM5B抑制了哪些基因以帮助肿瘤细胞存活。利用RNA测序和染色质定位,他们发现KDM5B直接抑制了DUSP4基因,后者正常情况下作为对主要生长和应激反应通路MAPK的刹车。KDM5B结合于DUSP4启动子并清除“开启”标记,降低DUSP4水平,从而实际上解除了对MAPK信号的抑制。DUSP4水平低时,MAPK活性上升,促进细胞生长并帮助细胞抵抗顺铂引起的DNA损伤。恢复DUSP4可逆转这种耐药,而删除DUSP4则抵消去除KDM5B的益处,这在细胞培养和小鼠肿瘤中均成立。来自患者的数据也与此一致:高KDM5B且低DUSP4的肿瘤与更差的生存相关。
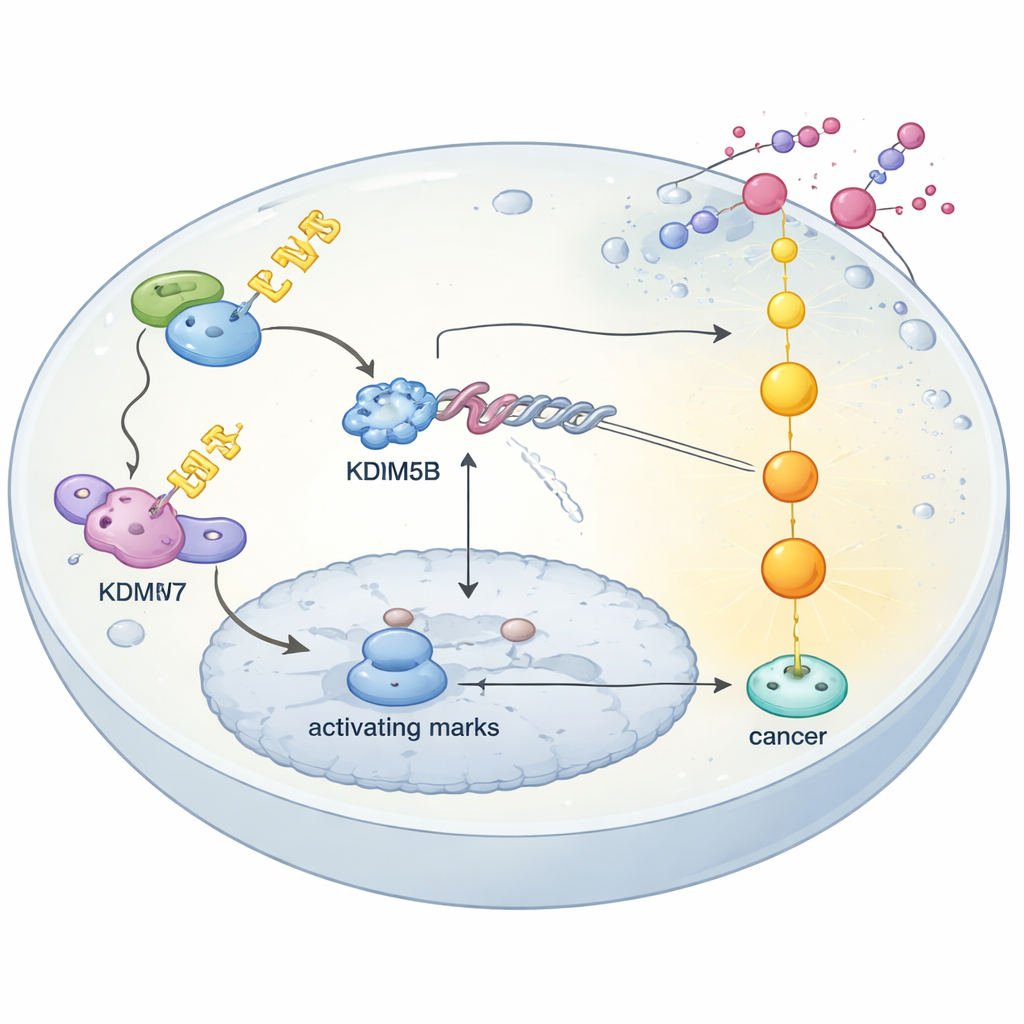
蛋白质质量控制塑造药物反应
该研究还揭示了癌细胞如何首先稳定KDM5B。在细胞内,许多蛋白质被基于泛素链的质量控制系统持续标记以便降解或被保护不被降解。研究者表明,一种称为USP7的酶通过去除这些标记来保护KDM5B,防止其被降解。当通过基因手段或小分子抑制剂阻断USP7时,KDM5B水平下降,耐药的卵巢癌细胞再次对顺铂敏感。相反,一个以FBXW7为核心的E3连接酶复合体仅在另一种酶HIPK1在特定位点磷酸化KDM5B后识别它并标记其被降解。破坏FBXW7–HIPK1通路会使KDM5B更稳定。总体而言,当USP7的保护作用超过FBXW7的清除作用时,KDM5B得以积累并持续抑制DUSP4,从而导致耐药。
对付顽固肿瘤的新策略
通过描绘USP7–KDM5B–DUSP4–MAPK轴,作者提供了一个连贯的解释,说明卵巢癌细胞如何进化出对顺铂的耐受性。对于非专业读者,关键信息是问题不仅仅源于更多突变,还包括基因控制和蛋白周转的重编程。该工作提出了几种可检验的策略:以KDM5B、USP7和DUSP4水平作为生物标志物来预测谁对铂类治疗反应较差;以及将顺铂与抑制KDM5B或USP7的药物联合使用,或与促进KDM5B降解的疗法合用,以恢复药物敏感性。尽管这些方法仍需临床验证,但它们为将部分耐药卵巢癌重新变为可治疗状态提供了可期的蓝图。
引用: Yoo, J., Kim, G.W., Jeon, Y.H. et al. Ubiquitin-mediated stabilization of KDM5B drives chemoresistance via repression of dual-specificity phosphatase 4 in ovarian cancer. Sig Transduct Target Ther 11, 89 (2026). https://doi.org/10.1038/s41392-026-02601-y
关键词: 卵巢癌, 顺铂耐药, 表观遗传调控, KDM5B, MAPK 信号通路