Clear Sky Science · zh
通过激活 AP-1 信号通路,消除 DUSP6 恢复因肿瘤 CD58 丢失而受损的 CAR T 细胞功能
为何增强抗癌细胞的能力至关重要
被工程化的免疫细胞——CAR T 细胞,已改变了某些血液癌症的治疗格局,但许多患者仍会复发,因为肿瘤学会了躲避攻击。这项研究揭示了一类肿瘤的隐蔽弱点:它们悄悄地在细胞内部使 CAR T 细胞失去功能——并展示了通过精准的基因改造如何恢复这些细胞的耐力、能量供给和杀伤力。对读者而言,这提供了一个窗口,展示下一代细胞疗法如何可能变得更持久、更有效,造福更多人群。
肿瘤细胞缺失的“把手”
CAR T 细胞需要与目标细胞建立稳固的“握手”才能有效工作。许多肿瘤细胞表面展示一种称为 CD58 的分子,充当免疫细胞的“把手”,帮助它们附着并形成紧密的接触区。早期研究表明,当癌细胞失去 CD58 时,CAR T 细胞难以形成这种接触,因而效果下降。本研究的研究者提出了更深层的问题:除了这一机械性握手问题外,CD58 的丧失如何改写 CAR T 细胞的内部生物学,随着时间推移削弱其功能?
CAR T 细胞内部的电路短路
通过比较暴露于正常肿瘤与面对缺失 CD58 的肿瘤的 CAR T 细胞,团队发现一个关键的控制枢纽——称为 AP-1——在 T 细胞内被选择性削弱,而其他主要信号通路大体保持完整。AP-1 是一组激活与存活相关基因的蛋白质。当 AP-1 活性下降时,CAR T 细胞显示出典型的内部能量危机迹象:线粒体数量和体积减少(线粒体是细胞的动力工厂)、耗氧能力与糖代谢下降,以及线粒体膜电位丧失。与此同时,有害的活性氧分子积累。综上,这些改变推动 CAR T 细胞走向一种基于自身线粒体损伤的自毁程序,即便没有外部死亡信号。
关闭一个内部刹车
为了解释为何 AP-1 被抑制,研究者向上游寻找可能过度活跃的分子“刹车”。他们发现,面对 CD58 阴性肿瘤的 CAR T 细胞提高了若干磷酸酶的表达——这类酶会关闭信号通路——其中尤以一种称为 DUSP6 的磷酸酶最为显著。通过药物处理与精确的基因编辑阻断这些酶后,他们发现敲除 DUSP6 最显著地恢复了 AP-1 活性。DUSP6 编辑的 CAR T 细胞增殖更好,形成更多线粒体,更有效地燃烧能量底物,产生更多杀癌分子,并且在反复面对缺失 CD58 的肿瘤细胞时不易进入凋亡。
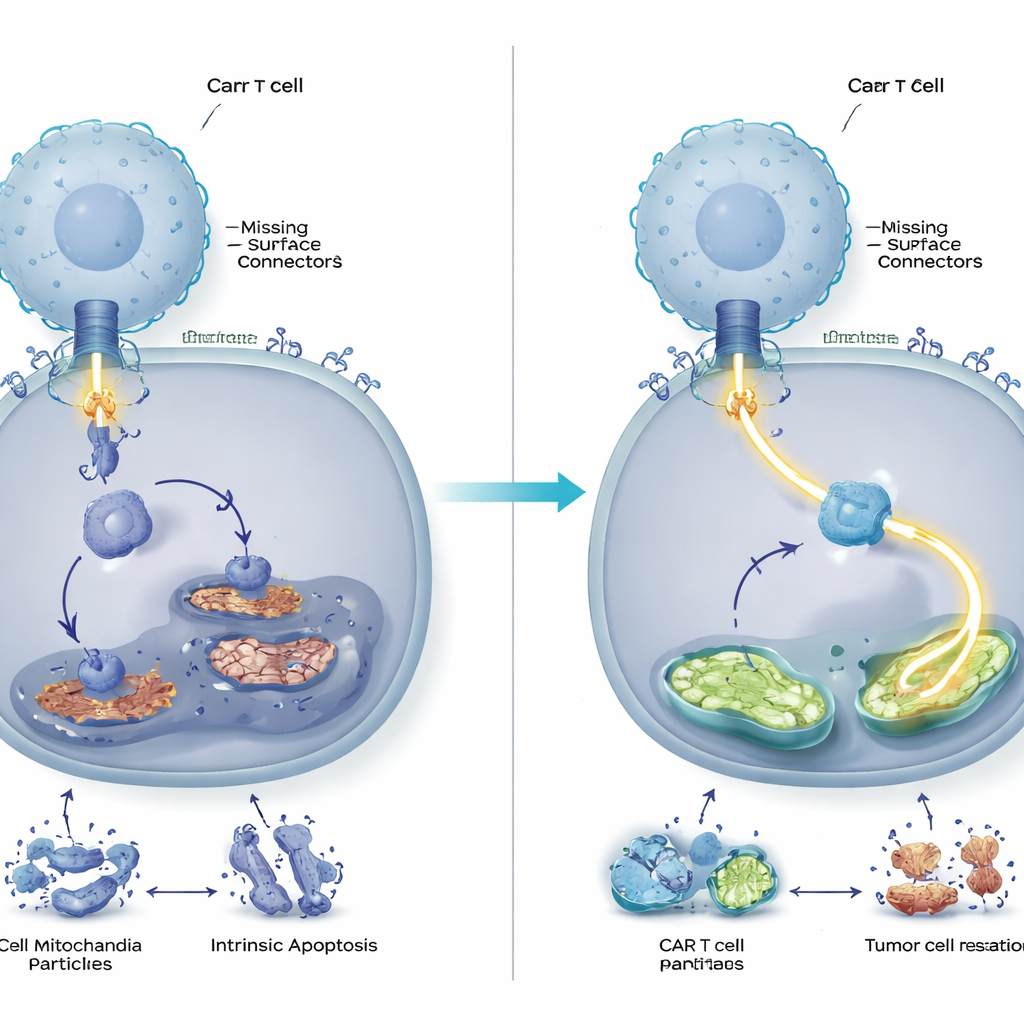
动物实验中更强且更持久的肿瘤控制
团队接着测试这种分子微调在体内是否重要。在携带有人源血液癌细胞(有或无 CD58)的小鼠体内,缺失 DUSP6 的 CAR T 细胞比常规 CAR T 细胞更有效地清除肿瘤并更长时间地控制肿瘤生长。这些工程化细胞增殖更强,表现出更少的衰竭标志,并分泌更高水平的关键免疫信使。值得注意的是,去除 DUSP6 带来的益处不仅在肿瘤缺失 CD58 时可见,在肿瘤保留 CD58 的情况下同样有效,这表明该改造可能广泛地增强 CAR T 细胞疗法,而非仅针对罕见肿瘤亚型的狭义修补。
来自患者数据的线索
为探讨在人类中的相关性,研究者分析了接受 CAR T 细胞或免疫检查点抑制剂治疗患者的基因表达数据。在接受双靶点 CAR T 治疗的弥漫性大 B 细胞淋巴瘤患者中,输注前或输注后不久 CD8 细胞中的 DUSP6 水平较低与更高的完全缓解率相关。在另一组接受抗 PD-1 抗体治疗的皮肤癌队列中,未获应答者的耗竭 CD8 细胞往往比应答者表达更多的 DUSP6。综合这些观察,提示 DUSP6 作为不同免疫疗法中 T 细胞功能的负面标志,降低其表达可能改善疗效。
这对未来癌症疗法意味着什么
对普通读者而言,结论是:一些肿瘤逃避 CAR T 细胞攻击不仅通过躲避识别,还通过破坏细胞内部的“引擎”来完成。肿瘤细胞丧失 CD58 这一“把手”,会悄然降低 CAR T 细胞的 AP-1 信号,耗尽其线粒体、增加有毒副产物并促使其提前死亡。通过去除 DUSP6 这一刹车,研究者能够恢复丢失的信号,修复线粒体健康,使 CAR T 细胞获得更强的耐力和杀伤力,即便面对耐药肿瘤。尽管还需进行更多的安全性和临床检验,消除 DUSP6 显示出作为一种有前景的工程策略,能使“活体癌症药物”更强、更持久,并可能惠及更广泛的患者群体。
引用: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
关键词: CAR T 细胞, CD58, DUSP6, 癌症免疫治疗, T 细胞代谢