Clear Sky Science · zh
通过诱导多能干细胞衍生多器官类器官平台实现基于药代-药效学指导的个性化治疗:针对 NF1 突变乳腺癌
为什么这项研究对病人很重要
许多癌症患者接受的药物在某些人身上效果很好,但在其他人身上无效,并且常伴随严重副作用。本研究描述了一种使用来自患者自身细胞培养的迷你器官在体外测试癌症治疗的新方法。工作聚焦于一种由 NF1 基因改变驱动的难治性乳腺癌,展示了将基因修复策略与靶向药物相结合,如何可能带来更安全、更有效且真正个性化的治疗。
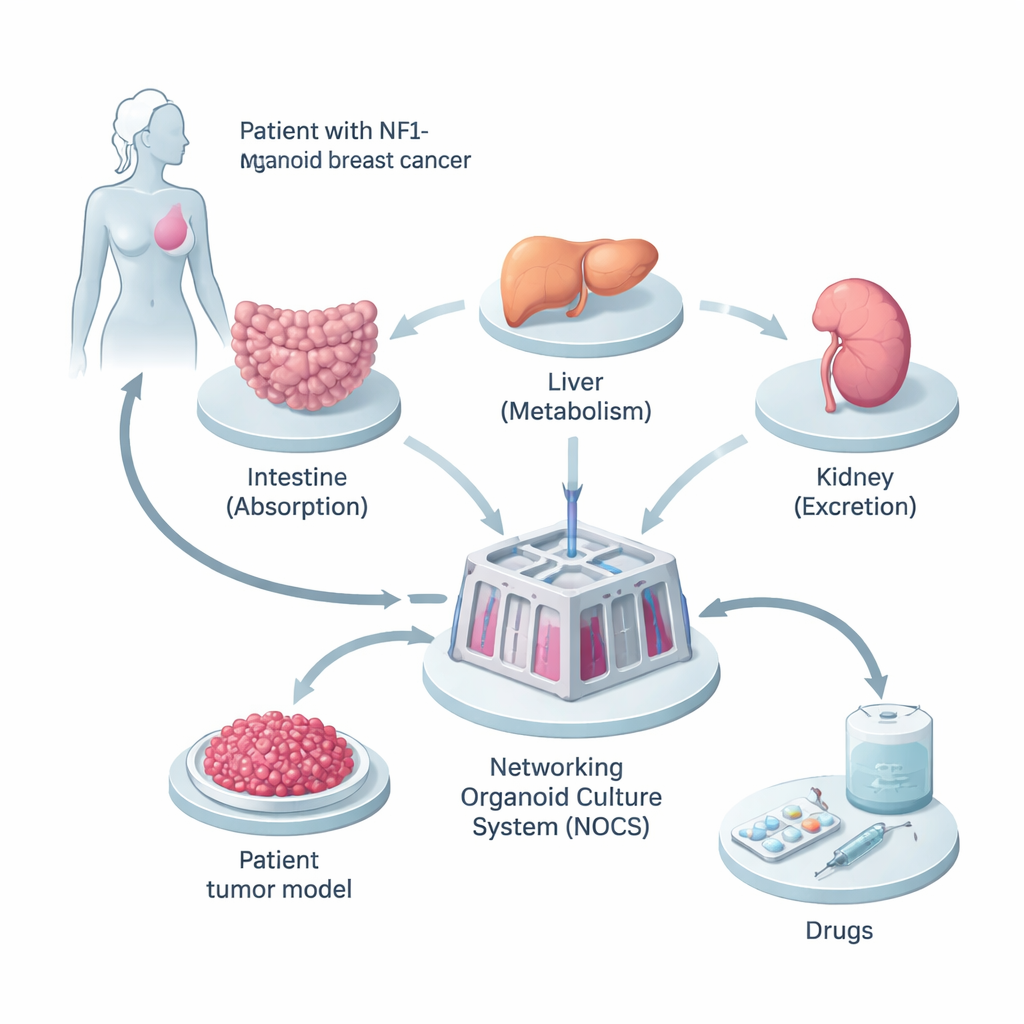
构建患者身体的微型版本
研究人员从一名携带遗传性 NF1 突变的乳腺癌女性取材。他们将其正常的皮肤样细胞重编程为诱导多能干细胞,这类细胞几乎可以分化为任何体内细胞类型。基于这些细胞,他们培养了三类微型器官—小肠、肝脏和肾脏—因为这些是药物被吸收、代谢和清除的关键部位。同时,他们还用患者的癌细胞构建了三维肿瘤“球状体”,保留了原始肿瘤中的细胞成分组合和遗传改变。
一个活体的药物测试回路
为了让这些微型器官更像真实身体,团队将它们连接到一个充液装置中,称为网络类器官培养系统(Networking Organoid Culture System,NOCS)。在这个装置里,培养基在小肠、肝脏、肾脏和肿瘤舱室之间流动,模拟血液循环。药物可以以类似口服或注射的方式加入,传感器和泵控制“血液”的流速和更新频率。这使科学家能够追踪药物被吸收的程度、被分解的速度以及对肿瘤的作用强度——所有这些都在以患者为特异性的人源模型中完成。
用外显子跳跃修复破损基因
患者的肿瘤携带一个破坏性的 NF1 突变,该突变使生长信号通路持续激活,并令许多常规药物失效。团队设计了短片段的遗传物质,称为反义寡核苷酸,以诱导细胞的 RNA 处理机制跳过 NF1 基因中的有缺陷片段(外显子 2)。通过一种能持续多日起效的病毒递送系统,他们在患者的癌细胞中诱导出稳定的“外显子跳跃”。这产生了较短但功能性的 NF1 蛋白,降低了过度活跃的生长信号,并使肿瘤细胞对治疗更为敏感。
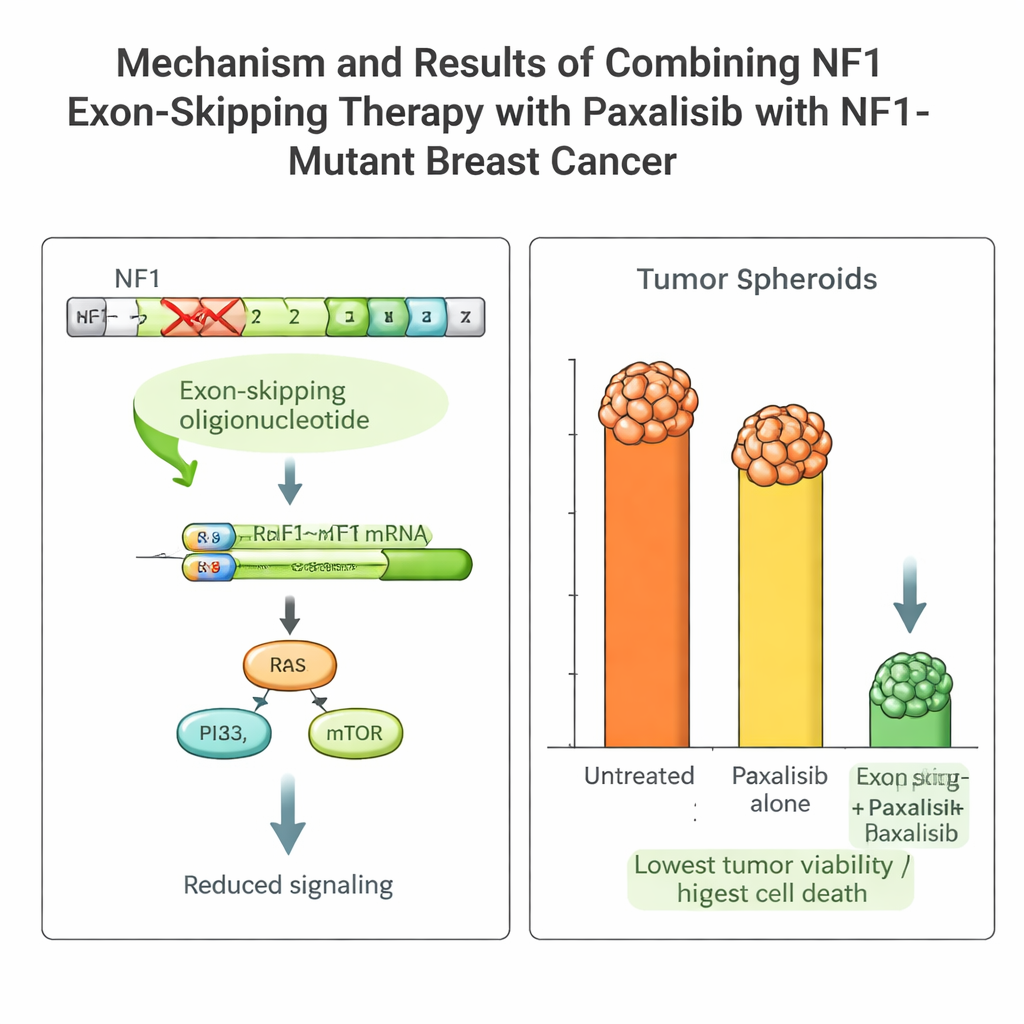
借助药代/药效学指导选择合适的靶向药物
有了这个平台,团队比较了数种阻断 PI3K–mTOR 通路的先进药物,该通路位于 NF1 的下游。他们在小鼠和 NOCS 中测量了药代动力学(身体如何处理药物)和药效学(药物如何作用于肿瘤)。其中一种药物 Paxalisib 脱颖而出:它在小肠中吸收良好,在系统中保持有用浓度,并在动物体内与类器官装置中表现出相似的行为。当与 NF1 外显子跳跃联合使用时,Paxalisib 对患者肿瘤细胞的杀伤力显著增强,肿瘤生长大幅受抑,并出现明确的程序性细胞死亡迹象,这在 NOCS 与携带患者肿瘤的小鼠中均有体现。
在各器官间权衡益处与风险
由于小肠、肝脏和肾脏模型被纳入同一回路,研究人员还可以监测器官损伤的早期迹象。Paxalisib 在肠和肾模型中引发了应激反应与轻微屏障受损,并在肝脏中显示出应激征象,但在所测剂量下并未导致明显的细胞存活率下降。这种基于人组织的整体视角,提供了一种在药物进入患者体内之前,不仅比较肿瘤缩小效果也评估对健康器官影响的方法。
这对未来癌症护理的可能意义
通俗地说,本研究表明现在可以培养出一个简化的、患者特异性的“芯片上的微型身体”,用于测试不同药物乃至基因修复方法的行为和相互作用。对于这位 NF1 突变乳腺癌患者而言,最佳策略是将 NF1 外显子跳跃疗法与口服药物 Paxalisib 联合使用,两者合用比单独任一疗法更显著地减缓肿瘤生长。如果进一步开发并在更多患者中验证,这类平台可引导医生制定基于每位患者基因与生物学特征的个体化治疗方案,从而提高疗效并减少不必要的毒性。
引用: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
关键词: 个体化肿瘤学, 乳腺癌, 类器官, NF1 突变, 靶向治疗