Clear Sky Science · zh
利用脂质驱动的免疫代谢通路改造卵巢癌大网膜转移以增强患者的免疫治疗
为什么腹部周围的脂肪对卵巢癌很重要
卵巢癌常常转移到腹部的一块脂肪组织,即大网膜。该区域富含脂肪细胞和免疫细胞,远不只是被动的旁观者。本研究的摘要显示,免疫细胞在这些大网膜病灶中如何使用和处理脂质,有助于解释为什么只有少部分患者能从现代免疫疗法中获益。研究还提出了新的药物组合和基于影像的检测方法,可能使更多患者受益。
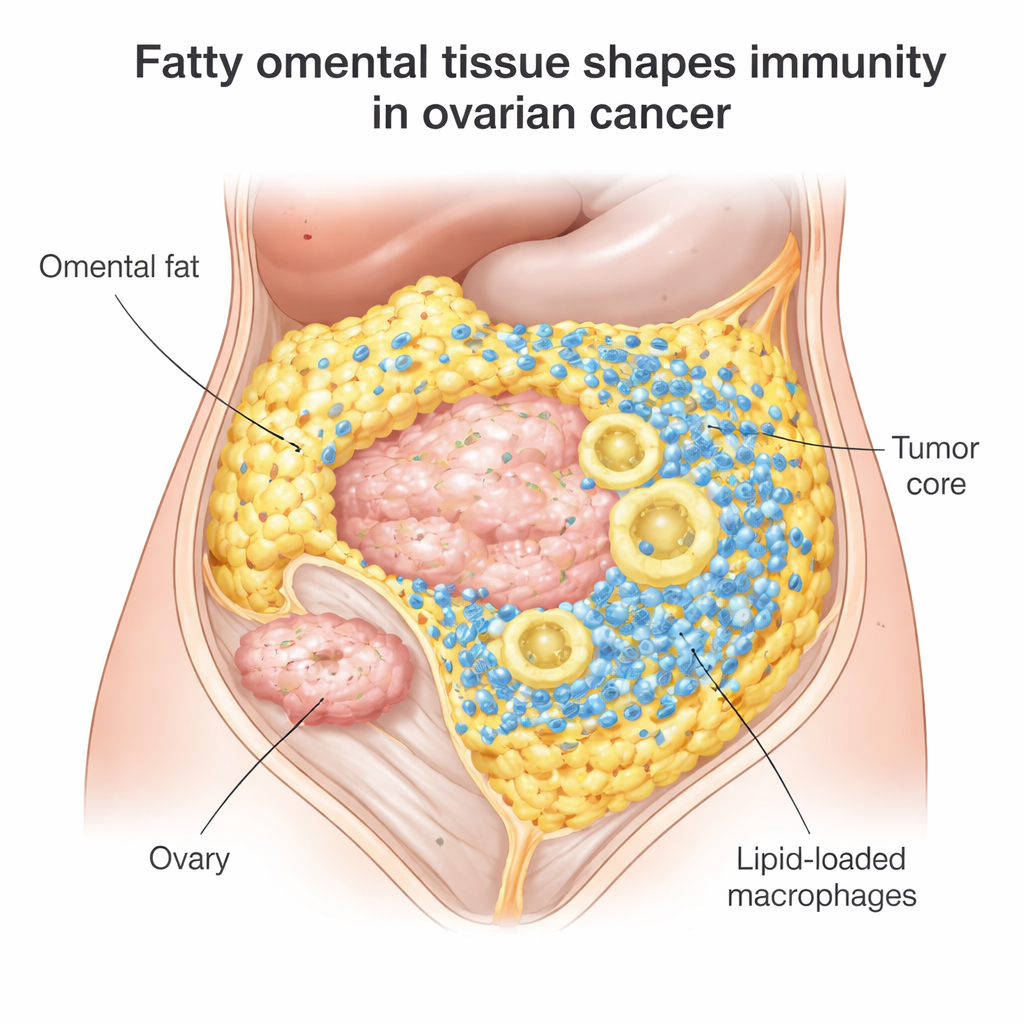
腹部脂肪中的隐秘战场
大多数上皮性卵巢癌女性最初对手术和化疗有反应,但70–80%会复发,像nivolumab或pembrolizumab这样的免疫检查点抑制剂仅帮助大约10–15%。研究者将注意力集中在大网膜转移,这是卵巢癌常见的在脂肪细胞间播散的部位。对100多份肿瘤样本的检查发现,大网膜肿瘤富集大量免疫细胞:能够攻击癌细胞的杀伤性T细胞,以及称为巨噬细胞的大型清道夫细胞。但情况并非全是好消息:这些T细胞倾向于聚集在肿瘤与脂肪的边界,而非渗入肿瘤核心——而肿瘤核心恰恰是最需要它们的地方。
脂肪既滋养某些免疫细胞也压垮另一些
深入研究表明,这些脂肪肿瘤中的T细胞通过从邻近脂肪细胞摄取脂质来适应局部环境。这似乎维持了它们的代谢“健康”:基因表达和体外实验显示它们能够识别并杀伤患者自身的肿瘤细胞。与此同时,大网膜中的许多肿瘤相关巨噬细胞充满了脂滴。这些脂质堆积的巨噬细胞表现出高氧化应激的迹象——与活性氧相关的化学损伤——并向免疫抑制、支持肿瘤的状态转变。换言之,同一脂肪富集的环境既能滋养有效的T细胞,也会将巨噬细胞推向削弱整体免疫攻击的有害模式。
用现有药物重新编程被过度喂养的巨噬细胞
研究人员接着探问,能否将这些受压的巨噬细胞转变为盟友。利用在体外培养的新鲜肿瘤碎片,他们测试了两种方法。一种使用maraviroc,这是一种阻断CCR5(免疫信号CCL5的受体)的艾滋病毒药,该信号在肿瘤–脂肪边界丰富;另一种阻断CD36,这是一种允许巨噬细胞摄取脂肪酸的关键“清道夫”受体。两种处理都减少了巨噬细胞内的脂质负荷,降低了氧化应激和有害脂质过氧化的标志,并释放出一系列炎性信号。关键是,这些处理使杀伤性T细胞增殖并从脂肪边缘迁入肿瘤核心,提升局部免疫活性,而无需外源性免疫细胞加入。
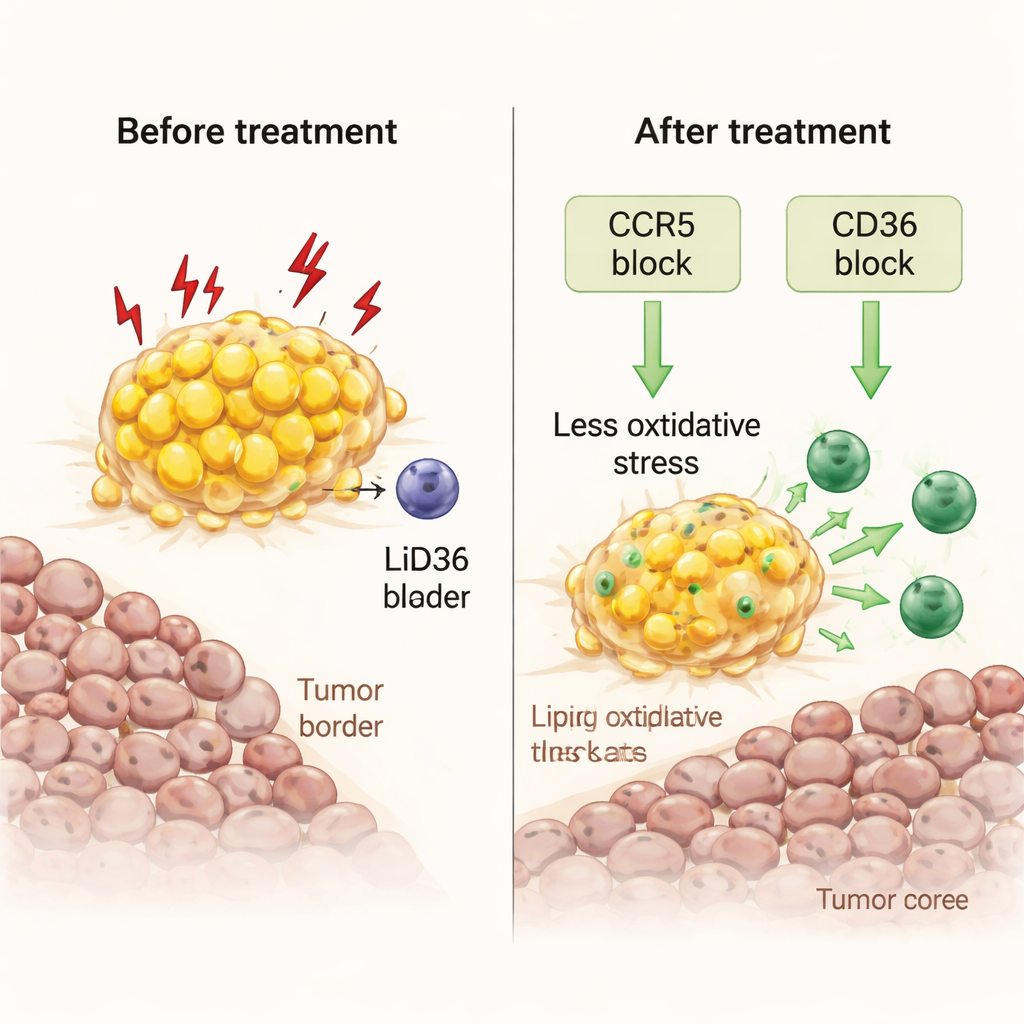
从细胞通路到现实模型与患者
为在更现实的情景中检验这些想法,研究团队使用了带有人类化免疫系统的人源化小鼠,并在富脂组织中植入了人类乳腺癌。maraviroc处理以与患者来源样本相似的方式重新编程了这些动物体内的人类巨噬细胞:脂质和应激特征减少,细胞因子产生增加,并更强烈地支持T细胞相关通路。在临床层面,研究者重新审视了一项针对化疗耐药卵巢癌的日本nivolumab试验。所有从该药物获益的患者,其手术样本中都有可见的大网膜转移。通过将CT或MRI影像与体脂分布的机器学习分析相结合,他们构建了一棵决策树,可以非侵入性地标记出肿瘤可能靠近内脏脂肪的患者——在一例前瞻性病例中,该方法成功预测出随后对nivolumab有反应的患者。
这对未来治疗可能意味着什么
对于非专业读者,结论是:卵巢癌在体内“在哪里”生长,以及邻近脂肪如何重塑免疫细胞,都会强烈影响免疫疗法的效果。富脂的大网膜病灶似乎既含有有活力的T细胞,也含有被过度喂养、应激的巨噬细胞,这些巨噬细胞会抑制免疫攻势。通过减轻这些巨噬细胞的脂质负担并缓解其氧化压力——使用如maraviroc的CCR5阻断剂、针对CD36的药物或相关策略——可能将部分受阻的免疫反应转变为对肿瘤的全面进攻。同时,基于影像的大网膜受累评估可帮助医生选择最有可能从免疫检查点药物中获益的患者,从而为卵巢癌治疗带来更个性化且潜在更有效的路径。
引用: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
关键词: 卵巢癌, 大网膜脂肪, 免疫疗法, 肿瘤相关巨噬细胞, 脂质代谢