Clear Sky Science · zh
GPR54 通过多巴脱羧酶调控非小细胞肺癌的发展
这则肺癌报道为何重要
肺癌仍然是致死率极高的癌症之一,大多数病例属于一种称为非小细胞肺癌(NSCLC)的类型。许多患者最终会用尽有效的治疗选择,因为肿瘤会对现有药物产生适应或耐药。该研究揭示了肺癌细胞内一个此前被低估的调控体系,核心由一种称为 GPR54 的受体和一种名为多巴脱羧酶(DDC)的酶构成。通过弄清这些分子如何帮助肿瘤生长并为自身提供能量,研究人员指出了放慢或缩小 NSCLC 的新途径。
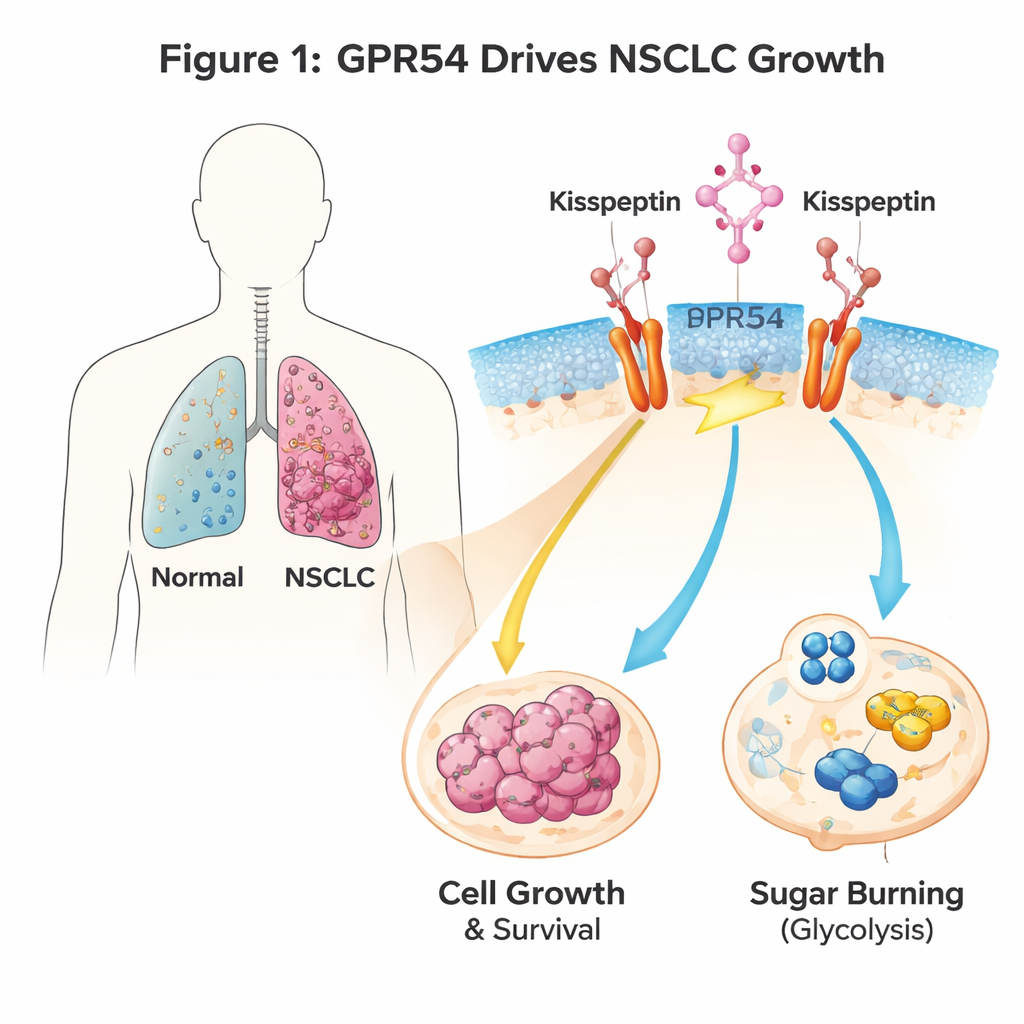
肺癌细胞表面的信号开关
GPR54 是位于细胞表面的传感器,对一种天然信号分子 kisspeptin 做出反应。它最为人所知的是在青春期和生殖方面的作用,但也在多种癌症中出现。作者使用了经过基因改造的小鼠模型:当肺细胞中一个驱癌基因 Kras 被激活时,这些小鼠会发展为 NSCLC。当他们在这些小鼠中删除 Gpr54 基因时,动物寿命延长,肺肿瘤数量和体积减少,且癌细胞出现明显的自我毁灭迹象(凋亡)。人类 NSCLC 细胞系也呈现相同迹象:降低 GPR54 水平后,肿瘤细胞增殖变慢,形成的集落减少,并且更容易死亡,不论其具体基因突变如何。
GPR54 如何维持肿瘤细胞存活
进一步深入研究时,研究人员探查了 GPR54 所依赖的细胞内回路。他们发现 GPR54 将信号传入两个主要的生长通路,分别是 AKT 和 ERK。这两条通路都是常见的“配线枢纽”,可指示癌细胞分裂并抵抗细胞死亡。当阻断或去除 GPR54 时,AKT 和 ERK 的活性下降,细胞更容易发生凋亡。恢复强烈的 AKT 或 ERK 信号可以部分挽救细胞,这证实了 GPR54 通过依赖这些生长回路来帮助 NSCLC 细胞存活。
改变癌细胞利用糖的方式
癌细胞常常重编程其养分利用方式,偏向快速分解糖(糖酵解)以支持生长。缺乏 Gpr54 的小鼠肿瘤的基因表达谱显示,许多参与糖代谢和能量产生的基因被下调。在用 kisspeptin 激活 GPR54 的肺癌细胞中,氧气利用和酸产生的测量——作为能量代谢的替代指标——显示 GPR54 提升了糖酵解。阻断 GPR54 通路的不同环节(如 Gαq/11 开关、PI3K、AKT 或 mTOR)会减少葡萄糖消耗和乳酸产生,并推动细胞走向凋亡。简言之,GPR54 帮助 NSCLC 细胞更快更有效地燃烧糖,为其快速生长提供支持。
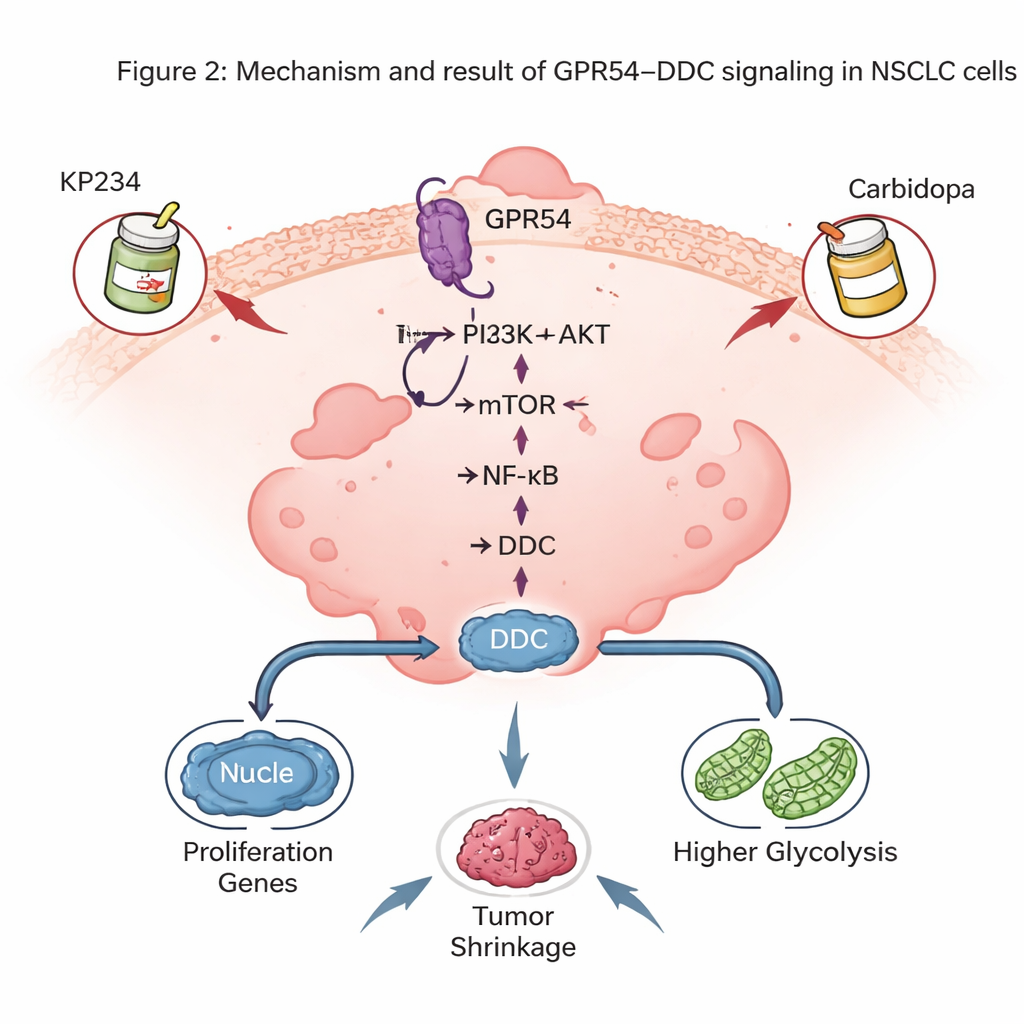
一种与大脑相关的酶的意外角色
其中最引人注目的发现之一是 GPR54 控制着 DDC 的水平;DDC 是一种以合成脑内化学物质多巴胺和血清素而闻名的酶。在小鼠肿瘤中,DDC 水平与 GPR54 的量紧密相关:GPR54 减少时 DDC 也减少。人类 NSCLC 肿瘤和细胞系也显示出比正常肺细胞更高的 DDC 表达,且 DDC 更高的患者预后更差。在小鼠中,下调肺癌细胞的 DDC 会减慢肿瘤生长,在培养皿中减少细胞分裂并触发更多凋亡。在分子水平上,DDC 有助于维持 NF-κB 通路的活性——该通路是促进癌细胞存活和炎症的主控调节器——并且支持肿瘤细胞的高糖酵解状态。
测试一种药物联合策略
由于 DDC 在帕金森病中已可被药物卡比多巴(carbidopa)靶向,作者探讨了将 GPR54 抑制剂(KP234)与卡比多巴联合使用是否能从两方面打击 NSCLC。在细胞培养和将人类 NSCLC 细胞种植入肺中的小鼠模型中,双药治疗比单药更能抑制肿瘤生长并增加癌细胞死亡,且动物体重未见明显下降。这些组合疗法在与针对突变 RAS 基因的一些现代靶向药物联合时也显示出潜力,表明 GPR54–DDC 信号可以叠加到现有的精准疗法之上。
这对未来肺癌治疗意味着什么
对非专业读者而言,关键的信息是:NSCLC 细胞依赖于一个此前被低估的表面开关(GPR54)与代谢酶(DDC)之间的合作关系来维持存活并快速消耗燃料。破坏这一合作关系会削弱肿瘤,使其在实验模型中生长更慢并更容易凋亡。尽管在此类策略进入临床之前仍需大量工作,这项研究将 GPR54 和 DDC 定位为识别侵袭性 NSCLC 的潜在生物标志物,以及作为可能改善当前对抗难治肿瘤患者结局的新型联合治疗靶点。
引用: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
关键词: 非小细胞肺癌, GPR54, 多巴脱羧酶, 癌症代谢, 靶向治疗