Clear Sky Science · zh
癌症中的活性氧(ROS):从机制到治疗意义
当有益分子变得危险
在每个细胞内部,被称为活性氧(ROS)的微小化学火花在正常生命活动中不断产生。在适当的水平上,它们有助于细胞生长、通讯并防御病原体。但这篇综述解释了同样的分子如何也能损伤DNA、扭曲细胞信号通路,并推动癌症生长、转移和耐药。理解ROS的这种“二重性”正帮助科学家设计新的癌症疗法,或是平抑有害的氧化应激,或是有意将其推至极限以杀死肿瘤细胞。
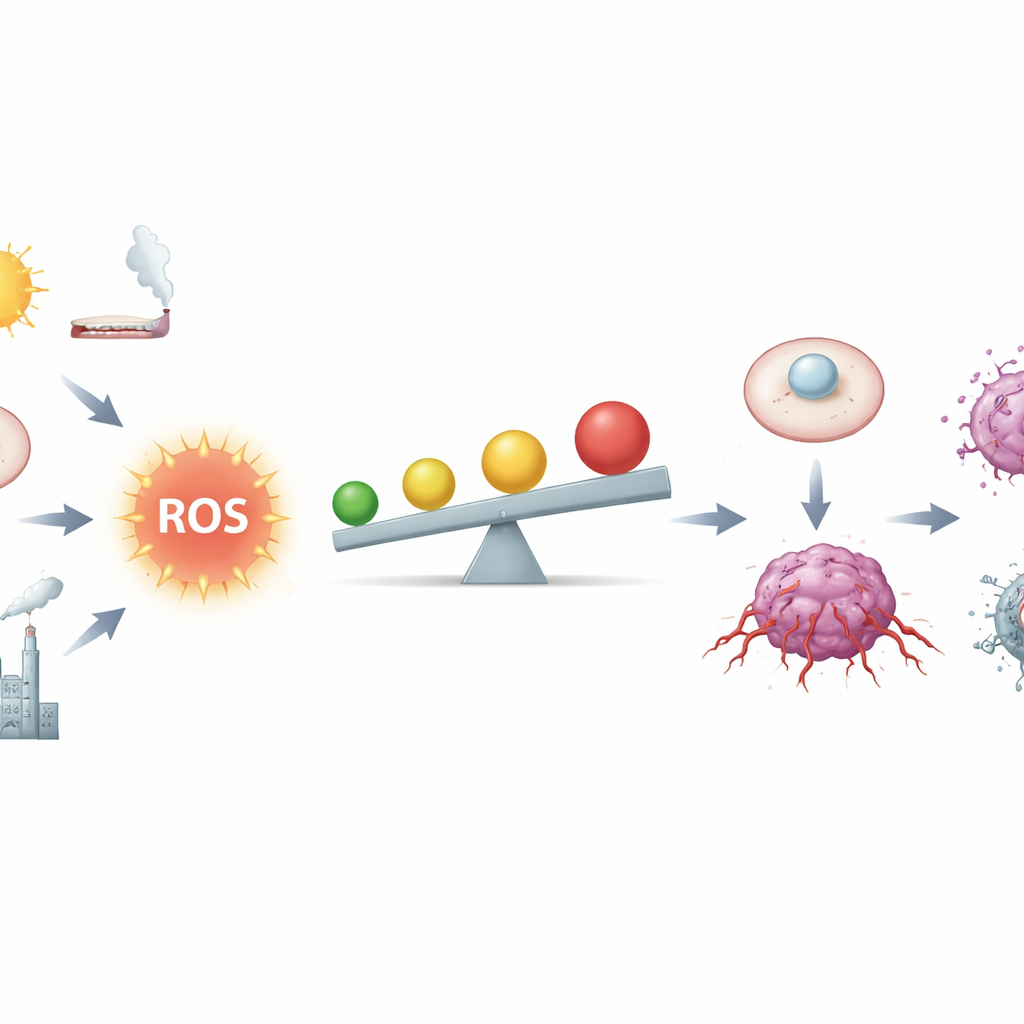
燃料与火焰之间的细微界限
作者将ROS描述为呼吸和代谢的化学副产物,同时也是强有力的信使。在健康组织中,低量的ROS有助于控制细胞周期、修复损伤并微调免疫反应。细胞通过复杂的抗氧化网络来控制这些信号,包括谷胱甘肽等分子以及由名为Nrf2的主开关调控的酶。然而,癌细胞却更接近危险区域:基因缺陷、负荷过重的线粒体、慢性炎症、烟草烟雾、辐射和某些金属都会提高ROS水平。在中等偏高的水平下,ROS可造成DNA切割、染色体不稳定,并长期激活促生长和生存的回路,使正常细胞更易转变为癌细胞。
氧化应激如何塑造肿瘤行为
一旦肿瘤形成,ROS仍继续影响其生物学特性。中度氧化应激能激活许多促进细胞分裂、血管生成、组织侵袭和耐化疗的生长通路。ROS可重编程癌细胞对糖类、脂肪和氨基酸的利用,将燃料引向产生额外抗氧化能力和新细胞构建块的途径。它们还影响细胞命运的决策:根据强度和环境,ROS可使信号偏向生存或触发若干程序性细胞死亡形式,包括经典的凋亡以及较新的形式如铁死亡(ferroptosis)、坏死性凋亡(necroptosis)和铜依赖性细胞死亡(cuproptosis)。这使得ROS既是肿瘤进展的同谋,又可能成为肿瘤自我毁灭的触发点。
改造免疫与药物反应
综述强调,ROS并不只是作用于癌细胞本身——它们也重塑肿瘤的周边环境。高氧化应激可使抗癌的T细胞和自然杀伤细胞耗竭或死亡,同时有利于那些抑制性细胞的活性,这些细胞为肿瘤提供保护。ROS还帮助肿瘤上调“别杀我”信号,如检查点蛋白,从而削弱免疫治疗的效果。与此同时,中等水平的ROS可通过增强药物外排泵和应激反应来驱动耐药,使癌细胞能将化疗药物排出或修复其造成的损伤。然而,在其他情况下,将ROS推过关键阈值可以瓦解这些防御,重新使肿瘤对治疗敏感。
将氧化还原脆弱性转化为治疗策略
由于癌细胞在利用ROS与被ROS毒害之间走钢丝,作者认为ROS平衡是一个可利用的治疗杠杆。一种广泛策略是降低有害的ROS或增强抗氧化能力,主要用于预防或在治疗期间保护健康组织。另一种则在肿瘤中采取相反做法:抑制抗氧化系统或提高ROS产生,直到癌细胞越过致死阈值,尤其是与放疗、靶向药物或免疫治疗联合时。第三种方法是不直接改变ROS水平,但阻断肿瘤依赖的特定ROS敏感开关——信号蛋白、代谢酶或死亡通路。在这些思路中贯穿着个体化的主题:不同癌症具有不同的“氧化还原签名”,因此未来的疗法可能需要通过血液或组织检测氧化损伤、抗氧化能力和与ROS相关的基因,以为每位患者选择合适的靶向氧化还原治疗。
这对患者意味着什么
通俗地说,本文认为ROS既非全然有害亦非全然有益;它们是细胞乃至癌症所利用的强大工具。癌细胞倾向于在比健康细胞更接近氧化应激临界点的状态下运行,这可能创造出一个治疗窗口。然而,由于抗氧化剂和促氧化剂在剂量、时机和肿瘤类型不同的情况下都可能带来益处或危害,盲目使用补充剂或提升ROS的药物存在风险。作者得出的结论是,未来在于精心设计的疗法与诊断,先测定每个肿瘤的氧化还原状态,然后适度调整ROS与抗氧化系统——要么下调以保护正常组织,要么上调以将癌细胞推向其承受极限之外。
引用: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
关键词: 活性氧, 氧化应激, 癌症代谢, 氧化还原疗法, 肿瘤微环境