Clear Sky Science · zh
DNA 与 RNA 分型的一致性分析:MD 安德森 IMPACT2 精准肿瘤学研究
这项研究对癌症患者为何重要
癌症治疗正越来越多地依据每位患者肿瘤的遗传特征来制定。医生已经使用 DNA 检测来发现可用特定药物靶向的突变,但这些检测无法完整反映肿瘤的行为。本研究来自 MD 安德森癌症中心,提出了一个务实的问题:如果我们同时查看 RNA——即基因的“工作拷贝”,能反映哪些基因实际被打开或关闭——是否能更好地理解患者的癌症以及他们的生存几率?
两层信息:DNA 与 RNA
每个癌细胞都携带 DNA 改变,但 DNA 大体上是静态的蓝图。相比之下,RNA 捕捉细胞在某一时刻的活跃状态。在 IMPACT2 试验中,800 多名晚期癌症患者接受了肿瘤基因分型。其中 253 名患者同时获得了 DNA 和 RNA 数据。研究者比较了在 DNA 水平上有改变的基因(例如突变或拷贝数变化)与在 RNA 水平上呈现异常高或低表达的基因,探讨这两层信息在多大程度上讲述相同的故事,以及这些信息是否与患者生存时间相关。
当基因改变与活性一致时
研究团队首先寻找“相符”的事件——即同一基因在 DNA 和 RNA 上都异常的情况。在 253 名患者中,有 50 人至少出现了一次这样的匹配,共计 23 个基因上发生了 58 次事件。大多数情况涉及基因拷贝数的增减,同时伴随该基因 RNA 水平的升高或降低,这种一致性在已知的致癌关键基因(如 CDKN2A、AR、ESR1、KRAS、PIK3CA、AKT2、TP53 和 CCND1)中最为明显。这些发现支持这样一种观点:对于某些关键癌基因,结构性的 DNA 改变确实会转化为基因活性的升高或降低,从而强化它们作为治疗靶点的重要性。
RNA 信号揭示的隐藏关系
除了逐一对应的匹配外,研究者还测试了超过 12,000 对基因,查看一个基因的 DNA 改变是否与另一个基因在 RNA 水平上的异常表达持续相关。他们发现了 123 对显著关联。许多关联聚集在一个主要的生长与存活网络——PI3K/AKT 通路,这也是靶向药物常关注的对象。一个特别显著的模式将抑癌基因 TP53 的改变与 VEGFA 的过度 RNA 信号联系起来,VEGFA 有助于肿瘤形成新血管。这一关系可能有助于解释为何某些携带 TP53 异常的患者对阻断血管生成的药物贝伐单抗有反应,也说明了 RNA 数据如何揭露 DNA 单独可能无法发现的临床相关基因间相互作用。
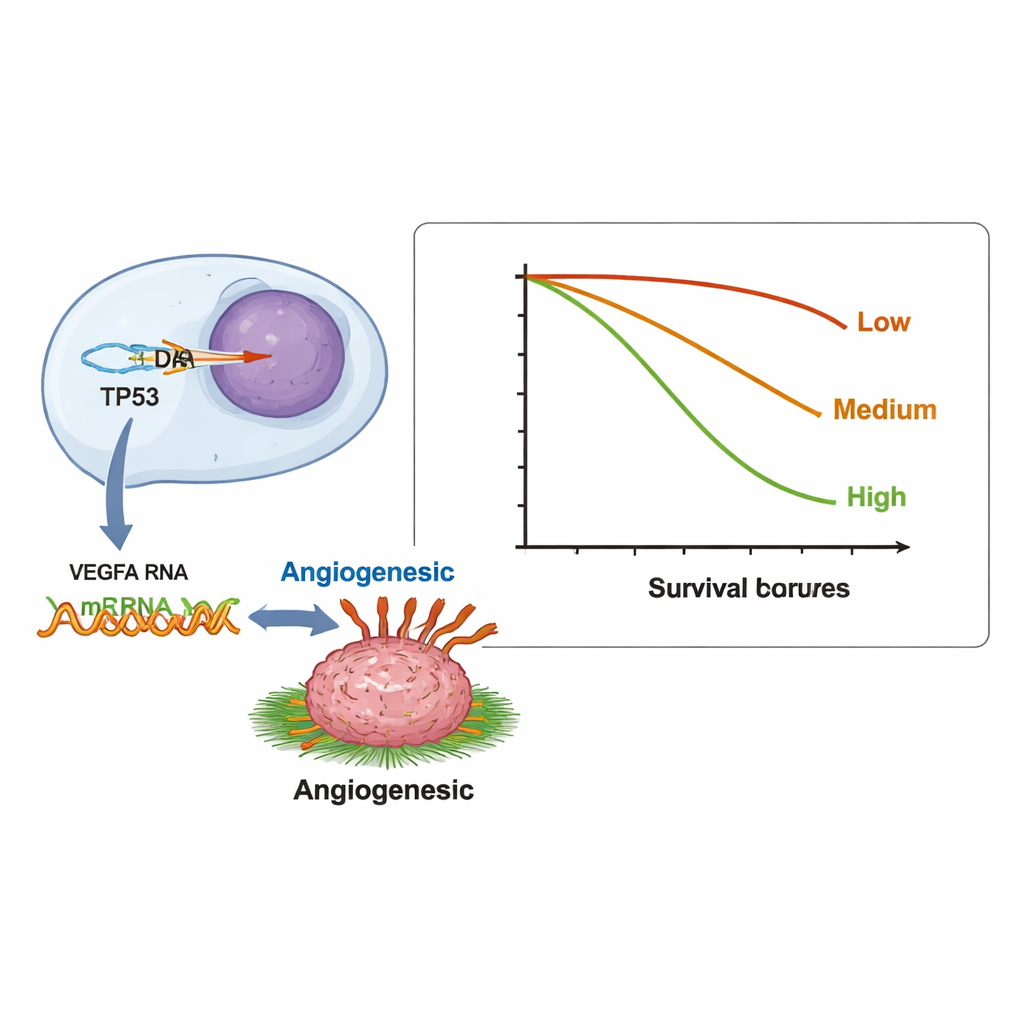
基因活性负荷与患者生存
研究者还考察了肿瘤中异常基因活性的总体数量——他们称之为肿瘤转录负荷(tumor transcriptional burden,TTB)——是否与患者生存期相关。他们统计了每位患者表现出异常 RNA 表达的基因数量,并将患者分为低(0–2 个基因)、中(3–5 个)和高(6 个或以上)三组。高组患者的中位生存期为 6.7 个月,而中低组分别为 9.8 个月和 11.9 个月。换言之,在 RNA 水平上存在大量异常基因的肿瘤往往更具侵袭性。缺乏 PD-L1(一个常用于选择免疫治疗患者的标志)的肿瘤也倾向于具有更多异常表达基因,这暗示广泛的基因扰动可能与肿瘤微环境抵御免疫攻击有关。
这对未来癌症护理意味着什么
这项研究表明,在真实世界的晚期癌症患者中,RNA 分型为 DNA 检测提供了有用且互补的信息。在某些基因中,DNA 改变与 RNA 活性一致并强化了已知的治疗靶点;在另一些基因中,RNA 模式揭示了可能指导用药的新关系,例如 TP53 与 VEGFA 之间的联系。对患者而言最重要的是,高度异常的基因活性负荷与较短的生存期相关,这表明基于 RNA 的指标可能帮助医生评估肿瘤的侵袭性并细化预后。尽管 RNA 检测尚未常规用于选择治疗方案,这些发现支持其作为精准肿瘤学下一步的潜力,尤其是随着更大规模的研究和更好的分析工具,转录组学分型有望进入日常癌症护理。
引用: Schmidt, S.T., Baysal, M.A., Fu, S. et al. Concordance analysis of DNA and RNA profiling: The MD Anderson IMPACT2 study in precision oncology. Sig Transduct Target Ther 11, 68 (2026). https://doi.org/10.1038/s41392-026-02580-0
关键词: 精准肿瘤学, RNA 分型, DNA 测序, 肿瘤转录负荷, 癌症生物标志物