Clear Sky Science · zh
通过精氨酸–mTORC1轴激活,过度谷氨酰胺分解驱动衰老与细胞衰老
这项研究对健康老龄化为何重要
衰老不仅是皱纹和白发——它还体现在全身细胞逐步丧失修复与再生能力。本文提出了一个看似简单但意义深远的问题:细胞如何“燃烧”氨基酸谷氨酰胺,是否会推动它们走向衰老?作者发现了一条此前被忽视的代谢链,将细胞处理谷氨酰胺的方式与一个强大的生长开关 mTORC1 相连,并表明该通路的过度激活会在果蝇和小鼠中主动加速细胞衰老。
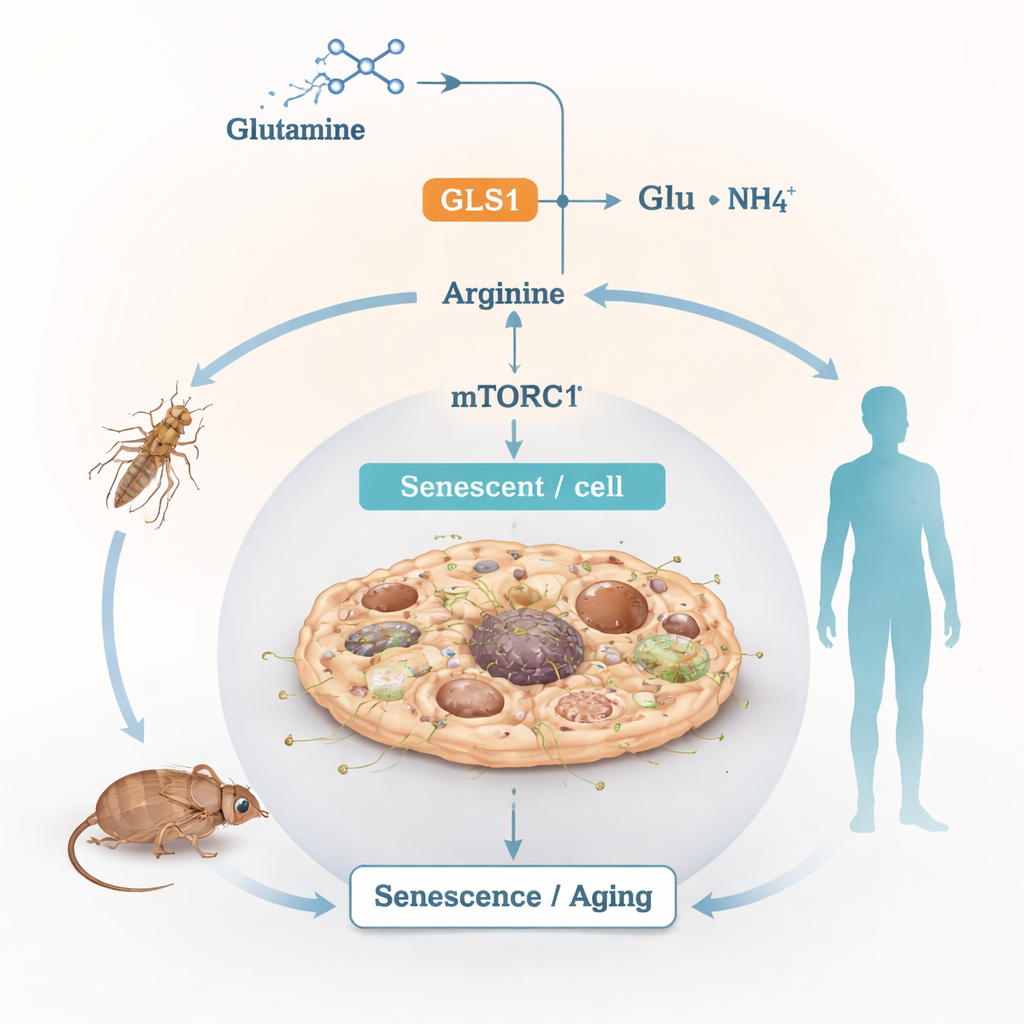
过热的燃料线
谷氨酰胺是血液和组织中最丰富的游离氨基酸。细胞将其用作多用途燃料与构建模块,通过称为谷氨酰胺分解(glutaminolysis)的过程将其分解。第一步由名为 GLS1 的酶催化,将谷氨酰胺转化为谷氨酸和铵;这些产物随后进入能量生产、抗氧化防御和其他氨基酸的合成。尽管这种分解对正常生命至关重要,作者关心的是在衰老与压力背景下,当这一过程长期过度活跃会发生什么。
在老化细胞与动物中发现“过度谷氨酰胺分解”
研究团队使用先进的代谢物谱分析,将处于分裂的年轻细胞与已停止分裂并分泌炎性因子的衰老细胞进行比较。他们发现多种氨基酸水平升高,而谷氨酰胺处于重编程网络的中心。衰老细胞摄取更多谷氨酰胺,GLS1 水平与活性更高,并积累了更多谷氨酸和铵。整体生物体中也出现类似变化:衰老的果蝇和年迈小鼠在多种组织中显示出升高的 GLS 活性。作者将这种共同表现为增强的谷氨酰胺分解状态命名为“过度谷氨酰胺分解”,并认为它是衰老的保守特征,而非微小的副作用。
抑制谷氨酰胺分解可以减缓衰老特征
既然过度谷氨酰胺分解与衰老伴随出现,它是否实际上推动了衰老?为检验这一点,研究人员用多种方法阻断谷氨酰胺分解:降低培养基中的谷氨酰胺、用药物抑制 GLS 或基因水平下调 GLS1。在受压或复制性衰老的细胞中,这些干预减少了典型的衰老标志,如 SA-β-gal 染色、细胞周期抑制因子 p16 和炎性“SASP”信号。在果蝇中,遗传敲低 GLS 或低剂量 GLS 抑制剂延长了寿命,改善了攀爬能力(活力测试),并减少了与年龄相关的肠道通透性增加。重要的是,当在压力暴露之初就限制谷氨酰胺分解时,效果并非主要通过清除老细胞实现,而是通过阻止它们首先进入衰老状态。
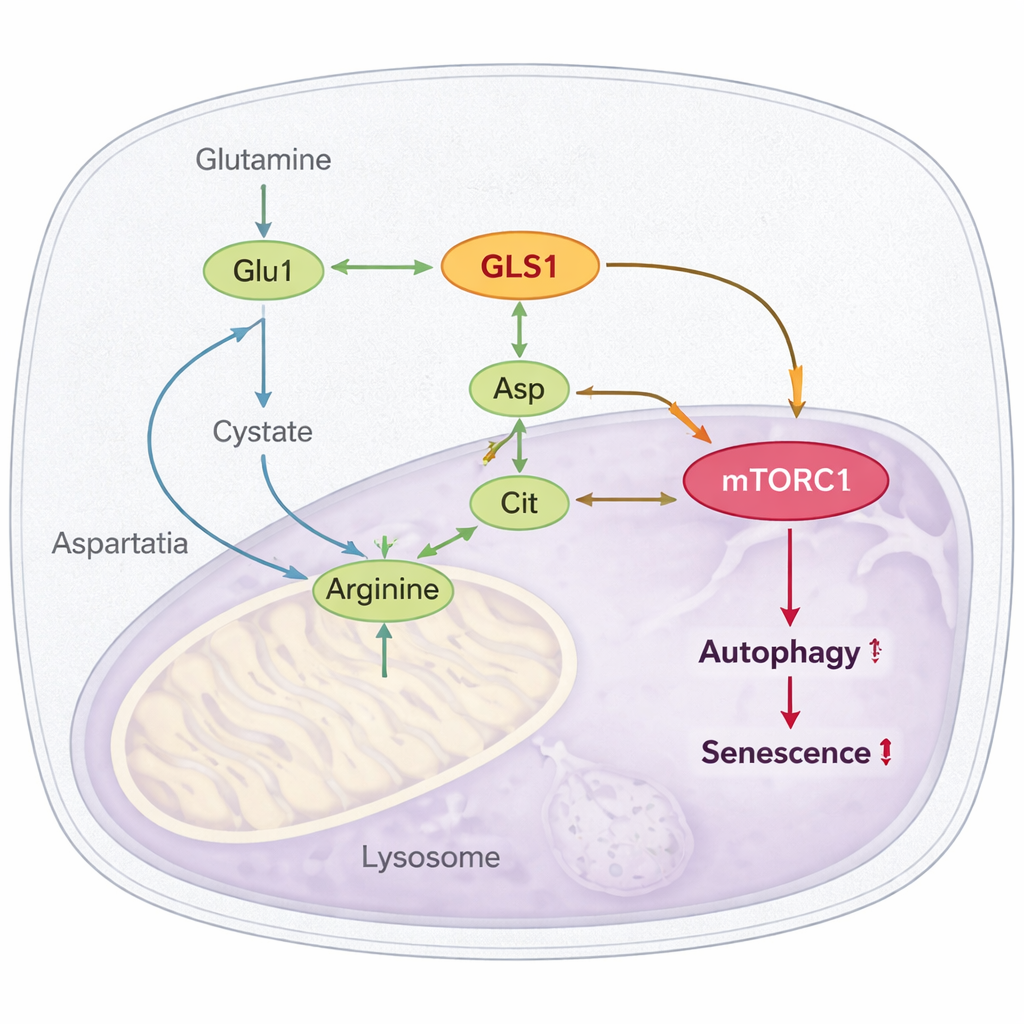
一条隐秘回路:从谷氨酰胺到精氨酸再到 mTORC1
最引人注目的发现是该过度通路如何接入 mTORC1——一个主控因子,当持续开启时已知会促进衰老并抑制细胞自噬(清理机制)。作者展示,过度的谷氨酰胺分解提升了精氨酸的生成,精氨酸是一种能直接激活 mTORC1 的氨基酸。由谷氨酰胺产生的谷氨酸和铵进入天冬氨酸和瓜氨酸的合成,再与之合成精氨酸。在衰老细胞与果蝇中,精氨酸及其前体水平上升;阻断 GLS 或敲低关键的精氨酸合成酶(ASL)会降低精氨酸并减弱 mTORC1 活性。研究还进一步证明了精氨酸传感蛋白 CASTOR1 对该效应的必要性:当 CASTOR1 被破坏时,阻断谷氨酰胺分解不再能抑制 mTORC1 或改善自噬,衰老缓解效果丧失。
好东西过量会加速衰老
为检验仅仅加强该通路是否能让细胞更快衰老,研究组在数周内向本来健康的细胞大量供应谷氨酰胺、精氨酸或中间代谢物组合。结果是衰老标志和炎性基因明显上升。在果蝇中,长期补充额外谷氨酰胺或精氨酸缩短了中位与最大寿命。综合来看,这项工作描绘了一条完整级联:过度的谷氨酰胺分解(过度谷氨酰胺分解)放大了精氨酸生成,精氨酸被 CASTOR1 感知,导致 mTORC1 异常持续活化,抑制细胞清理功能,从而促进细胞衰老和机体衰老。
这对未来抗衰策略的含义
对非专业读者而言,这项研究将谷氨酰胺代谢重新框定为一把双刃剑:它对健康必不可少,但在中晚年长期过度驱动时可能有害。通过绘制出从谷氨酰胺分解到 mTORC1 过度激活的具体路线,作者指出了新的干预节点——例如 GLS1 和 ASL 酶或精氨酸感知步骤——这些点可被调整以减缓与年龄相关的衰退,而不必完全关闭关键代谢通路。虽然将这些发现直接转化为饮食建议或治疗方案还为时过早,但这项工作为日常营养处理如何将我们的细胞推向韧性或加速衰老提供了重要线索。
引用: Chen, H., Huang, N., Xu, W. et al. Hyperglutaminolysis drives senescence and aging through arginine-mTORC1 axis activation. Sig Transduct Target Ther 11, 64 (2026). https://doi.org/10.1038/s41392-026-02576-w
关键词: 谷氨酰胺代谢, 细胞衰老, mTORC1 信号, 精氨酸生物合成, 延缓衰老干预