Clear Sky Science · zh
外源性EB病毒核抗原1诱导ADAR1驱动的肿瘤免疫疗法耐受性
为什么一种常见病毒对癌症治疗很重要
许多癌症现在使用可激活机体自身免疫系统的免疫治疗药物。然而大多数患者仍无法从中获益,因为肿瘤学会了如何躲避免疫攻击。本研究揭示了一种非常常见的病毒——埃伯斯坦—巴尔病毒(EBV)——如何帮助肿瘤关闭免疫防线并抵抗这些强效药物,以及一种新型设计分子如何可能重新开启这些防御。
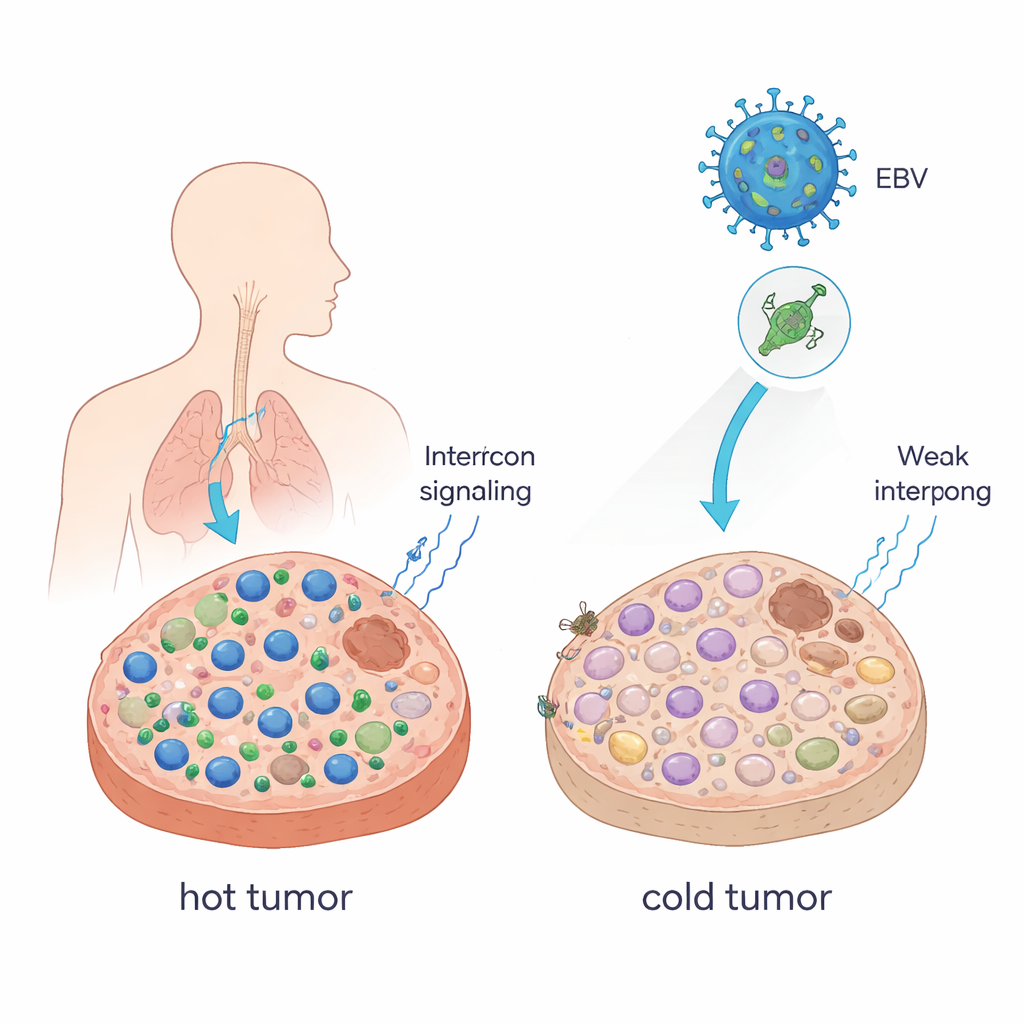
将“热”肿瘤变为“冷”肿瘤
医生常将富含杀癌T细胞的肿瘤称为“热”肿瘤,而那些这类细胞稀少的称为“冷”肿瘤。热肿瘤通常对免疫检查点抑制(ICB)药物如抗PD-1抗体反应良好;冷肿瘤则常常无效。作者表明,单一EBV蛋白EBNA1就能将肿瘤推向这种更冷、更易逃逸的状态。当他们在免疫系统完整的小鼠体内强制使小鼠肿瘤细胞表达EBNA1时,肿瘤长得更大,CD8+ T细胞和自然杀伤细胞减少,而具有免疫抑制功能的巨噬细胞增多。所谓的干扰素信号——那些帮助动员免疫细胞的关键使者——也显著降低。在与EBV高度相关的癌种鼻咽癌的患者样本中,表达EBNA1的肿瘤同样显示出比正常组织更少的CD8+ T细胞浸润。
病毒直达细胞RNA调控机器的捷径
为理解EBNA1如何重塑肿瘤微环境,研究者寻找与其发生物理相互作用的人类蛋白。他们聚焦于一种称为IGF2BP3的蛋白,该蛋白读取信使RNA上的小化学标记(m6A),能增强这些RNA的稳定性或促进其翻译成蛋白。EBNA1在多种细胞类型中,包括EBV阳性癌细胞,与IGF2BP3紧密结合。来自患者肿瘤的数据表明,高水平IGF2BP3与干扰素相关基因活性低以及较少CD8+ T细胞浸润并存,提示这种病毒—宿主联盟可能会抑制抗肿瘤免疫。
增强一种沉默危险信号的RNA编辑酶
更深入的分析突出了该相互作用的一个关键靶点:ADAR1,这是一种通过将双链RNA中的特定“A”碱基改写为“I”来编辑RNA的酶。这类编辑可以使细胞内类病毒RNA显得不那么危险,从而减少干扰素反应。作者发现,EBNA1、IGF2BP3和一个翻译因子EIF4G1在ADAR1的mRNA上形成三元复合体。该复合体增加m6A修饰,招募翻译机器,并选择性地提高ADAR1蛋白的产生,而不提升其mRNA水平。结果,肿瘤细胞在靠近干扰素相关基因的重复基因元件中进行更多RNA编辑。这些编辑减少了未编辑双链RNA的数量,而这些未编辑RNA本来会激活诸如MDA5和PKR之类的传感器,从而触发干扰素产生;编辑的增加使干扰素产生受抑,帮助肿瘤躲避免疫攻击。
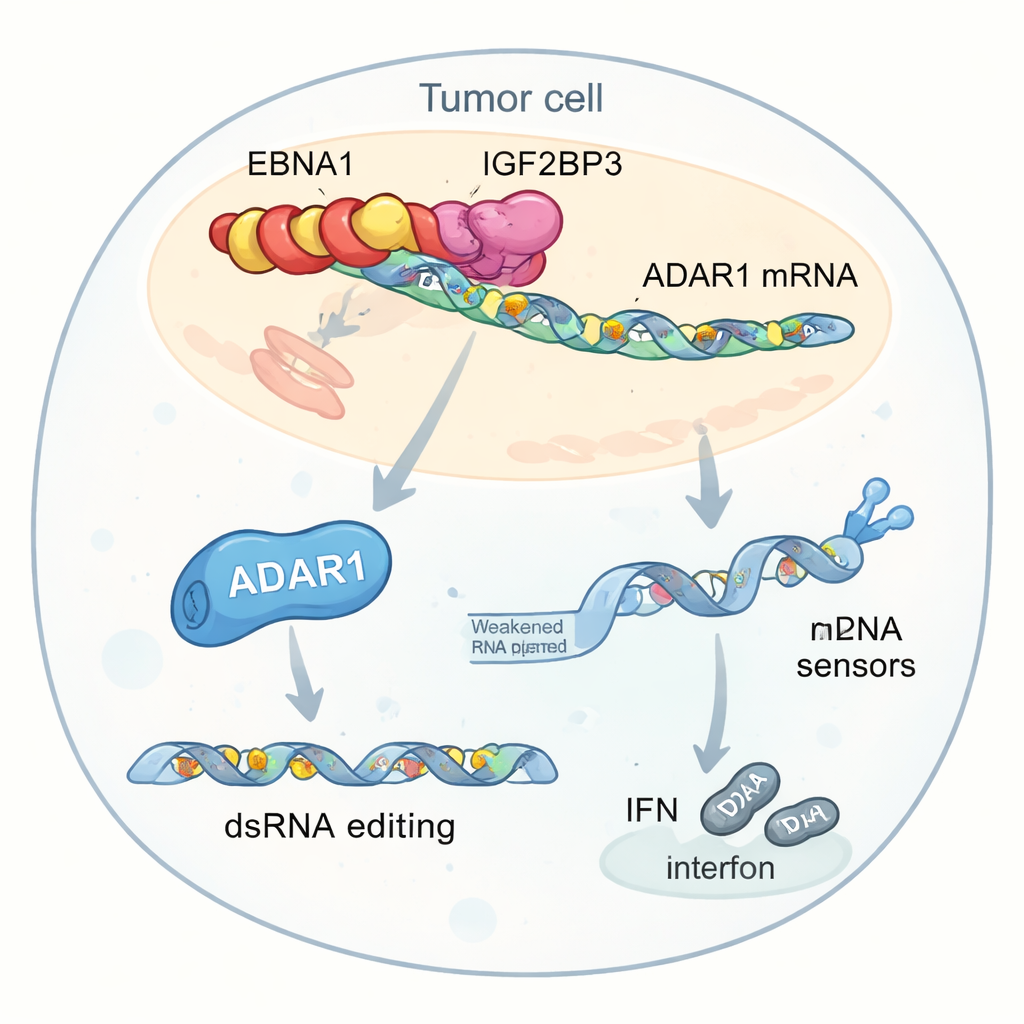
干扰素减少,免疫治疗效果削弱
当表达EBNA1的肿瘤细胞在体外暴露于T细胞和抗PD-1抗体时,它们比对照细胞更难被杀死,并且释放的干扰素更少。即使直接用干扰素处理,携带EBNA1的细胞也较不敏感,其内部RNA传感器的激活也较弱。降低ADAR1水平可部分逆转这些效应,恢复传感器活性和干扰素信号。遗传学与测序实验证实,表达EBNA1的细胞在特定RNA区域显示更多A到I的编辑事件,尤其在干扰素刺激后更为明显,进一步支持病毒促进ADAR1活性有助于中和那些本应触发强烈免疫反应的危险信号的观点。
一种能重新唤醒免疫攻击的设计型降解剂
研究团队随后探问,剥离肿瘤中的EBNA1是否能恢复其对免疫治疗的敏感性。他们设计了一种PROTAC分子EP-1215,使EBNA1被细胞自身的降解系统标记并清除。低剂量时,EP-1215高效降解EBNA1并降低ADAR1蛋白水平。在小鼠实验中,EP-1215单独对EBNA1阳性肿瘤影响有限,单用抗PD-1亦弱。但两者联用时,肿瘤明显缩小,CD8+ T细胞浸润增加,产干扰素的T细胞增多。在携带人体免疫细胞和EBV相关肿瘤的人源化小鼠模型中,组合疗法同样优于单一治疗,且未见明显肝肾毒性。
这对未来癌症治疗意味着什么
对非专业读者而言,结论是:一种常见病毒能够悄然重编程癌细胞,削弱其内部警报系统,关闭那些本可吸引并激活免疫细胞的化学信号。EBNA1通过劫持宿主的RNA读取器(IGF2BP3)和翻译因子(EIF4G1)来促使过量产生RNA编辑酶ADAR1,ADAR1则编辑掉免疫传感器本应识别的RNA结构。通过使用像EP-1215这样的定制PROTAC降解EBNA1,作者能恢复这些危险信号并使原本耐药的肿瘤再次对现有的检查点抑制药物产生反应。如果类似策略在人群中证明安全且有效,则针对诸如EBNA1的病毒辅助因子,或可为将冷的、EBV相关的肿瘤转变为能被现代免疫疗法识别和攻击的“热点”提供一种新途径。
引用: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
关键词: 埃伯斯坦—巴尔病毒, 免疫治疗耐药, ADAR1, RNA编辑, 鼻咽癌