Clear Sky Science · zh
胆固醇依赖的膜融合在 SARS-CoV-2 进入过程中的分子机制
为什么胆固醇对呼吸道病毒很重要
引起 COVID-19 的病毒 SARS-CoV-2 通过将其外层包膜与宿主细胞膜融合进入细胞。本文提出了一个看似简单但影响深远的问题:作为一种常与心血管疾病相关联的脂质,胆固醇在多大程度上影响这一融合步骤?作者表明,病毒膜中的胆固醇并非仅仅微调感染效率;它实际上帮助将病毒的刺突蛋白组织成强有力的停靠平台,从而使入侵更容易、更可靠。
构建病毒进入的简化模型
为了解析这一过程,研究者在试管中用称为脂质体的小脂泡重建了病毒–细胞相遇。一组脂质体承载 SARS-CoV-2 刺突蛋白,代表病毒膜;另一组承载 ACE2 受体,模拟宿主细胞表面。当混合并由能将刺突“切割”成融合就绪形式的特定酶激活时,这些人工膜发生融合,让荧光染料从一个脂质体转移到另一个。这一简化体系使团队能够精确调整两侧的脂质组成——包括胆固醇含量——并逐步观察融合如何展开。 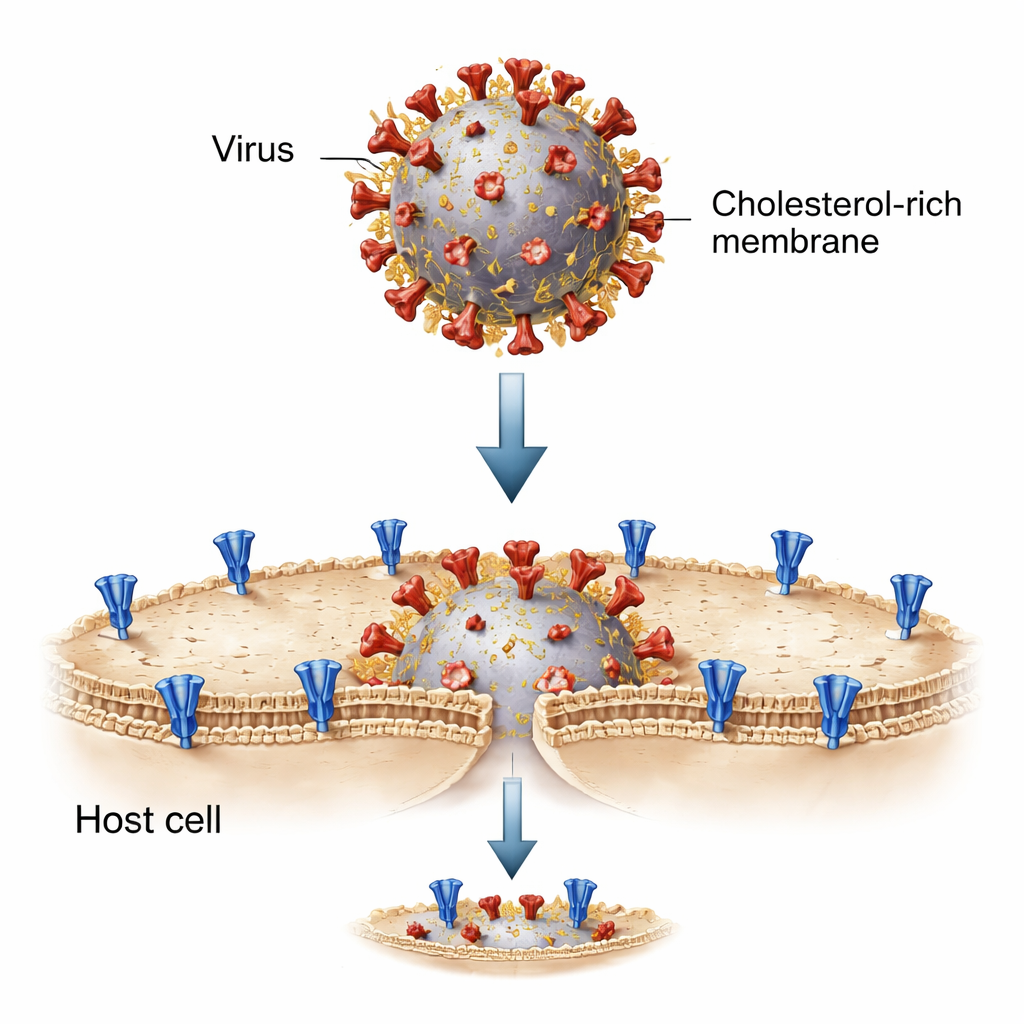
胆固醇更多地提升停靠而非融合本身
通过调节胆固醇,团队发现将胆固醇加入承载刺突的膜会使融合更频繁,但方式并非直觉所及。高胆固醇并未显著改变已附着的两片膜最终合并的概率;相反,它大幅提高了刺突膜小泡首次停靠到 ACE2 膜小泡的频率。单粒子成像显示,当刺突位于富含胆固醇的膜中时,成功停靠事件显著增多,而一对已停靠的粒子随后完全融合的概率大致保持不变。有趣的是,将胆固醇加载到 ACE2 一侧几乎无益,且在非常高水平时甚至抑制融合,这表明驱动作用主要来自病毒一侧的胆固醇而非宿主侧。
从模型膜到活细胞
研究者接着探查这一模式在活细胞中是否成立。他们改造人类细胞分别表达刺突或 ACE2,并在混合时观察它们形成大的融合结构(合胞体)。从表达刺突的细胞中去除胆固醇几乎使合胞体形成消失,而恢复胆固醇则挽救了融合。在使用 SARS-CoV-2 “假病毒”(利用冠状病毒刺突进入细胞的无害病毒颗粒)的平行实验中,从病毒膜去除胆固醇显著降低了感染性,反之按剂量依赖性地补充胆固醇可增强感染。相比之下,仅改变 ACE2 表达细胞上的胆固醇变化很小。所有检测结果一致传达一个信息:承载刺突的膜中的胆固醇对高效进入至关重要。
刺突簇:胆固醇的秘密武器
为什么病毒侧的胆固醇如此重要?对细胞膜的高分辨成像显示,在胆固醇丰富时,刺突蛋白倾向形成致密簇,而在胆固醇耗尽时则更为分散。单分子测量进一步显示,这些簇在富胆固醇条件下含有更多刺突拷贝。作者将此效应追溯到刺突尾端靠近膜的一段富含半胱氨酸的区域(CRR)。该片段通过棕榈酰化被修饰——这是一种偏向胆固醇富集膜区的脂质“锚定”修饰。当团队截短刺突尾或将十个半胱氨酸全部突变以阻断棕榈酰化时,刺突不再与胆固醇聚集,且胆固醇驱动的停靠与融合增强效应消失。 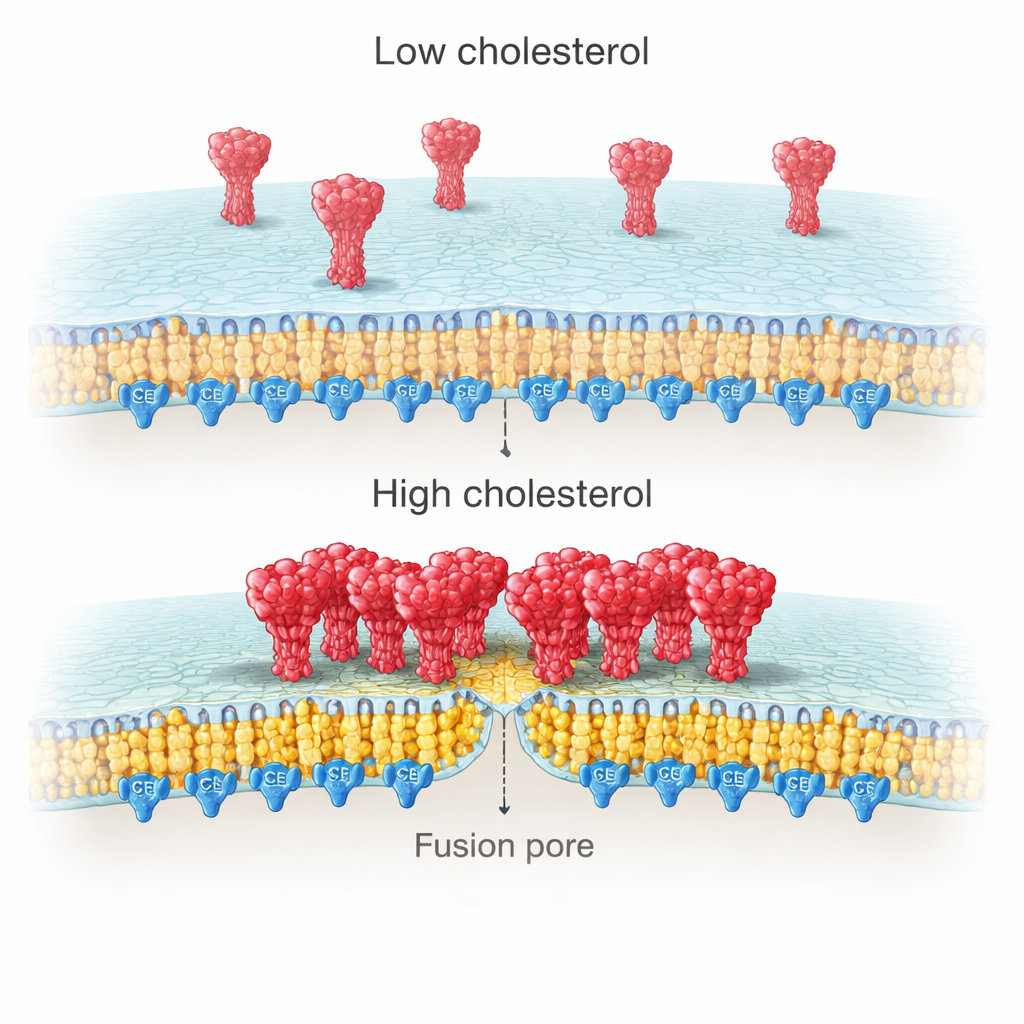
这如何助力未来治疗
简而言之,研究得出的结论是:胆固醇通过使许多刺突蛋白通过其被棕榈酰化的尾部区域聚集成紧密簇,将病毒膜转变为一个融合平台。这些簇更高效地停靠到宿主细胞的 ACE2,从而提高了任一接触事件发展为成功融合和感染的几率。对非专业读者而言,关键结论是胆固醇并非病毒外衣中的被动成分;它是刺突装置的主动组织者。这使得刺突的富半胱氨酸、对胆固醇敏感的尾部以及负责棕榈酰化的酶,成为有望对不同冠状病毒变体均有效的广谱抗病毒策略的有吸引力靶点。
引用: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
关键词: 胆固醇, SARS-CoV-2 刺突蛋白, 膜融合, 病毒入侵, 棕榈酰化