Clear Sky Science · zh
PKC-eta 通过调控 Hippo–YAP 信号通路促进乳腺癌转移
这项研究为何重要
三阴性乳腺癌(TNBC)是乳腺癌中最危险的类型之一,因为它早期发生转移且缺乏可用的靶向疗法。本研究揭示了癌细胞内一种名为 PKC‑eta(PKCη)的特定酶如何充当“主开关”,帮助肿瘤细胞脱落、在体内迁移并在远处播种新肿瘤。通过理解这一开关,研究者还发现了一种能将其关闭的小型天然肽,指向一种潜在的新型治疗途径,可用于应对这种侵袭性疾病。 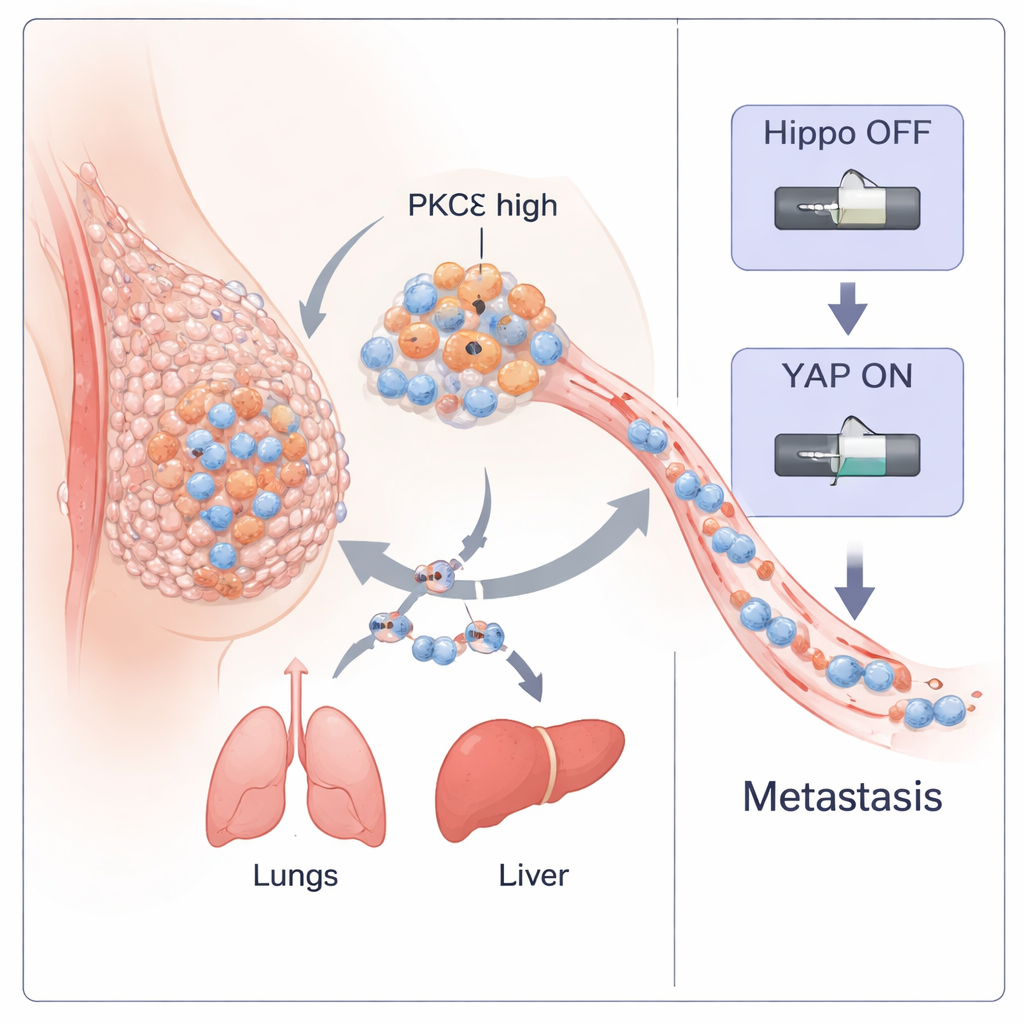
侵袭性乳腺肿瘤中的隐性驱动因子
研究团队首先挖掘了大量乳腺癌患者数据,发现编码 PKCη(基因名 PRKCH)的表达在一种称为“claudin‑low”的肿瘤亚型中特别高,该亚型与三阴性乳腺癌高度重合,并富含具有干样特征且高度可迁移的细胞。在多个患者队列中,PRKCH 高表达的肿瘤显示出强烈的上皮–间质转化(EMT)基因特征——这是一种细胞失去原本紧密连接、形态改变并变得更具侵袭性的过程。PRKCH 水平在转移样本中也高于原发肿瘤,且对人类 TNBC 组织的蛋白免疫染色显示在高级别、晚期肿瘤中存在更多活跃的、靠近细胞核的 PKCη。综合这些发现表明,PKCη 与肿瘤的侵袭性和转移密切相关。
从培养皿到小鼠:证明 PKCη 促进转移
为检验因果关系,研究者用 CRISPR 基因编辑从两种高度转移性的 TNBC 细胞系中去除了 PKCη,一种小鼠细胞系(4T1)和一种人类细胞系(MDA‑MB‑231)。缺失 PKCη 后,细胞向更“上皮性”状态转变:黏附蛋白如 E‑cadherin 和 EpCAM 增多,而经典的间质标志物(如波形蛋白和 N‑cadherin)减少。缺失 PKCη 的细胞形成的克隆更少更小,迁移和侵袭能力下降,悬浮状态下对细胞死亡更敏感,并且癌症干细胞特征显著下降,包括 CD44high/CD24low 和 ALDH 阳性细胞减少,以及球体形成能力降低。注射到小鼠体内时,缺失 PKCη 的细胞形成的原发肿瘤更小,肺、肝、脑及其他器官的转移显著减少;小鼠存活期也延长。恢复 PKCη 能逆转这些变化,证明该酶主动促进 TNBC 的进展和转移。
PKCη 如何劫持生长控制通路
研究进一步聚焦 PKCη 如何发挥这种促转移作用。患者数据表明,PKCη 的水平与 YAP 同步升降——YAP 是受 Hippo 通路调控的一个强效基因调控蛋白,Hippo 通路相当于细胞的“安全刹车”,通常限制生长。PRKCH 或 YAP1 的高表达都预示着较差的患者结局,而两者同时高表达则与远处无转移生存期显著更差相关。在 TNBC 细胞中,删除 PKCη 会降低总 YAP 水平并使其从细胞核转移到细胞质,处于失活状态。生化实验显示 PKCη 与 YAP 发生物理结合,并特异性地在 Ser128 位点为 YAP 添加磷酸化标记。这一修饰稳定了 YAP 并有助于其进入细胞核,启动驱动 EMT、干性和转移的基因表达。当 PKCη 缺失时,YAP 则在其他位点(Ser127 和 Ser397)被磷酸化,这促使其结合 14‑3‑3 蛋白、被滞留于细胞质并最终被降解。PKCη 还提升了抑癌蛋白 PTEN 的水平——PTEN 是对 AKT 酶的天然抑制因子,从而保持 AKT 活性较低并抑制上游会使 YAP 失活的 Hippo 激酶。通过这两条途径,PKCη 一方面直接激活 YAP,另一方面间接关闭 Hippo“刹车”。 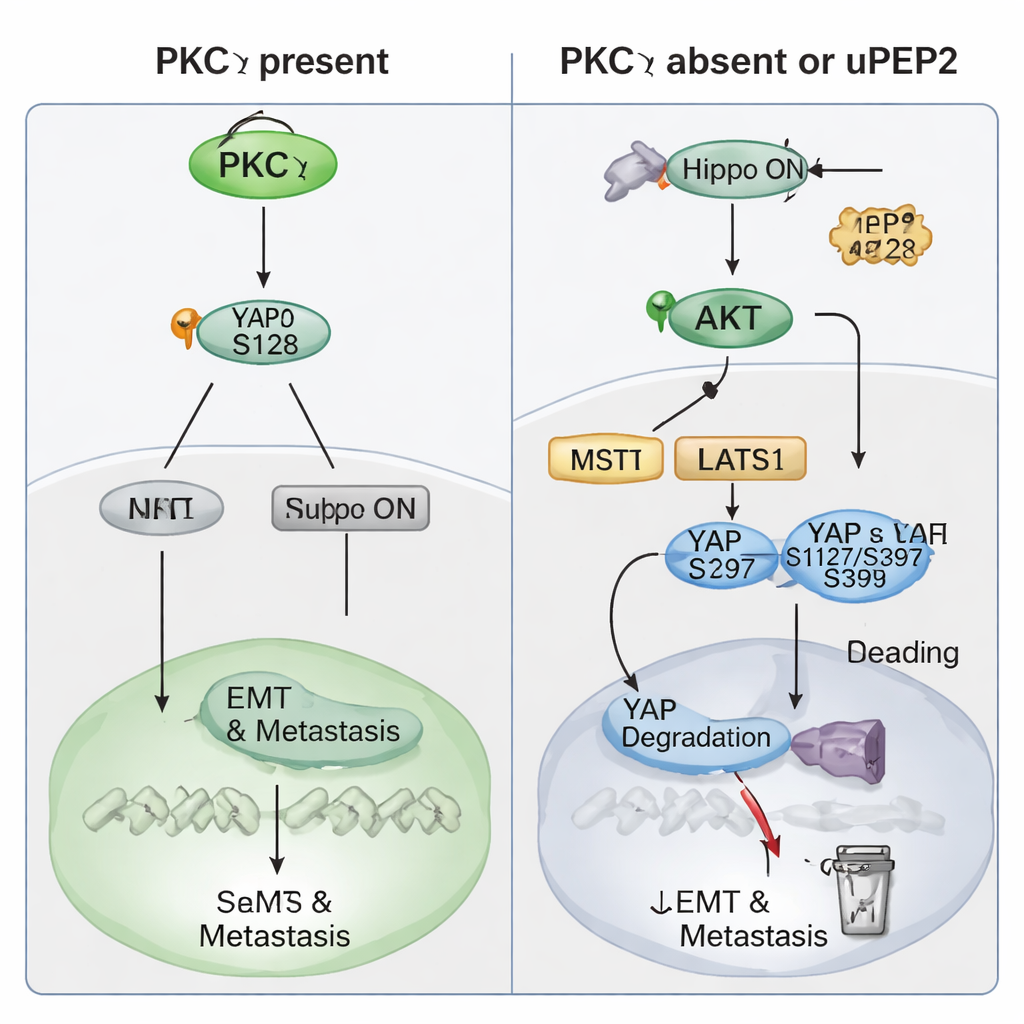
一个能解除癌症开关的小肽
有趣的是,PKCη 基因包含一个短的上游开放阅读框(uORF),编码一种称为 uPEP2 的微肽。先前研究显示 uPEP2 能结合并抑制 PKCη 及相关酶。在本研究中,用合成 uPEP2 处理 TNBC 细胞模拟了 PKCη 基因敲除的效应:迁移、侵袭和干样行为均下降,EMT 标志物向较不侵袭的模式转变,YAP 水平下降且其“失活”磷酸化标记增加。在小鼠肿瘤模型中,uPEP2 降低了原发肿瘤中的 PKCη 和 YAP,增加了 YAP 的失活,并与肝脏和肺部微转移的减少相关。机制上,uPEP2 促使 PKCη 被降解,使 Hippo 通路重新被激活,推动 YAP 被滞留于细胞质并被降解。
对未来治疗的意义
对非专业读者来说,关键信息是研究者确定了 PKCη 作为一个枢纽因子,帮助最具侵袭性的乳腺癌通过关闭自然的生长控制系统并激活 YAP“油门”来松散、迁移并在远处定植。通过敲除 PKCη 或使用天然小肽 uPEP2 促使其降解,研究者能够恢复 Hippo 的安全刹车、抑制 YAP,并在临床前模型中显著减少转移。尽管该工作仍处于实验阶段,并在细胞系和免疫缺陷小鼠中完成,但它强调了 PKCη 及其与 YAP 的相互作用作为 TNBC 新疗法的有前景靶点,并提示类似 uPEP2 的药物有望在未来帮助预防或限制这种难治性癌症的扩散。
引用: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
关键词: 三阴性乳腺癌, PKC-eta, Hippo-YAP 通路, 上皮-间质转化, 癌症转移