Clear Sky Science · zh
骨关节炎:分子发病机制与潜在治疗选择
当日常关节痛成为全身性问题
酸痛的膝盖或僵硬的手指常被视为衰老无法避免的一部分。然而骨关节炎——全球最常见的关节疾病——并非仅仅是“磨损”。这篇综述文章揭示了在疼痛关节内部真正发生的事情,从误发的痛觉神经到过度工作的细胞机器,并探讨了新一代远超止痛药的治疗手段。
常见疾病,却付出沉重个人代价
骨关节炎影响近8% 的全球人口,数以亿计的人长期承受慢性疼痛和活动受限。该病更常见于女性、55岁以上人群,以及超重者或因工作和运动对关节反复施加较大压力的人。现行标准治疗——运动、减重、支具、抗炎药、关节注射以及在严重情况下的关节置换——可以缓解症状,但很少能阻止疾病持续恶化。治疗需求与可用疗法之间的差距促使科学家更深入地研究骨关节炎如何发起以及为何会如此疼痛。
关节为何疼痛:电路、化学物质与信号
骨关节炎的疼痛并不能仅靠X光解释:有些损伤不严重的人却痛得厉害,而有些严重改变的人却感觉不明显。文章描绘了从膝关节到脊髓再到大脑的疼痛路径。关节内的神经末梢——特别是细薄的Aδ 和C纤维——浸泡在一锅炎性化学物质中,包括白细胞介素和肿瘤坏死因子,以及神经生长因子。这些物质开启神经末梢中特别的通道,通透钠和钙,使神经更易、更频繁地发放冲动。随着时间推移,脊髓和大脑的疼痛通路可能变得过度敏感,以致正常运动或轻微的寒冷都会感到剧烈灼痛。
关节细胞内部的隐性负荷
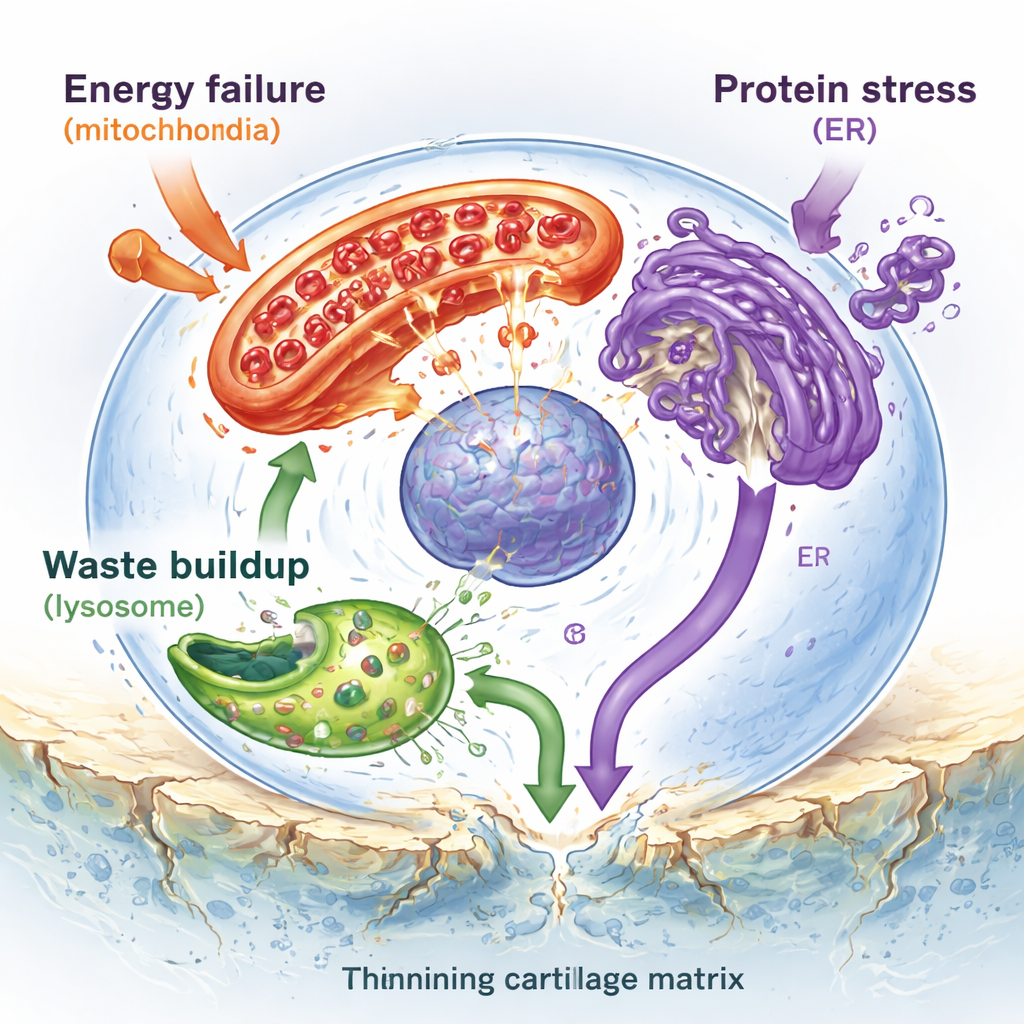
在软骨深处,唯一的驻留细胞——软骨细胞——正努力维持使骨骼顺滑滑动的弹性基质。作者指出这些细胞在多方面受到围攻。线粒体——细胞内微小的能量工厂——受损且效率下降,产生过少的能量并产生过多的活性氧,损伤DNA与蛋白质。溶酶体作为细胞的回收中心,被硬矿物晶体压垮,膜变弱,导致破坏性酶泄漏入细胞并触发细胞死亡。内质网——新蛋白折叠的膜迷宫——被错误折叠的分子堵塞,激发慢性的“应激反应”,最终将细胞推向自毁。各类受损的细胞器共同助长炎症,加速软骨的丧失与钙化。
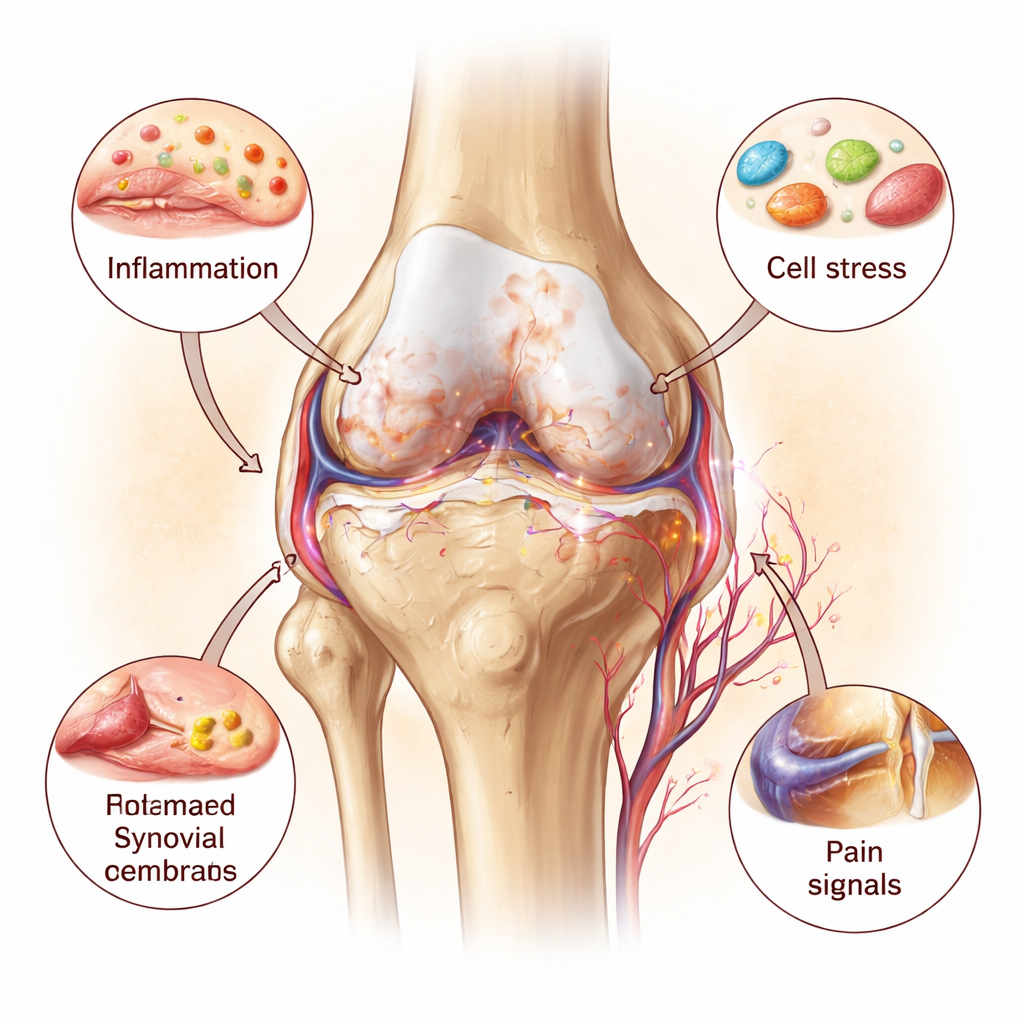
炎症:火上浇油
炎性信使分子是这一过程的扩音器。三种尤其重要的分子——白细胞介素‑1、白细胞介素‑6 和肿瘤坏死因子‑α——与细胞器损伤形成恶性循环。它们驱使软骨细胞产生分解软骨的酶,并促进关节面下异常的骨生成。与此同时,受损的线粒体和渗漏的溶酶体释放自身的求救信号,进一步激活关节内的免疫传感器。血管和痛觉纤维长入通常安静且无神经的软骨区域,提高了疼痛敏感性。整体的关节视角将骨关节炎描绘为一种进展缓慢但自我强化的炎性疾病,而非被动的机械性软骨磨损。
新治疗思路:从离子通道到细胞“能量工厂”
凭借这张机制图,研究者正在测试新的药物和递送系统。在止痛方面,实验性药物通过阻断或温和去敏化诸如TRPV1(辣椒素受体)、TRPA1、TRPM3/8及特定钠通道(Nav1.7 和 Nav1.8)等神经通道,或中和神经生长因子以防止神经过度敏感。在改变病程方面,靶向抗体旨在调低关键炎性细胞因子,而小分子和“清除衰老细胞”药物则试图恢复更健康的细胞行为。一个特别令人振奋的前沿是针对细胞器的治疗:能够刺激线粒体自净(mitophagy)、稳定溶酶体酸性与膜完整性,或缓解内质网应激的化合物。复杂的纳米颗粒、脂质体和工程化外泌体正被设计用于定位软骨细胞乃至特定细胞器,将药物精确递送到所需之处。
这对骨关节炎患者意味着什么
文章总结称,骨关节炎应被视为并治疗为一种复杂的生物学疾病,涉及紊乱的细胞代谢、慢性低度炎症和不适应的疼痛回路。尽管许多提出的药物和递送系统仍处于早期实验室或动物检测阶段,但它们指向一个未来:治疗将同时是多模态且个体化的——通过平息过度活跃的神经缓解疼痛,同时保护或恢复关节自身的细胞及其内部机器。对患者而言,这最终可能意味着不仅让活动更不痛苦,而且能减缓甚至逆转今天往往被视为不可避免的结构性损伤。
引用: Zhang, Y., Han, Y., Sun, Y. et al. Osteoarthritis: molecular pathogenesis and potential therapeutic options. Sig Transduct Target Ther 11, 81 (2026). https://doi.org/10.1038/s41392-025-02556-6
关键词: 骨关节炎, 关节疼痛, 软骨, 炎症, 线粒体