Clear Sky Science · zh
基于纳米颗粒的光疗系统:分子机制与临床应用
光:一种温和的医疗工具
大多数人把光看作让我们看见、给皮肤带来温暖或为太阳能电池供能的东西。本文综述探讨了一个更令人惊讶的角色:通过精确调控的光结合微小的工程化颗粒,从内到外诊断和治疗疾病。作者描述了“基于纳米颗粒的光疗”如何将损伤聚焦于癌细胞,缓解心脏和关节的炎症,甚至帮助大脑清除如阿尔茨海默病等疾病中的有毒蛋白,同时尽可能保护大部分健康组织。
微小颗粒如何将光转化为药物
这一方法的核心是纳米颗粒——比人类头发宽度小数千倍的结构,它们可以携带药物、吸收光并将光转化为热或瞬时的化学爆发。主要有两种策略。在光动力疗法中,颗粒表面或内部的光激活分子产生活性氧物种——高能量的氧形式,可刺穿邻近的细胞组分。在光热疗法中,另一些颗粒,如金或黑磷,将近红外光转化为热量,从内部短暂加热肿瘤细胞而导致其死亡。由于光可以定向照射且颗粒可被设计为主要在病变组织中富集,医生因此获得了传统化疗和放疗所缺乏的空间精确性。 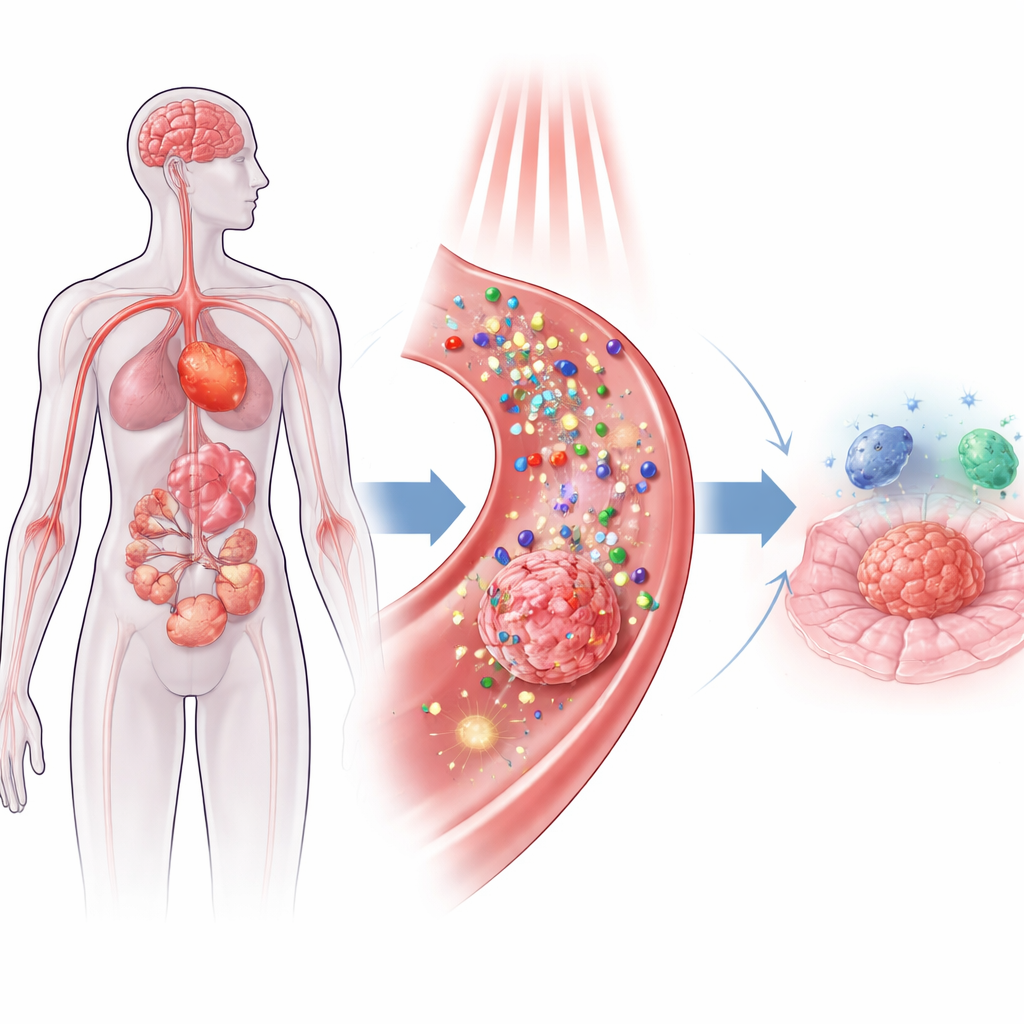
构建更智能的载体与递送路径
仅仅向身体照射光不够;挑战在于把合适的颗粒送到正确的位置并让它们停留足够长的时间发挥作用。综述列举了一套递送系统工具箱,包括脂质体等软载体、固体脂质颗粒与基于聚合物的球体或胶束,以及由二氧化硅、金属、碳或金属有机框架构建的刚性支架。它们的表面可以被隐形聚合物包覆以延长循环时间、用天然细胞膜来躲避免疫防御,或带有识别癌细胞或炎性细胞标志物的“地址标签”。一些设计具有“智能”特性:在血液循环中保持惰性,但在肿瘤内的酸性、酶或氧化还原环境中改变尺寸、电荷或形状,仅在需要处释放内容物。
光照下细胞内部发生了什么
一旦光被开启,一连串分子事件便展开。作者解释了光激发颗粒如何产生氧化剂爆发,攻击膜、DNA以及线粒体和溶酶体等关键结构。这可以使细胞进入有序的自我毁灭(凋亡),或在损伤严重时进入更混乱的死亡方式。细胞也可能增强自噬——一种内部回收过程,能在温和压力下帮助细胞存活,或在被压垮时加速其灭亡。关键在于,死亡的肿瘤细胞会释放“危险”信号以召集免疫系统:在表面暴露某些蛋白、释放吸引树突状细胞的因子,并将肿瘤相关免疫细胞从抑制性状态重塑为抗肿瘤状态。实际上,局部的光治疗可同时起到个性化癌症疫苗的作用。 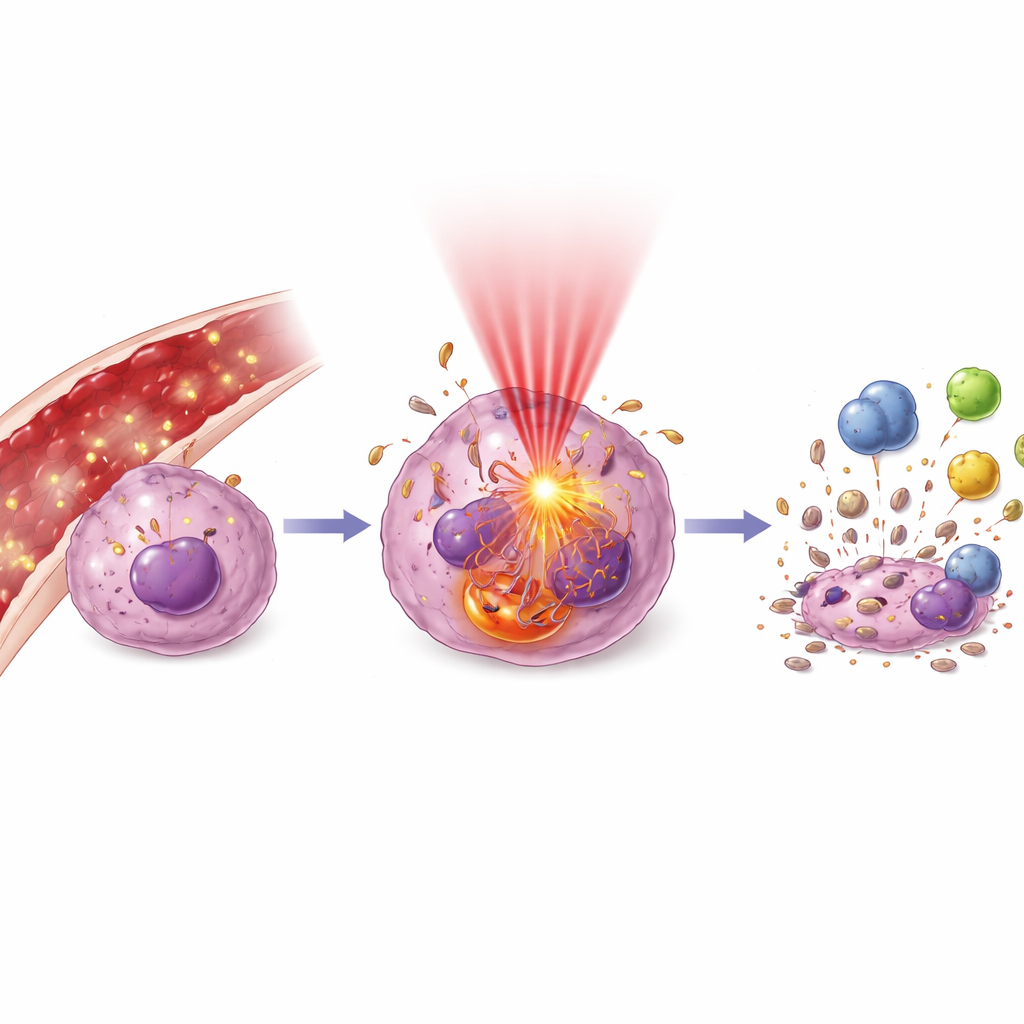
超越癌症:心脏、大脑与自身免疫靶点
尽管癌症是最为成熟的应用领域,相同的原理也被用于慢性疾病的适配。在心血管疾病中,基于光的方法目标并非杀死细胞,而是减少氧化应激、稳定血管内皮细胞,甚至帮助缩小或钙化危险斑块。在大脑中,由于神经元高度敏感,更温和的光方案——通常称为光生物调节——旨在提升线粒体能量产出、减少有毒蛋白团块并抑制小胶质细胞和星形胶质细胞驱动的炎症。综述还强调了代谢和自身免疫疾病方面的早期工作,在这些领域,适当剂量的光与纳米颗粒可以将免疫细胞从侵袭性、损伤组织的行为引导到更具调节性和镇静性的角色,同时在一定程度上改善胰岛素敏感性和脂肪组织信号传导。
从实验室到临床:希望与障碍
尽管研究几十年,只有少数光激活药物获得全面批准,主要用于眼病和某些肿瘤。作者认为,纳米技术正开始开启下一波机会,使光更深地穿透、更好地靶向,并内置成像以实时监控治疗。然而重大障碍依然存在:如何以一致质量放大纳米颗粒生产、证明长期安全性及体内清除、有效将光传递到深部器官,以及满足严格的监管要求。综述结论指出,通过将材料科学、光学、生物学与人工智能引导的设计相结合,基于纳米颗粒的光疗有望从利基手段演变为更广泛的、非侵入性的精准医学支柱。
引用: Chauhan, D.S., Prasad, R., Dhanka, M. et al. Nanoparticles-based phototherapy systems: molecular mechanisms and clinical applications. Sig Transduct Target Ther 11, 95 (2026). https://doi.org/10.1038/s41392-025-02536-w
关键词: 纳米颗粒光疗, 光热疗法, 光动力疗法, 癌症纳米医学, 光生物调节