Clear Sky Science · zh
IFFO1通过LaminA/C–PGC1α轴协调线粒体分裂与脂肪酸合成,从而抑制乳腺癌
这项研究为何重要
乳腺癌仍是女性癌症死亡的主要原因之一,部分原因在于某些肿瘤持续生长、转移并逃避免疫或治疗手段。本研究揭示了一个此前未被充分重视的细胞“刹车”分子――IFFO1,它通过抑制两个支持肿瘤生长的核心引擎(细胞能量工厂线粒体和脂质合成储存系统)来减缓乳腺癌进展。理解这个刹车机制为跨多种乳腺癌亚型的潜在治疗策略提供了新的视角。
位于乳腺细胞内的隐秘守护者
研究人员首先分析了来自30名乳腺癌患者的样本以及大型公开癌症数据库,发现肿瘤组织中IFFO1蛋白水平持续低于邻近正常乳腺组织。癌症分期越晚,IFFO1越少;而肿瘤中IFFO1较高的患者通常具有更长的生存期。在体外培养的乳腺癌细胞中,强制过表达IFFO1显著抑制了细胞的增殖、分裂和迁移——这些行为是肿瘤扩张和转移所必需的。IFFO1还抑制了一种称为上皮-间质转化(EMT)的细胞程序,该程序帮助癌细胞脱离并侵袭其他组织。
平息过度活跃的能量工厂
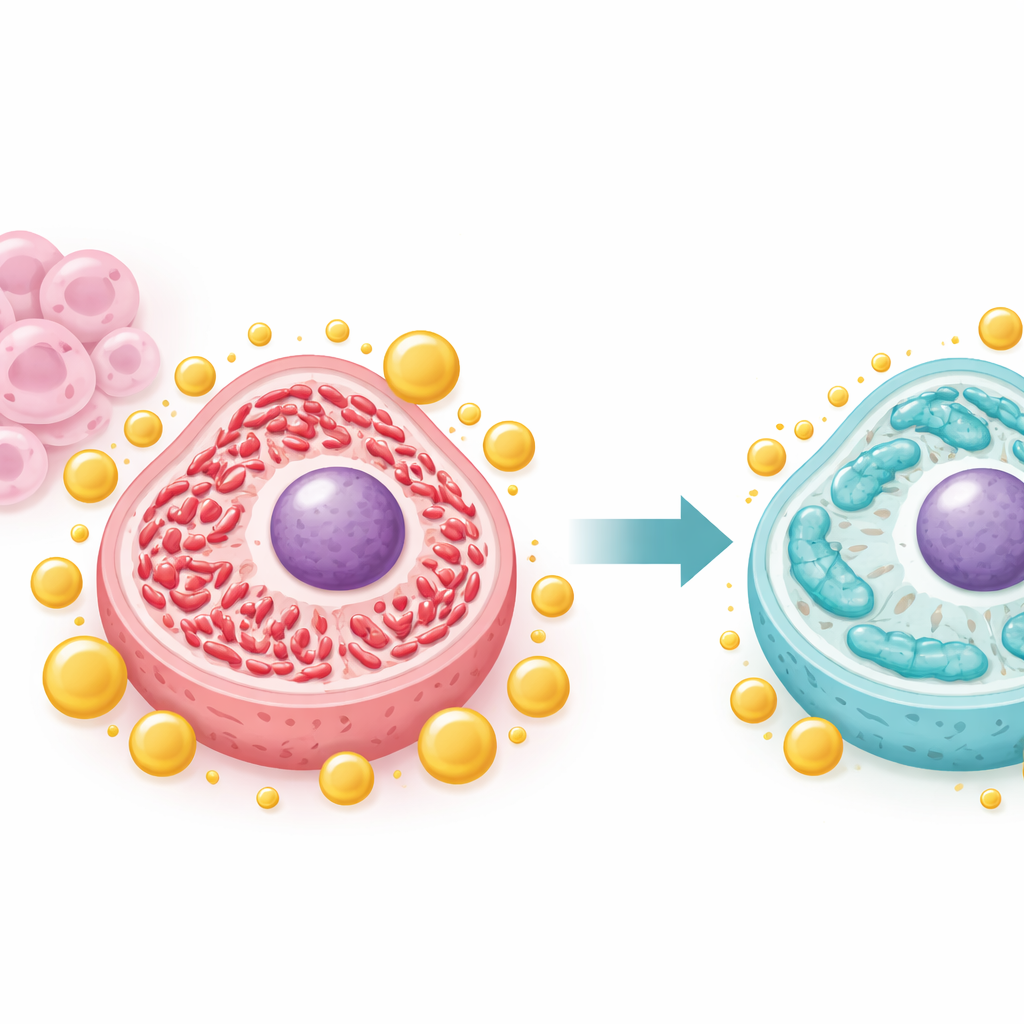
癌细胞常通过重塑线粒体来满足快速生长的需求。团队显示IFFO1将线粒体状态从高度碎裂的“分裂”态转向更为延长的“融合”态,后者通常与更健康、更稳定的线粒体相关。当IFFO1丰富时,关键分裂蛋白如Drp1和Fis1下降,而融合蛋白上升。显微镜观察显示线粒体变得更长且不再高度片段化,线粒体DNA含量和能量输出也从侵袭性细胞中异常升高的水平回落。这些变化提示IFFO1阻止线粒体进入支持失控肿瘤生长的超活跃构型。
切断脂质补给线
快速生长的肿瘤不仅需要能量,还需要持续的脂质供应以构建新膜和信号分子。研究发现IFFO1同样抑制了这一代谢加速器。在过表达IFFO1的细胞中,核心脂质合成蛋白(包括FASN、SREBP‑1、SCD1等)水平降低。酶学检测证实脂质合成活性降低,化学测定显示游离脂肪酸、甘油三酯和胆固醇含量下降。标记脂质储存的染料显示脂滴减少、细胞内中性脂总体减低。相反,提高分裂蛋白Drp1则促进脂质生成,而沉默Drp1可抑制脂质生成——支持线粒体形态与癌细胞脂质供应之间的直接联系。
从细胞核到线粒体的信号链
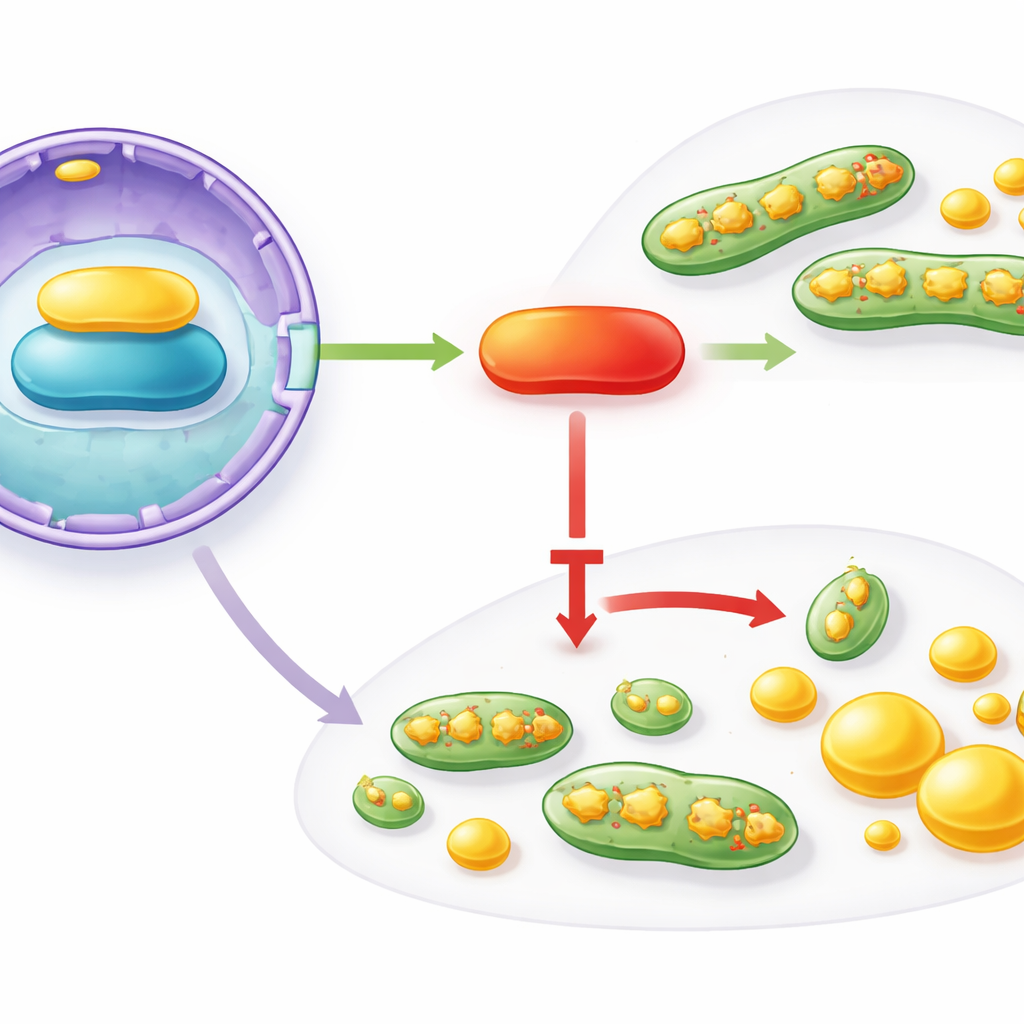
IFFO1如何协调这些广泛变化?作者追踪到一条从细胞核到线粒体及脂质合成机器的相互作用链。IFFO1可与核包膜结构蛋白Lamin A/C发生物理结合并提升其水平。Lamin A/C反过来支持PGC1α的活性,PGC1α是一个调控线粒体健康与代谢的主控因子。在乳腺癌组织和细胞中,Lamin A/C与PGC1α均表现降低,类似于IFFO1的丢失。当研究者人工提升IFFO1时,Lamin A/C和PGC1α上升,线粒体分裂减少,脂质合成减弱。敲低Lamin A/C会消除这些益处,但恢复PGC1α则能将其带回,指出IFFO1 → Lamin A/C → PGC1α轴在功能上抑制了促进肿瘤的线粒体和脂质改变。
在活体动物中测试这一刹车
为验证这些细胞效应是否可转化为真实肿瘤抑制,团队将有或没有额外IFFO1的人源乳腺癌细胞植入小鼠体内。过表达IFFO1的肿瘤生长更慢、实验终点时质量更轻,并显示出较少的脂质堆积。在一项通过将癌细胞注入血流以播散肺转移的模型中,过度表达IFFO1的细胞在肺部形成的肿瘤结节明显更少。这些小鼠的组织分析与细胞培养结果一致:Lamin A/C与PGC1α更高、线粒体分裂减少、脂质合成降低。
对未来治疗的意义
总体而言,这项工作将IFFO1呈现为一个多层次的肿瘤抑制因子,连接了细胞的结构支架、能量工厂与脂质合成机械。通过稳定Lamin A/C并促进PGC1α,IFFO1防止线粒体过度碎裂并切断癌细胞依赖的脂质过度生成。对非专业读者来说,关键结论是这一蛋白在抑制驱动乳腺癌生长与转移的能量与构建材料方面起到类似内在刹车的作用。将来提升IFFO1水平或模拟其对Lamin A/C–PGC1α通路作用的药物,可能为尤其中度侵袭性或耐药性乳腺癌提供新的治疗选择。
引用: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
关键词: 乳腺癌, 线粒体动力学, 脂肪酸合成, 肿瘤代谢, PGC1α通路