Clear Sky Science · zh
共培养癌细胞与宿主细胞的转录组谱分析识别出缺氧为骨骼肌对癌细胞抗增殖作用的驱动因子
为何某些组织能抵抗癌细胞扩散
癌症致命通常是因为肿瘤细胞逃离原发部位并在远处器官定植。有趣的是,某些组织如肺是常见的落脚点,而其他组织如骨骼肌几乎不被癌细胞占据,尽管其占据大量体重。本研究提出一个对患者和临床医生都重要的简单问题:肌肉究竟有什么特性使其成为对癌细胞生长极为不友好的“土壤”,理解这种天然防御是否能改变我们对转移治疗的思路?
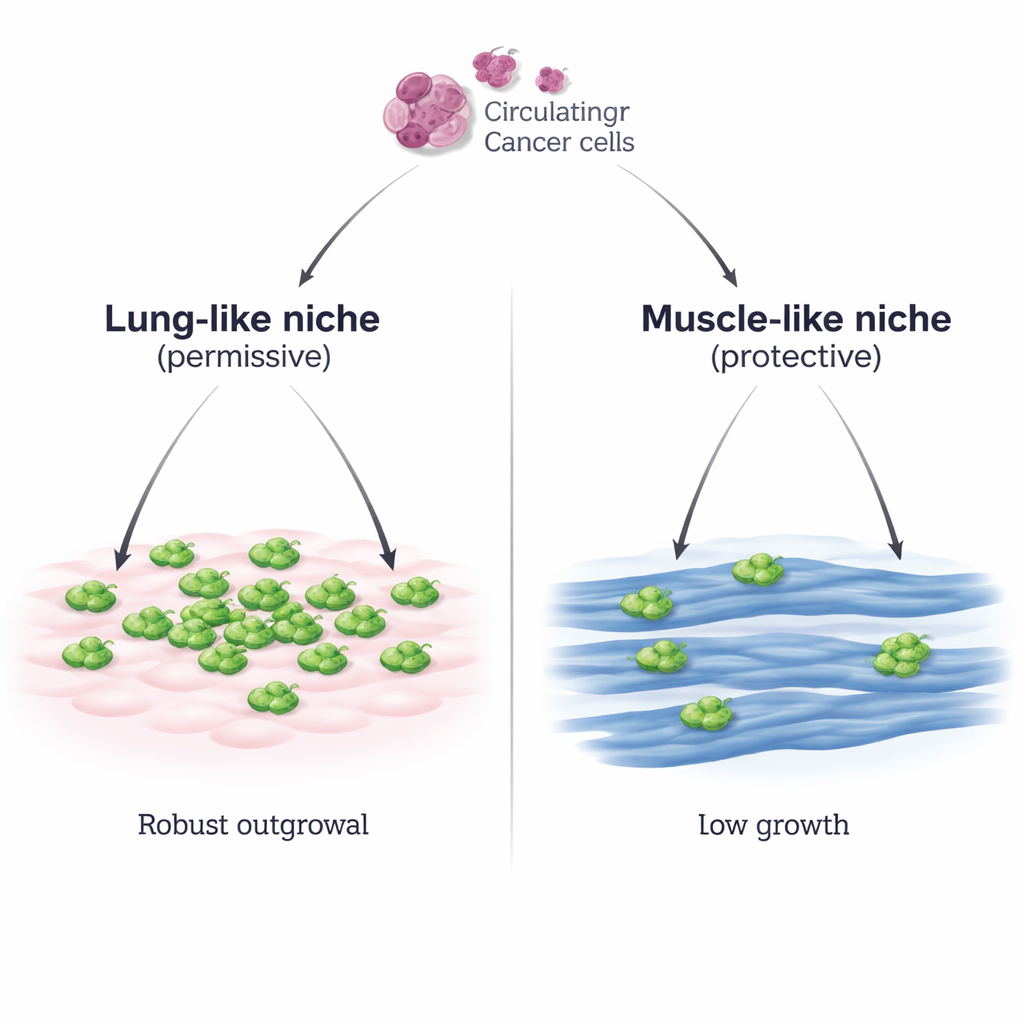
两种肿瘤细胞可能遇到的“社区”
研究者建立了一个受控的实验体系,模拟乳腺癌细胞可能遇到的两种不同“社区”:由肺成纤维样细胞(MLg)构成的类肺环境,以及由成熟骨骼肌纤维(C2C12 骨骼肌管)构成的类肌肉环境。他们将小鼠乳腺癌细胞置于每层之上并观察其命运。在类肺细胞上,癌细胞附着良好并迅速增殖,形成致密斑块。在肌肉细胞上,癌细胞附着同样良好,但生长呈稀疏且缓慢,即便起始接种量显著增加或使用第二条乳腺癌细胞系亦是如此。另一条骨骼肌细胞系(Sol8)也显示出同样抑制癌细胞生长的能力,强调这是肌细胞的一般特性,而非某一细胞系的个别现象。
癌细胞与宿主细胞如何重编程其活性
为了弄清细胞内发生了什么,团队从共培养体系中分离出癌细胞和宿主细胞并对它们的RNA进行了测序,RNA反映了哪些基因被开启或关闭。与在肺细胞上生长的癌细胞相比,位于肌肉纤维上的癌细胞经历了更大范围的基因表达变化,表明肌肉环境强迫它们进行显著适应。在肌肉环境中,癌细胞激活了与肌肉样特征、能量代谢以及令人意外的低氧(缺氧)反应相关的基因程序。与此同时,通常驱动快速细胞分裂的基因程序被下调。相比之下,生长在肺细胞上的癌细胞保持明显以增殖为导向的表达谱,所需的重编程更少,这与类肺生态位对肿瘤细胞更为宽容、易于利用的观点一致。
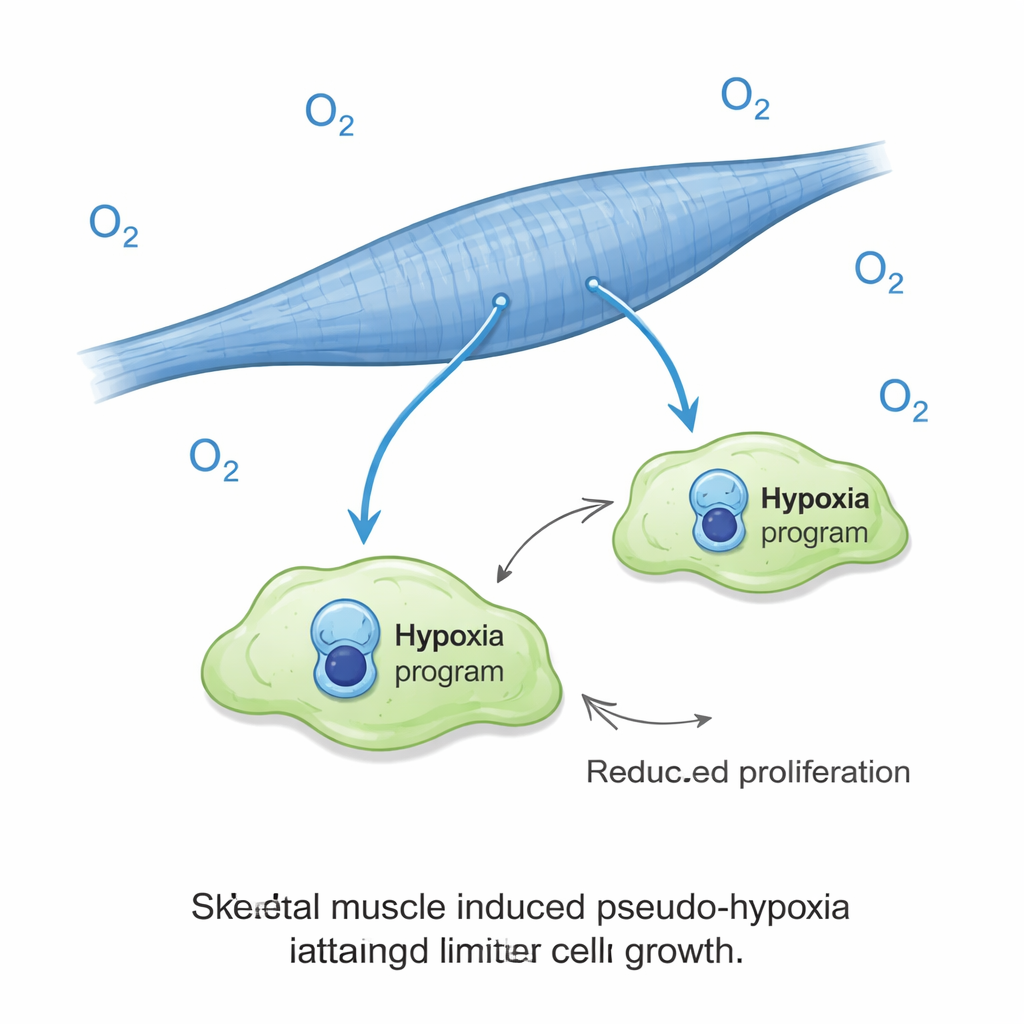
缺氧信号的一个令人意外的角色
一个最显著的发现是,尽管在正常氧气条件下培养,位于肌肉纤维上的癌细胞仍开启了类缺氧的基因签名。在大多数肿瘤中,缺氧通常是一个不良指标,常与侵袭性行为和不良预后相关。但在这里,缺氧相关的状态却与相反的结果相关:生长受抑。研究人员随后将培养物暴露于真正的低氧条件,发现这几乎消灭了肌肉上癌细胞的扩展,而在类肺培养中则实际上促进了癌细胞生长。换言之,同样的信号在通常有利于肿瘤生长时,在肌肉环境中却变成了制动器。这一氧气效应似乎不能简单用培养基中乳酸、酸度或糖类供应的变化来解释。
不只是分泌因子
团队还检验了肌肉细胞释放的可溶性物质是否足以解释其保护作用。额外添加乳酸、改变酸度、调整葡萄糖水平或将癌细胞置于先前接触过肌肉细胞的条件培养基中,都无法复现直接接触共培养中观察到的强烈抑制效果。这表明紧密的物理接触或非常短程的细胞表面信号,对肌肉细胞将癌细胞推入低增殖、可能休眠状态至关重要。有趣的是,肌肉细胞自身在面对癌细胞时其基因活动相对稳定,而肺细胞更容易被重编程,凸显肌肉作为一种稳健的“转移抵抗”组织的特征。
对患者与治疗的意义
总体而言,这项研究揭示了骨骼肌充当一种不友好栖息地,迫使癌细胞进入一种类缺氧、低增殖模式,即使在氧气充足的情况下也如此。这有助于解释为什么肌肉是罕见的转移部位。研究还为药物开发提供了警示:旨在全身阻断缺氧信号的疗法可能无意中削弱这种基于肌肉的天然防御,使癌细胞更容易在原本不易定植的部位生长。理解并保护,甚至模拟,肌肉组织的这些保护特性,可能为预防或控制转移性疾病开辟新的途径。
引用: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
关键词: 癌症转移, 骨骼肌, 缺氧, 肿瘤微环境, 癌症休眠