Clear Sky Science · zh
由FABP4介导的脂肪酸摄取通过脂质过氧化在富脂肪细胞的卵巢癌微环境中促进CD8+T细胞衰老的形成
为何脂肪与免疫细胞在卵巢癌中重要
卵巢癌常向腹腔播散,在那里会遇到大量脂肪沉积。这个富脂环境并非被动背景——它积极影响免疫细胞的行为。尤其是,它能削弱本应攻击肿瘤的CD8“杀伤”T细胞。本研究探讨了来自脂肪的物质如何将这些T细胞推向衰老和功能耗损的状态,以及阻断一种关键脂肪转运蛋白是否能帮助恢复它们的抗癌能力。
使免疫卫士提前衰老的富脂周围环境
临床上长期观察到,许多晚期卵巢癌患者出现腹腔积液,且肿瘤常位于称为网膜的富脂组织中。通过分析患者的单细胞RNA数据并在显微镜下检查肿瘤样本,研究者发现靠近这些脂肪沉积的CD8 T细胞更可能表现出细胞衰老的特征。这些“衰老”T细胞积累色素废物、停止增殖,并产生炎性信号而不是杀伤癌细胞。在人样本和小鼠模型中,取自富脂和含液肿瘤区域的CD8 T细胞明显比淋巴结或脾脏中的更具衰老表型,将富含脂肪的肿瘤微环境直接与T细胞衰老联系起来。
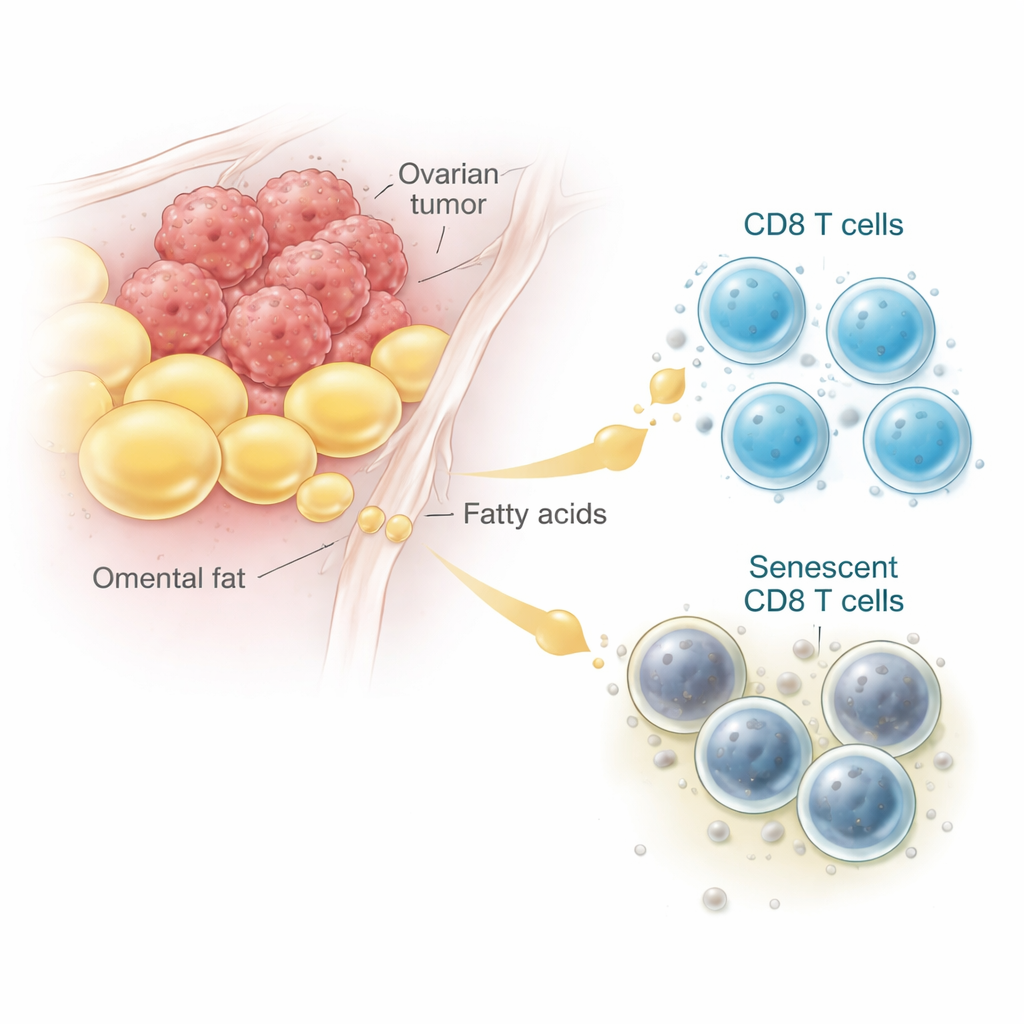
常见脂肪酸如何将有用燃料变成有害物质
为弄清脂肪对T细胞的作用,研究团队在体外重建了肿瘤环境。他们将卵巢癌细胞与小鼠CD8 T细胞共培养,然后加入来自脂肪组织的提取物或一种称为油酸的特定脂肪酸——油酸在卵巢癌腹水中含量丰富。在中到高剂量下,油酸使更多CD8 T细胞进入衰老,但这一效应仅在存在肿瘤细胞时出现。T细胞并未将摄入的脂肪作为能量燃烧,而是积累起发生化学损伤的脂质,这一过程称为脂质过氧化。基因和脂质分析显示氧化脂质和应激标志物增加,而来自脂肪的能量产出保持不变。简言之,在肿瘤存在的情况下,本应作为燃料的脂肪被转向产生损伤的反应,从而加速并削弱T细胞。
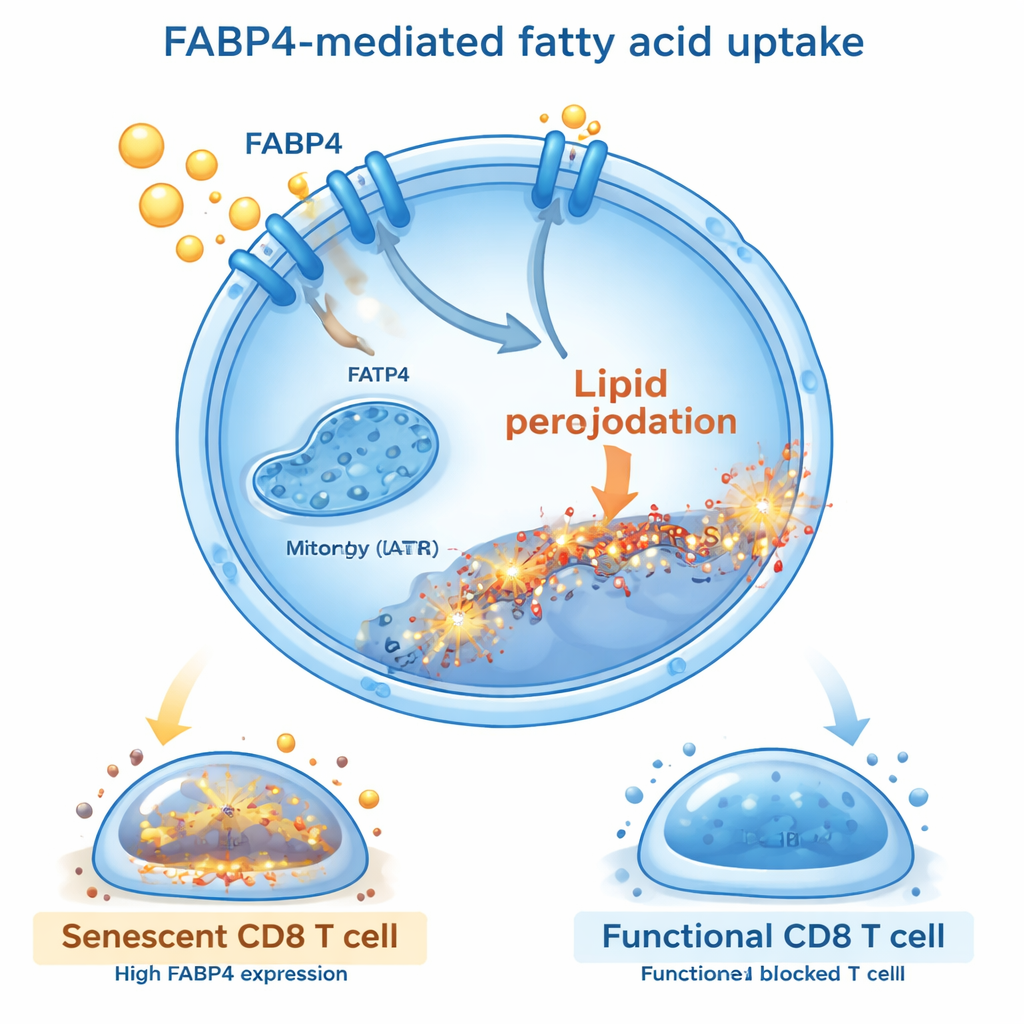
脂肪转运蛋白FABP4作为关键看门人
进一步探究中,研究者寻找控制这一有害脂肪流入的分子。他们发现,在暴露于脂肪提取物或油酸的CD8 T细胞中,名为FABP4的转运蛋白被强烈诱导表达。FABP4像一辆穿梭车,将长链脂肪酸携带进细胞。当用小分子抑制剂(BMS309403)或基因沉默方法阻断FABP4时,T细胞摄脂减少,脂质过氧化降低,衰老倾向也随之下降。受保护的T细胞增殖更好,产生更多干扰素-γ和颗粒酶B等杀癌分子,同时释放较少的抑制性和炎性信号。恢复FABP4表达会逆转这些益处,证实该转运蛋白是连接脂肪摄取与T细胞衰老的核心开关。
从小鼠实验到潜在治疗策略
研究团队随后在腹腔内扩散的卵巢癌小鼠体内测试了FABP4抑制。给予FABP4抑制剂的老鼠,其腹水中提取的CD8 T细胞脂肪摄取与脂质损伤减少,衰老T细胞比例降低,关键效应分子水平上升。当FABP4抑制剂与常规化疗联合使用时,老鼠的可见肿瘤结节更少,脾脏、淋巴结和腹水中的T细胞应答更强,且存活期延长,优于单用化疗的对照组。这些发现表明,通过靶向脂肪代谢可以通过恢复免疫系统前线效应细胞来增强现有治疗的效果。
这对患者意味着什么
对非专业读者而言,结论是:在卵巢癌中,不仅肿瘤本身重要,其所处的富脂“邻里”也影响病情。来自脂肪的分子,特别是某些脂肪酸,能使杀伤性T细胞过早衰老,剥夺它们攻击癌细胞的能力。本研究指出脂肪转运蛋白FABP4是该过程中的关键罪魁。阻断FABP4(至少在小鼠中)能够减少T细胞衰老、恢复其杀伤功能并提高化疗效果。尽管在将其作为患者治疗手段之前仍需更多研究,这项工作为一种新方向铺路:不仅治疗癌细胞本身,还要处理其微环境中的代谢陷阱以防止免疫系统被削弱。
引用: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
关键词: 卵巢癌, T细胞衰老, 脂肪酸代谢, 肿瘤微环境, FABP4