Clear Sky Science · zh
一种新型K6-K14角蛋白融合诱导的细胞骨架重塑通过cGAS-STING选择促进癌性干性与细胞可塑性
会变形的癌细胞如何智胜其周围环境
癌细胞不仅不受控地增殖;它们还学会弯曲和重塑自身的“内骨架”以求生存、隐匿和扩散。本研究揭示了头颈部癌细胞内一种特定结构异常如何破坏细胞核、触发内在的危险报警、将细胞推入休眠状态,并最终帮助它们以更具侵袭性、类似干细胞的表型卷土重来。理解这一路径中由机械作用驱动的癌症演化,可能为阻断复发与转移开辟新途径。
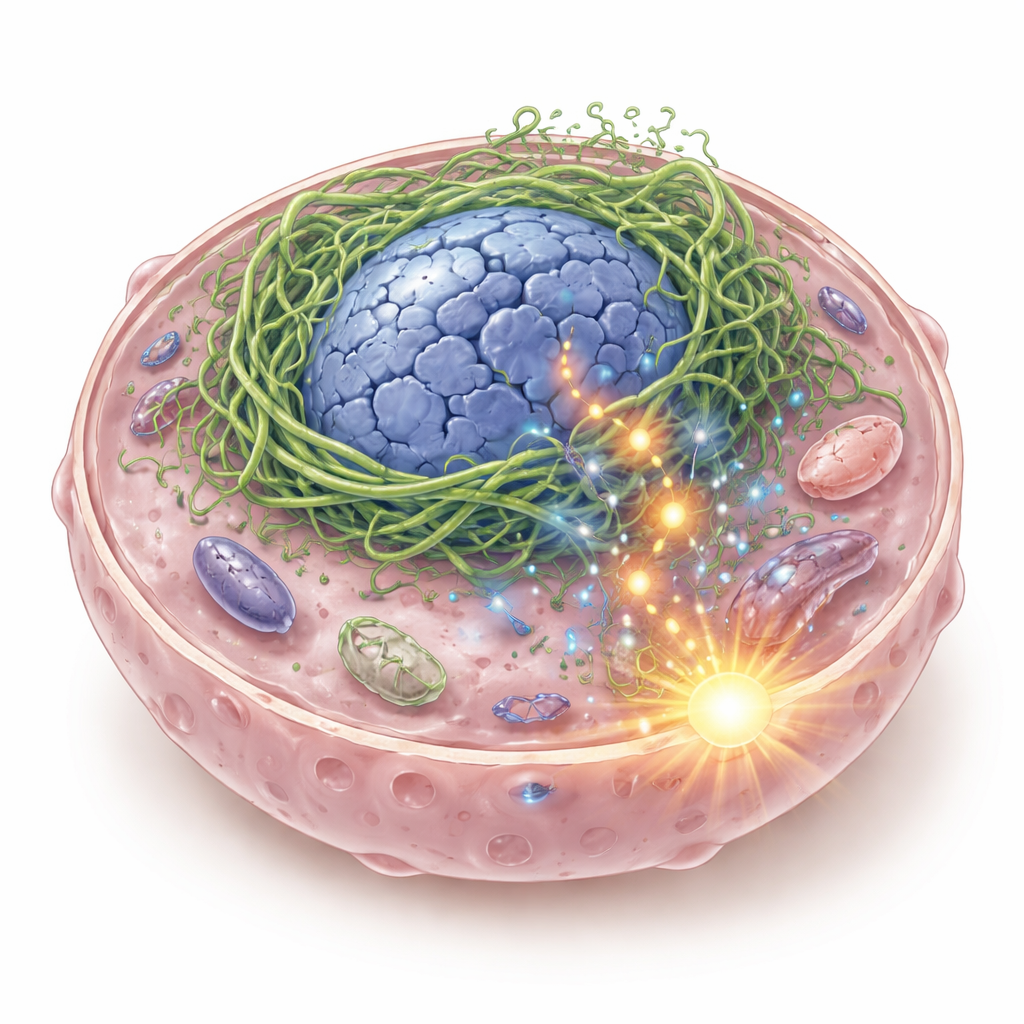
破裂的内部支架及其危险后果
每个细胞内部都有由蛋白丝构成的柔性支架,维持细胞与细胞核形态并帮助感知物理力。作者聚焦于角蛋白——一类在上皮组织(包括口腔和咽喉表面)中常见的支架蛋白。在某些头颈部鳞状细胞癌中,他们发现了一种混合角蛋白K6-K14/V5,它由两个角蛋白基因融合生成。当这种融合蛋白在癌细胞中表达时,它不会形成平滑的支持网络,而是紧密地在细胞核周围凝聚,将细胞核扭曲成空洞样、畸形的结构并导致DNA断裂。DNA片段泄漏到细胞质中,被一种称为cGAS–STING的免疫感应系统检测到,该系统通常在识别病毒DNA时发出警报。
从细胞死亡的压力到隐秘的存活
这种核损伤的直接影响对癌细胞是有害的:它们增殖减慢,许多细胞死亡。然而,仍有一部分细胞设法存活下来。这些幸存者强烈受其物理环境影响。在标准的平板培养皿上它们逐渐消失,但当在更接近真实组织质地的软胶原凝胶中培养时,它们得以存活并重新出现为一种新的群体,称为3D-V5细胞。基因表达分析显示,这些细胞对持续的DNA损伤警报作出反应,通过启动自噬这一自我清理程序来回收受损部件,尤其是有缺陷的线粒体。该应答帮助它们进入一种低活性、休眠状态,使其能在应激中存活而非被清除。
休眠细胞重编程并准备迁移
在休眠期间,这些幸存细胞悄然重写其内部程序。它们改变角蛋白的组合,进入一种“部分”上皮—间充质转化(pEMT)状态——一种保留部分上皮特征同时获得柔性与运动性的中间身份。它们在形成球体和播种新细胞簇方面的能力大幅提升,这是癌性干性的一个标志。随着时间推移,它们的力学特性恢复:再次使细胞核变得更坚固,重建强大的肌动蛋白纤维,并生成长的突出物以探测并抓握周围基质。它们还上调称为基质金属蛋白酶(MMPs)的酶,这些酶分解细胞外基质,为侵袭打开通道。
与邻近细胞对话以构建支持性生态位
这些重编程的癌细胞并非单打独斗。研究团队观察到3D-V5细胞向周围释放大量称为细胞外囊泡的小包。当这些囊泡作用于邻近的口腔成纤维细胞——一种结缔组织细胞时,成纤维细胞自身的基因表达发生改变,变得更像支持肿瘤生长的癌相关成纤维细胞。许多交换的信号围绕FGF–FGFR轴,这是一组已知驱动细胞增殖、可塑性和抗性的生长因子及其受体。在体外培养和小鼠肿瘤中,阻断FGFR活性能减弱这种生长优势。在动物体内,由3D-V5细胞形成的肿瘤分化差、侵袭性更强、富含干细胞标志物且更容易在注射部位之外扩散。
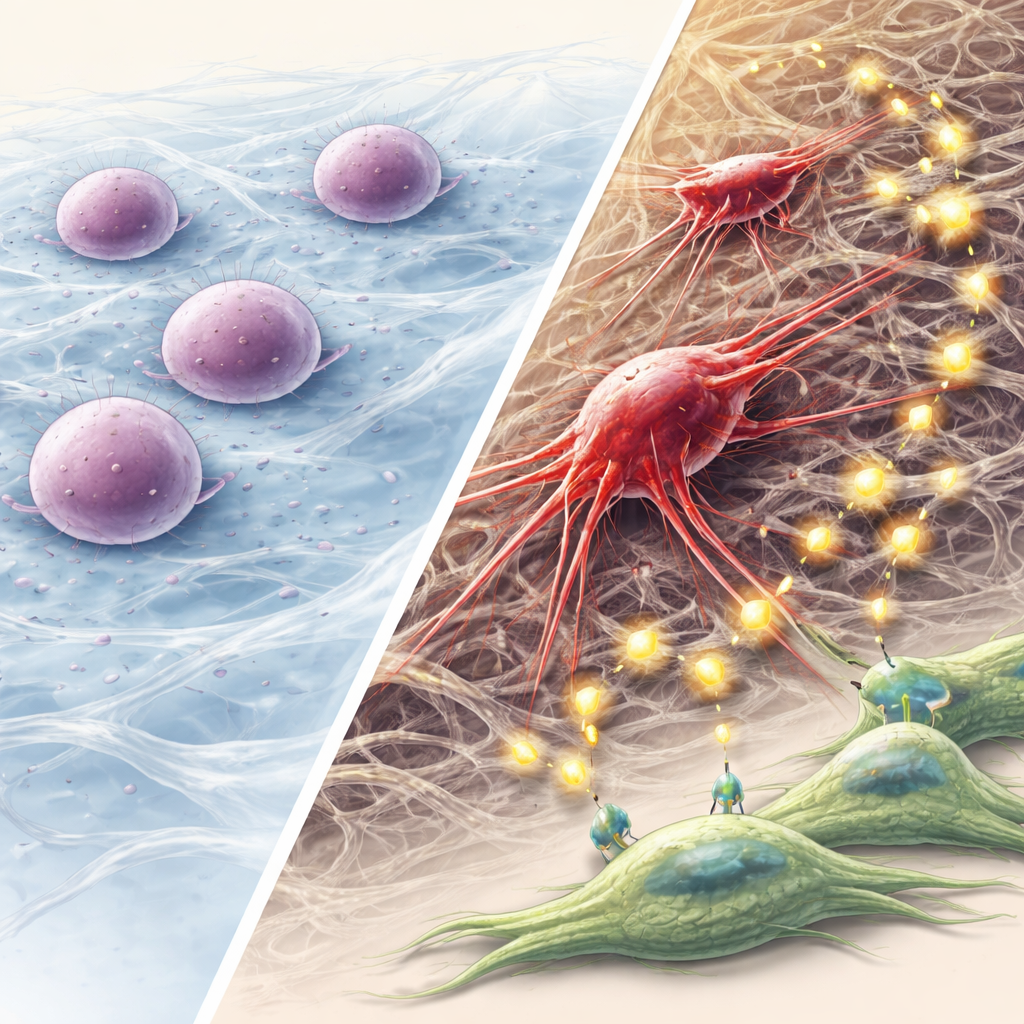
为何这条通向侵袭性癌症的机械通路重要
这项工作提出了一个逐步模型:角蛋白融合破坏细胞内部支架,压迫细胞核并触发DNA损伤警报;自噬随后允许少数细胞进入休眠而非死亡;随着时间推移,幸存者重组其骨架,获得干样与侵袭性特质,并通过囊泡与FGF信号重塑其周围环境。对非专业读者而言,关键信息是:细胞内的物理力与结构蛋白,在驱动癌症演化方面可以与基因和化学因素同样重要。针对这一机械应激—自噬—FGF通路,特别是在存在角蛋白融合的头颈癌中,可能为防止休眠肿瘤细胞重新激活与扩散提供新的策略。
引用: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
关键词: 癌性干性, 细胞骨架, 肿瘤休眠, 头颈部癌症, 机械传导