Clear Sky Science · zh
通过调控 SRXN1,组蛋白去甲基化酶 PHF2 在肝细胞癌中作为抑癌因子的作用
为何这项肝癌研究重要
肝癌是全球最致命的癌症之一,现有药物对许多患者仅能适度延长生存期。本研究提出了一个不同的问题:与其直接靶向常见的致癌基因,是否可以利用肝细胞内 DNA 的包装与化学标记方式寻找新的、更精确的治疗选择?研究人员聚焦于一种鲜为人知的蛋白 PHF2,并揭示了它如何可能帮助阻止肝细胞转化为癌细胞。
在癌症控制系统中寻找薄弱环节
癌症并非仅由基因突变驱动;错误的“表观遗传”控制——那些决定基因何时被打开或关闭的化学标记和蛋白复合体——也会助长癌症。在肝细胞癌(最常见的肝癌类型)中,许多此类调控因子受到扰动。研究团队在六种肝癌细胞系中系统地测试了497种表观遗传调控因子,使用 RNA 工具逐一暂时降低每种因子的表达,然后测量癌细胞的存活能力。这个大规模筛查旨在揭示癌细胞生长依赖的调控因子,以及那些通常对肿瘤形成起制动作用的因子。
发现新的促癌与保护因子
筛查结果揭示了两大类:可能的癌症“加速器”(致癌基因),其丧失会损害癌细胞存活;以及可能的“刹车”(肿瘤抑制子),其丧失会使癌细胞生长更好。通过将实验室数据与大型公开患者数据集结合,研究人员将候选名单缩小到一些与临床相关的因子。两个调控因子 SUPT7L 和 SMARCC1 在肿瘤中常表现为更高活性,并与较差生存相关。相反,调控因子 PHF2 在肝肿瘤中常常表达较低,且肿瘤中保持较高 PHF2 水平的患者通常存活更久。这些模式提示 PHF2 可能在人类肝癌中发挥抑癌作用。
失去 PHF2 后肝癌细胞发生的变化
为更深入测试 PHF2,研究团队工程改造肝癌细胞使其持续表达较少该蛋白,并随时间追踪其行为。PHF2 降低的细胞生长更快,并显示更高水平的 Ki-67(一种活跃细胞分裂的标志),表明 PHF2 通常有助于抑制增殖。这些效应在已经具有侵袭性的肝癌细胞系中最为明显,暗示单纯丧失 PHF2 可能不足以单独引发癌症,但在肿瘤形成后可加速恶性细胞的生长。
与细胞应激防御的意外关联
随后,研究人员使用现代蛋白质组学方法列出在 PHF2 降低时发生变化的数千种蛋白。众多细微变化中,一个模式格外突出:一种名为 SRXN1 的应激保护蛋白在 PHF2 丧失时持续下降。SRXN1 帮助细胞管理活性氧类——这些化学活性副产物既能损伤 DNA 和蛋白质,也能促使癌细胞发生适应。数据表明 PHF2 有助于维持 SRXN1 水平,改变这一平衡可能影响肝癌细胞对内部应激的应答,并最终影响其生长速度。
在已知应激通路之外发挥作用
SRXN1 通常受一个主控应激响应开关 Nrf2 调控,Nrf2 在细胞面临氧化应激时会开启许多抗氧化基因。鉴于 PHF2 被抑制时 SRXN1 下调,团队探讨 PHF2 是否仅通过已知的 Nrf2 通路发挥作用。他们检查了关键的 Nrf2 相关基因和蛋白,使用能通过抑制其抑制因子 Keap1 来激活 Nrf2 的药物,并用遗传工具直接降低 Keap1。跨越这些测试,缺失 PHF2 的细胞反应与正常细胞相似,且更广泛的通路与转录因子分析并未将 Nrf2 突出为主要参与者。相反,其他因子包括先前与肝癌相关的 ZNF384 和 Nrf1 成为候选。综合证据表明,PHF2 对 SRXN1 和抗氧化反应的调控可能绕过经典的 Nrf2 信号通路,暗示这些肿瘤存在一条不同的应激调控途径。
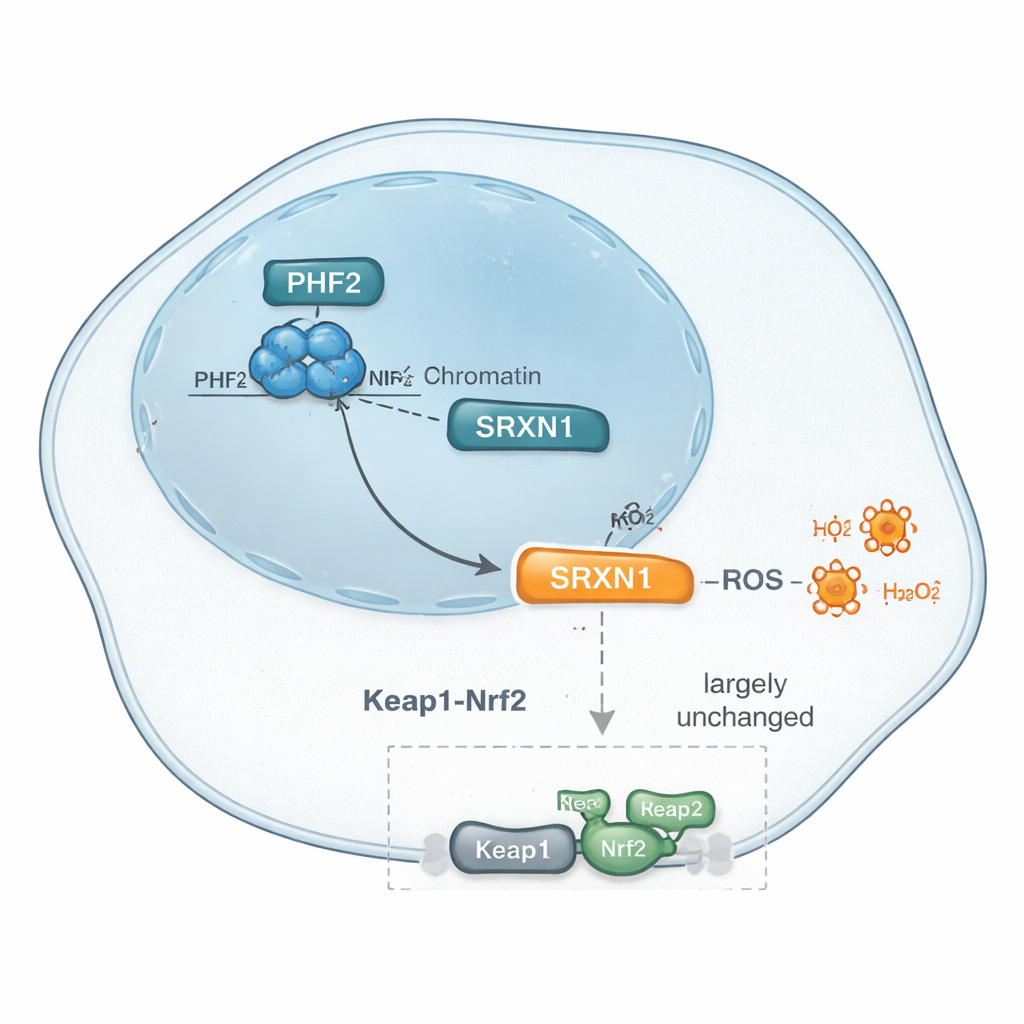
这对未来治疗可能意味着什么
对非专业读者来说,关键结论是:这项研究确认 PHF2 是肝癌中的一个有前景的保护因子——当 PHF2 存在且活跃时,肿瘤细胞生长更慢;当其减少时,细胞获得生长优势并改变其处理细胞应激的方式。由于 PHF2 本身可能难以通过传统小分子药物直接抑制或激活,作者提出了诸如基于 RNA 的疗法或通过上游信号伙伴增强 PHF2 活性的药物等新兴策略。他们还强调 PHF2 的效应具有情境依赖性——其影响可能随诸如 p53 状态等其他突变而变化——因此任何未来治疗很可能需要谨慎的患者筛选。总体而言,这项工作细化了我们对表观遗传调控因子如何塑造肝癌行为的理解,并为设计恢复或模拟 PHF2 抑癌作用的治疗开辟了新途径。
引用: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
关键词: 肝细胞癌, 表观遗传调控, PHF2, SRXN1, 肝癌治疗