Clear Sky Science · zh
通过自分泌–旁分泌信号,Rab37介导的OPN分泌富集SPP1+巨噬细胞以驱动肺肿瘤进展
免疫细胞如何悄悄助长肺肿瘤生长
肺癌并非孤立发生。它在一个充斥着免疫细胞和结缔组织的繁忙“邻里”中生长,有时会将本应防御的细胞变成帮凶。本研究揭示了一种位于免疫细胞内的小型运输蛋白Rab37,如何促使特定巨噬细胞分泌一种称为骨桥蛋白(OPN)的分子,从而营造有利于肿瘤的环境,使肺癌更具侵袭性并更难治疗。
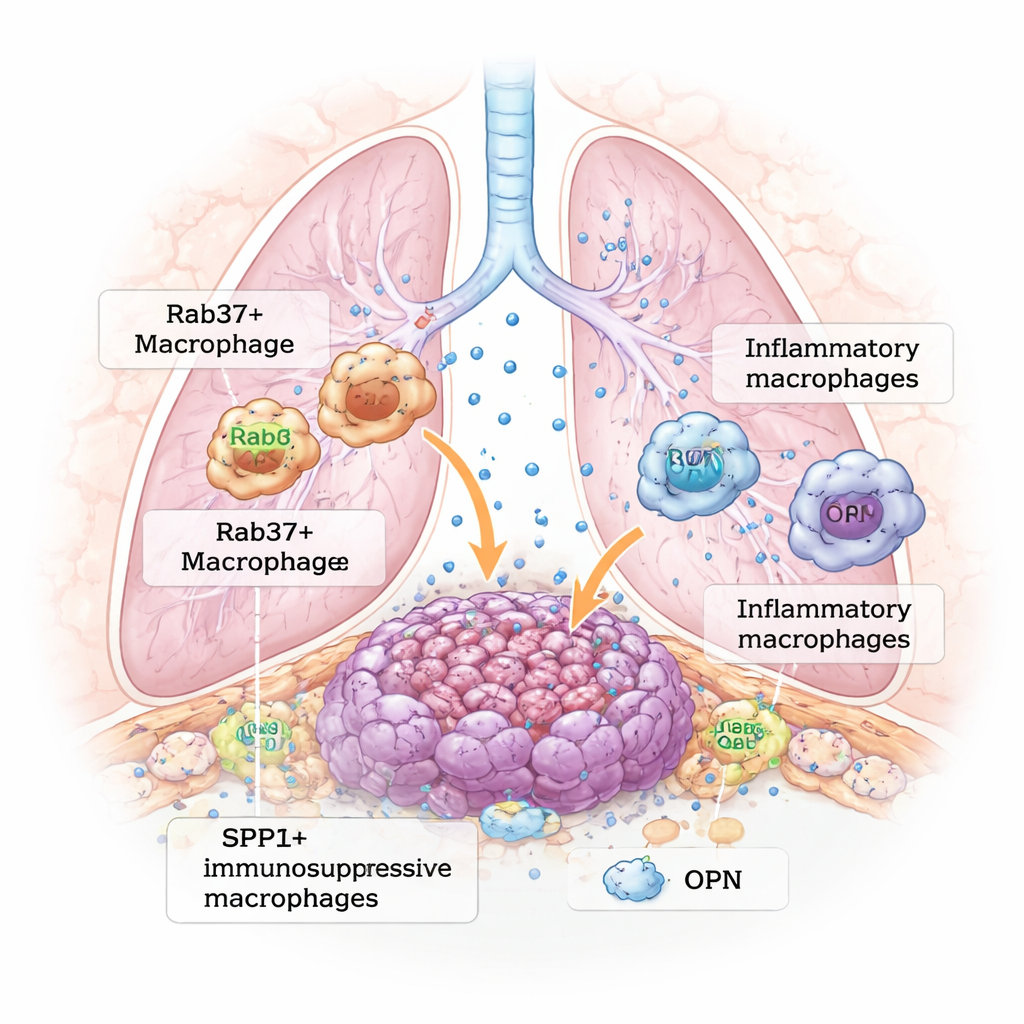
肺肿瘤内部的繁忙“邻里”
现代癌症研究表明,肿瘤更像是复杂生态系统,而非简单的异常细胞团。在肺肿瘤周围,免疫细胞、血管和支持细胞不断互相发送化学信号。其中,巨噬细胞——通常负责清除感染和碎屑的免疫细胞——常常以“肿瘤相关巨噬细胞”(TAMs)的形式定居于肿瘤内。许多情况下,这些细胞并非攻击癌细胞,而是转向支持性角色,抑制免疫反应并帮助肿瘤生长与扩散。本论文关注的核心问题是:是什么促使巨噬细胞转变为这种有害的、助长肿瘤的状态?
两类巨噬细胞:帮手与对抗者
研究者使用单细胞RNA测序技术,这种技术能读取单个细胞中数千个基因的表达情况,绘制小鼠肺肿瘤内免疫细胞的图谱。他们比较了正常小鼠与缺失Rab37的小鼠。来自正常小鼠的肿瘤中,发现大量富含SPP1基因的巨噬细胞,该基因编码骨桥蛋白(OPN)。这些SPP1+巨噬细胞表现出免疫抑制和助肿瘤的特性。相反,来自Rab37基因敲除小鼠的肿瘤中,SPP1+巨噬细胞更少,而表达另一基因THBS1的巨噬细胞更多,后者与更具炎性、可能抑制肿瘤的反应相关。在人类肺癌样本中,肿瘤内富含CD163、Rab37和OPN阳性巨噬细胞的患者更容易复发且生存更差,提示这种特定的巨噬细胞类型在临床上具有危险性。
增强OPN分泌的秘密运输蛋白
Rab37属于一类控制细胞如何打包并释放分子的蛋白家族。研究团队证明,Rab37将OPN装入巨噬细胞内的小囊泡,并驱动其释放到细胞外。当巨噬细胞具备功能性Rab37时,它们分泌的OPN显著增加,尤其在暴露于肺癌细胞发出的信号时。移除Rab37或阻断其活性会导致OPN释放显著下降。研究还发现了一个反馈回路:分泌出的OPN在巨噬细胞内激活一种名为STAT3的信号蛋白,继而增强SPP1基因的活性并推动巨噬细胞进一步偏向类似M2的促肿瘤状态。该回路使细胞维持在促肿瘤的身份,不断输出更多OPN。
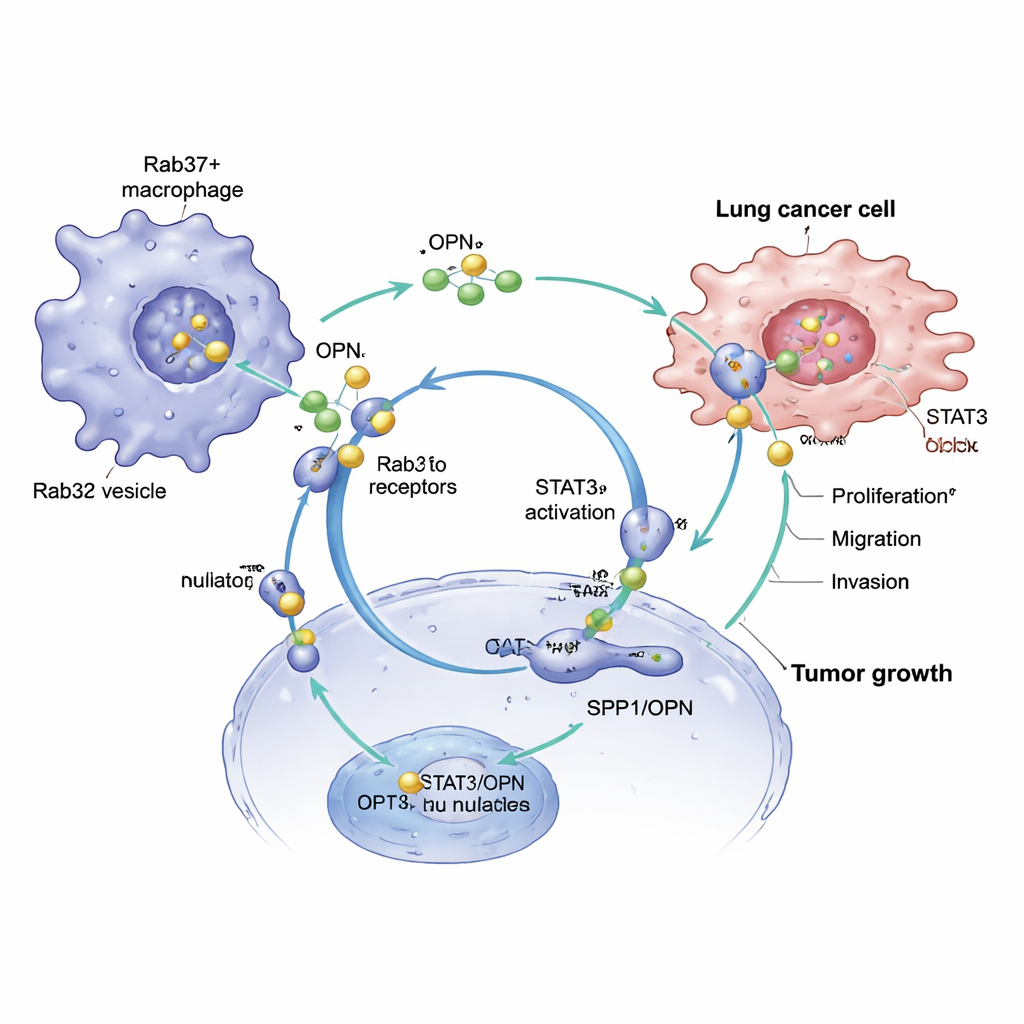
从免疫信号到更快速生长的肿瘤
OPN不仅作用于巨噬细胞——它也直接与癌细胞对话。当肺癌细胞被置于来自Rab37阳性巨噬细胞的培养上清液中时,它们生长更快、迁移性和侵袭性增强。阻断该上清液中的OPN会减弱这些效应,而补回纯化的OPN则能恢复这些效应。同样的Rab37–OPN–STAT3回路在重编程巨噬细胞的同时,也在肺癌细胞内部激活促进生长与存活的通路,鼓励增殖、移动并侵入周围组织。由此,一个单一的分泌分子既能重塑免疫行为,也能加速肿瘤进展。
将发现转化为治疗机会
对非专业读者来说,主要信息是:肿瘤内部的一些免疫细胞变成了“内应”,而Rab37是驱动这种叛变的重要协调者。通过帮助巨噬细胞分泌OPN并维持OPN驱动的反馈回路,Rab37促成了一个安静、耐受的环境,使肿瘤得以繁荣并扩散。肿瘤中富含Rab37+/OPN+巨噬细胞的患者预后较差,这意味着这种细胞类型既可作为危险信号,也可作为治疗靶点。阻断OPN、干扰STAT3或破坏Rab37的运输功能的疗法,可能有助于将巨噬细胞重新导向抗肿瘤角色,使肺癌对现有治疗(包括免疫治疗)更为敏感。
引用: Yang, YE., Lin, YA., Ling, LL. et al. Rab37-mediated OPN secretion enriches SPP1+ macrophages through autocrine–paracrine signaling to drive lung tumor progression. Oncogenesis 15, 4 (2026). https://doi.org/10.1038/s41389-026-00596-3
关键词: 肺癌, 肿瘤微环境, 巨噬细胞, 骨桥蛋白(osteopontin), STAT3信号通路