Clear Sky Science · zh
TRIM21介导的HILPDA降解通过限制PD-L1棕榈酰化克服乳腺癌对抗PD-1免疫疗法的耐药性
为什么某些癌症免疫疗法会失效
能够释放免疫系统的药物,如抗–PD‑1疗法,已经改变了包括侵袭性乳腺癌在内的多种癌症的治疗格局。然而,许多肿瘤要么从未响应,要么最终找到逃逸途径。本研究深入探讨了三阴性乳腺癌中这样一种逃逸机制,并展示了通过重塑肿瘤脂质代谢——以及一种已被重新定位的药物非诺替尼——如何在标准免疫疗法失效时重新打开免疫系统的作用之门。 
一种隐藏的帮手为肿瘤撑起保护伞
研究者把注意力集中在一种鲜为人知的蛋白HILPDA上,该蛋白此前与细胞在应激下处理脂质的方式有关。通过比较对抗‑PD‑1疗法仍敏感的小鼠乳腺肿瘤与已产生耐药性的肿瘤,他们发现耐药肿瘤中HILPDA的水平明显更高。对大型患者数据库和妇女乳腺肿瘤样本的分析也证实,肿瘤组织中HILPDA含量高于正常乳腺组织,尤其在三阴性乳腺癌中更为显著,而且肿瘤中HILPDA表达较高的患者预后往往更差。对来自未从PD‑1阻断药物获益的患者的肿瘤样本也发现HILPDA含量更高,将该蛋白直接与治疗失败联系起来。
肿瘤如何扭转免疫环境对抗我们
为了了解HILPDA在肿瘤内部的实际作用,研究团队构建了过表达或缺失该蛋白的乳腺癌细胞,并在与人类免疫细胞共培养或在小鼠体内生长时进行观察。当HILPDA含量升高时,肿瘤招募了更多调节性T细胞、骨髓来源抑制细胞和类似M2的巨噬细胞——这些免疫细胞类型会抑制免疫攻击并帮助癌细胞隐匿。与此同时,杀伤性CD8 T细胞和自然杀伤细胞的数量与活性下降,它们释放毒性分子和炎性信号的能力也被削弱。沉默HILPDA则改变了这一局面:肿瘤中抑制性细胞减少,活跃的杀伤细胞增多,肿瘤生长减慢、转移减少。关键的是,当低HILPDA肿瘤的小鼠接受抗‑PD‑1治疗时,肿瘤缩小更多,小鼠存活时间更长,表明HILPDA决定了免疫疗法的疗效。
脂质合成、分子盔甲与免疫逃逸
更深入的研究揭示了HILPDA如何重塑肿瘤代谢以强化免疫防线。在癌细胞内,HILPDA与分子伴侣蛋白HSP90结合以稳定转录因子KLF5,后者驱动脂质生成。这组三联体促进脂肪酸合成,尤其是棕榈酸的生成,并使肿瘤细胞充满脂滴。随后其中一种脂肪被连接到PD‑L1上——PD‑L1是位于肿瘤表面的检查点蛋白,会向免疫细胞发出“不要攻击”的信号。研究团队表明,将棕榈酸附着到PD‑L1的特定位点就像分子胶水:它帮助PD‑L1稳定地定位在细胞膜上并防止其被降解。突变这个单一附着位点会剥夺PD‑L1的稳定性并削弱其保护癌细胞的能力,即便在HILPDA丰富时亦然。换言之,HILPDA驱动的脂质生成为PD‑L1提供了一种化学修饰,使肿瘤的免疫保护从脆弱变为坚固。
可被推动的内在刹车
每个加速器都需要刹车,这里的刹车是另一种名为TRIM21的蛋白。作者发现TRIM21能识别HILPDA并给它打上分子“标签”,将其送往细胞的降解机制。在患者的乳腺肿瘤中,当HILPDA含量高时TRIM21往往较低,且低TRIM21与差的预后相关,这表明这一天然刹车系统在肿瘤中常被削弱。随后团队寻找可以强化TRIM21的药物,鉴定出已在人类中测试过的维甲酸类药物非诺替尼。在三阴性乳腺癌的细胞和动物模型中,非诺替尼增强了TRIM21的活性,加速了HILPDA的降解,减少了脂质合成和PD‑L1的保护性修饰,并减缓了肿瘤的生长与扩散。最引人注目的是,将非诺替尼与抗‑PD‑1疗法联合使用使肿瘤更容易受到免疫攻击,肿瘤微环境中的杀伤性T细胞和自然杀伤细胞增加,而抑制性细胞减少。 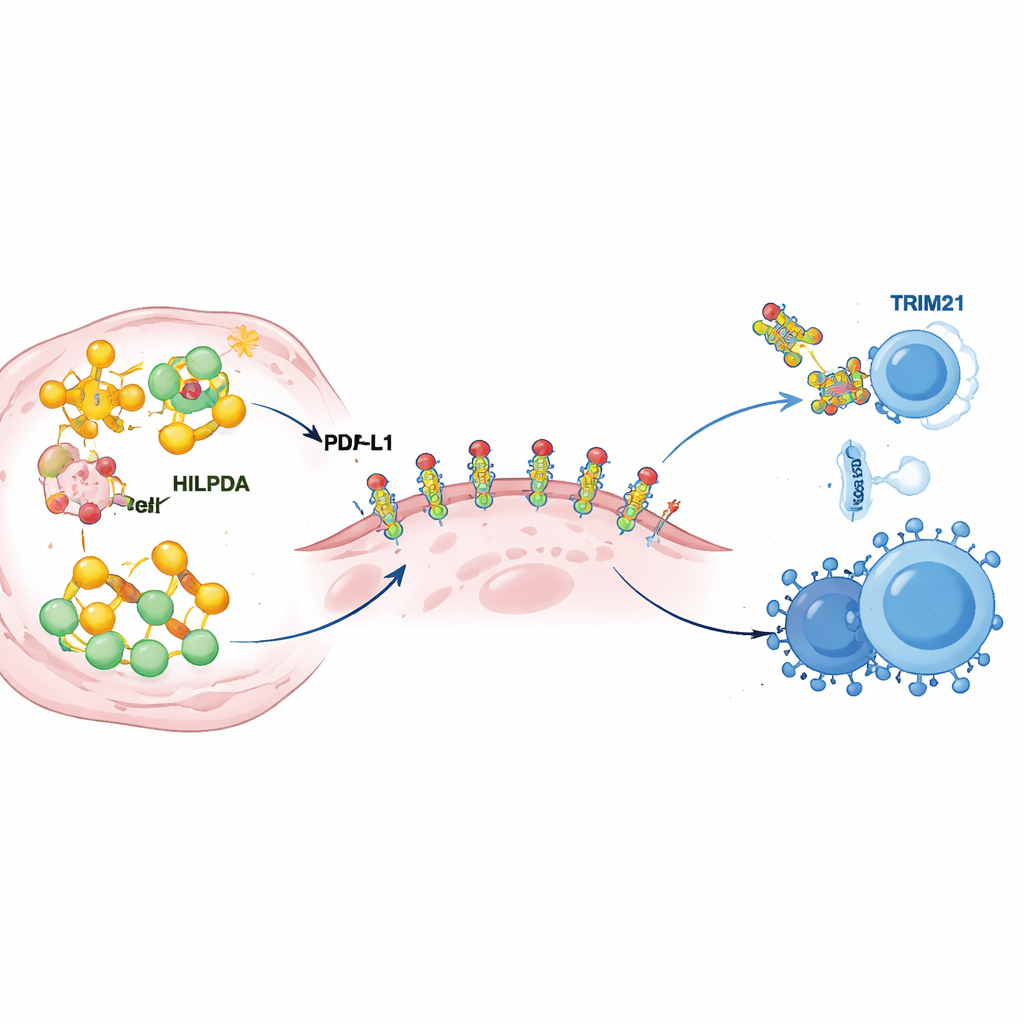
这对未来癌症治疗意味着什么
这项工作揭示了一条事件链:受压的乳腺癌细胞上调HILPDA,增加脂质合成,并在其表面的PD‑L1上进行化学加固,使它们即使在面对PD‑1阻断药物时也能持续抑制免疫细胞。TRIM21作为一种内生的保护机制可以瓦解HILPDA,但在肿瘤中常常太弱。研究发现非诺替尼能够重新激活这一保护机制,表明将代谢类药物与现有免疫疗法联合使用可能是克服耐药的切实策略。如果在临床试验中得到验证,针对TRIM21–HILPDA–PD‑L1轴的干预或能为难治性三阴性乳腺癌患者再次提供从免疫疗法中获益的机会。
引用: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
关键词: 三阴性乳腺癌, 免疫治疗耐药, PD-L1棕榈酰化, 肿瘤脂质代谢, 非诺替尼(fenretinide)