Clear Sky Science · zh
Cereblon (CRBN) 通过负向调控 6-磷葡萄糖酸脱氢酶 (6PGD) 抑制前列腺癌转移
这项研究为何重要
当前列腺癌从前列腺扩散到其他器官时,治疗难度显著增加,常常致命。该研究揭示了一种鲜为人知的细胞“质量控制”蛋白 cereblon(CRBN)如何通过拆除助长侵袭性的代谢酶来阻止前列腺癌扩散。理解这一内在制动机制为减缓或阻止转移提供了新思路,尤其对难治性病变具有潜在意义。
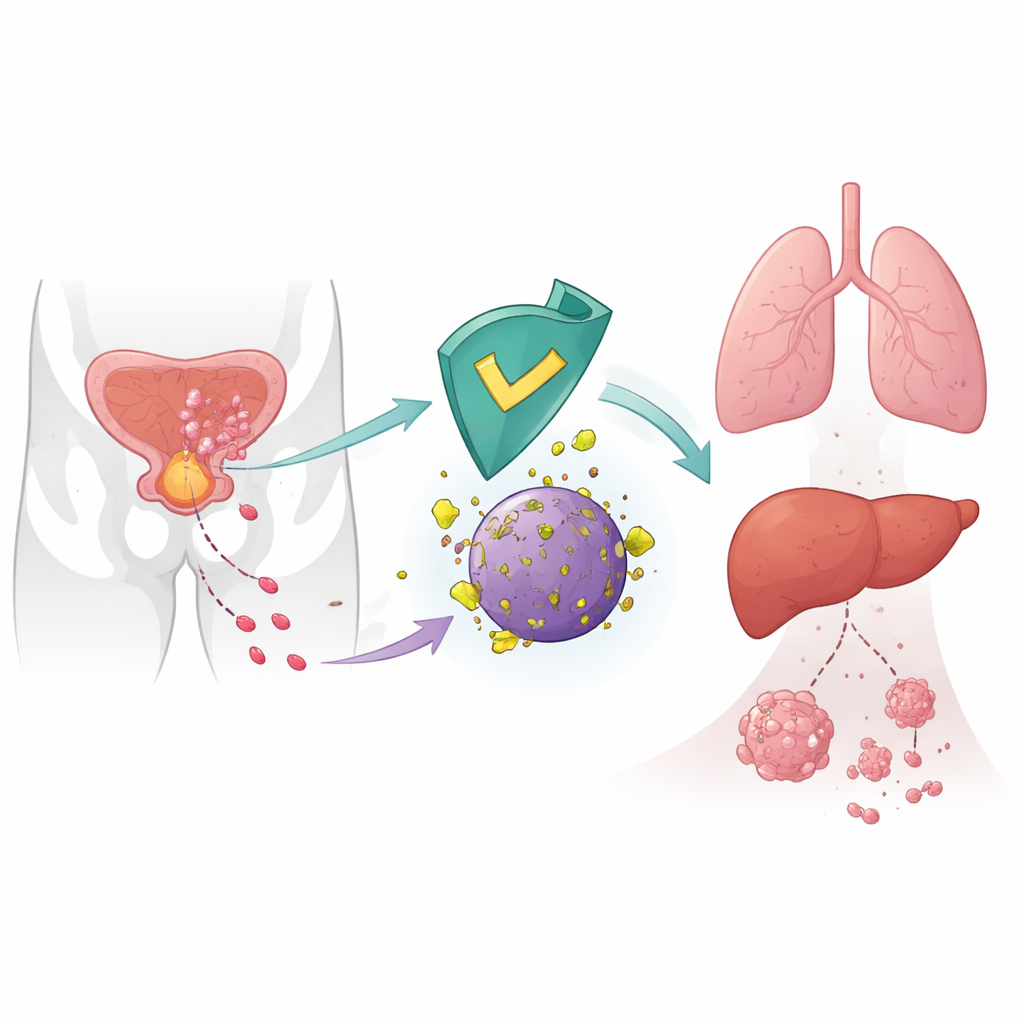
癌症扩散的内部刹车
癌细胞并非随机扩散;它们重编程内部机制以移动、侵入并在远处器官定殖。作者将注意力集中在 CRBN 上——一种以血液肿瘤用药(如沙利度胺)为靶点而闻名的蛋白。在健康细胞中,CRBN 是分子降解装置的一部分,负责标记并驱动特定蛋白被拆除。早期研究提示肿瘤中 CRBN 水平偏低与预后不良相关,但其对转移的直接作用尚不明确。本研究显示,CRBN 可作为抑制前列腺癌转移的天然抑制因子,通过将代谢酶 6-磷葡萄糖酸脱氢酶(6PGD)定向降解来发挥作用。
被癌细胞劫持的代谢引擎
6PGD 位于称为氧化性戊糖磷酸途径的代谢通路中,该通路帮助细胞生成 NADPH——既是合成构件的供体,也是抗氧化能力的来源。许多肿瘤增强该通路以加速生长并耐受应激。研究团队发现,患者的前列腺癌样本通常比正常前列腺组织具有更低的 CRBN 和更高的 6PGD,这种失衡在侵袭性疾病中尤为明显。在前列腺癌细胞系中,敲低 CRBN 或用定制化合物促其降解会导致 6PGD 蛋白水平和酶活性上升,从而提升 NADPH。恢复 CRBN 则产生相反效果,降低 6PGD 和 NADPH,但不改变 6PGD 基因的转录信息,表明这是一个蛋白水平的调控。
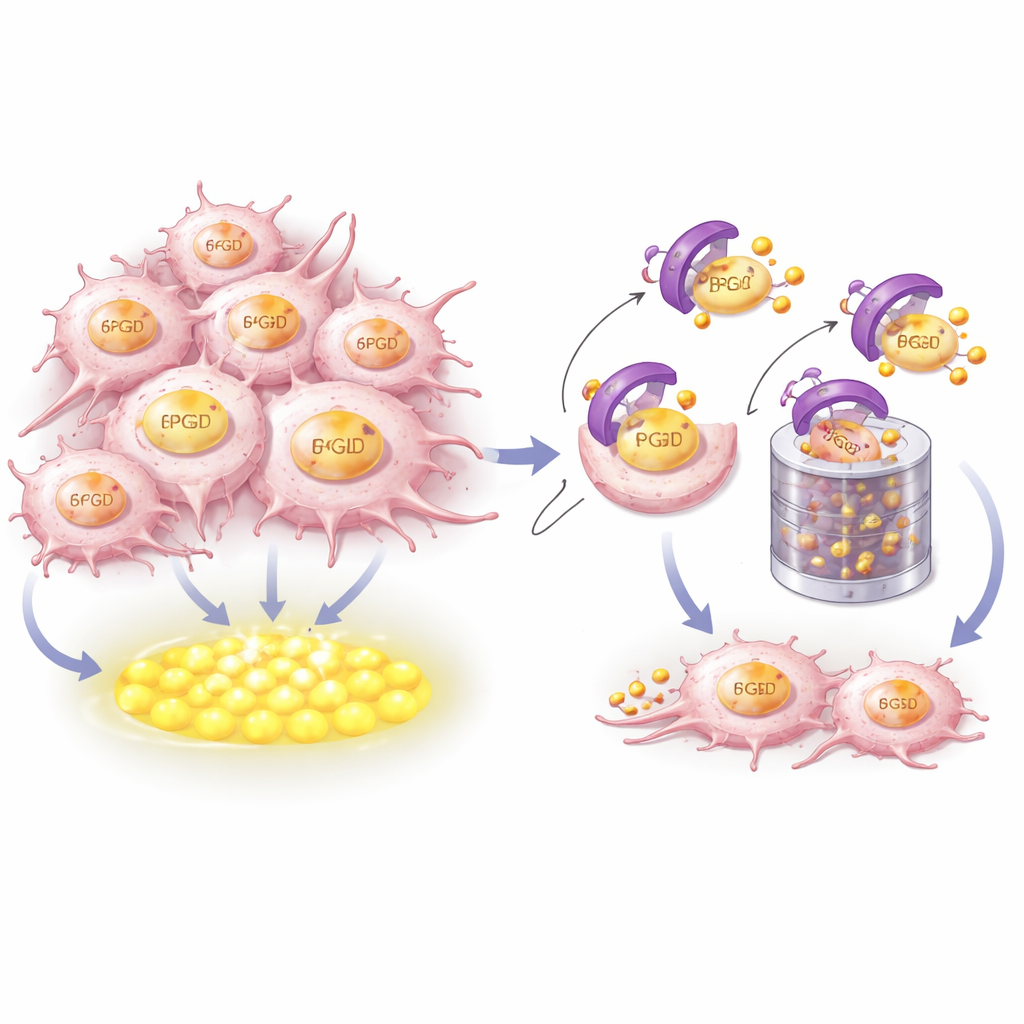
CRBN 如何识别并销毁“燃料”来源
为了解 CRBN 如何控制 6PGD,研究者将结构建模与生化实验结合。他们展示了 CRBN 通过紧密结合 6PGD 尾端附近的一段高度保守的短螺旋片段来直接抓取该酶。两者关键氨基酸形成了契合的对接界面。当这些接触点被改变时,CRBN 无法再与 6PGD 结合、附加标记其降解的小型泛素标签,或将其送往被称为蛋白酶体的细胞“碎纸机”。值得注意的是,这一识别表面与免疫调节药物结合 CRBN 的口袋不同,意味着 CRBN 对 6PGD 的控制属于其本来的家务性功能,而非药物诱导的效应。
从代谢改变到细胞迁移
这种分子握手的后果在细胞行为层面显现出来。在缺乏 CRBN 的前列腺癌细胞中,升高的 6PGD 和 NADPH 与增强的运动性和通过人工屏障的侵袭能力并存,这是转移潜力的标志。当 CRBN 过表达时,细胞的运动和侵袭性降低,尽管其增殖速率未发生改变。基因表达谱分析显示,CRBN 提高了与紧密排列的上皮细胞相关的 CDH1 水平,并降低了与组织降解与迁移相关的 MMP1 水平。重要的是,这些变化依赖于 CRBN 与 6PGD 的直接结合,且可被阻断 6PGD 酶活性的手段逆转,将代谢变化与转移行为的改变联系起来。
来自动物模型与其他癌种的证据
研究团队在小鼠体内检验了这些观点:通过将前列腺癌细胞注入血液或脾脏,带有额外 CRBN 的细胞在肝和肺中形成的转移结节远少于对照细胞,确认了其在活体动物中的抗转移作用。缺失 CRBN 的小鼠在多个器官中表现出更高的 6PGD 蛋白水平。在胶质母细胞瘤、肺癌和肾癌细胞系中也出现了类似模式:去除 CRBN 会增加 6PGD 并促进细胞运动与侵袭,而通过基因干预或药物抑制 6PGD 可以遏制这种侵袭行为。这些观察表明,CRBN–6PGD 对转移的制动并非前列腺癌所独有。
这对未来治疗意味着什么
总体而言,该研究提出 CRBN 作为一种代谢守门员,限制癌细胞为松散、迁移并播种新肿瘤所需的能量供应。当 CRBN 丢失或含量低时,6PGD 积累、NADPH 产量激增,细胞更容易发生有利于转移的变化。对患者而言,这提出两种可能性:检测 CRBN 与 6PGD 水平可用于标识高转移风险的肿瘤;以及增强 CRBN 功能或在 CRBN 缺乏的肿瘤中选择性抑制 6PGD 的疗法,可能为减缓或阻止前列腺癌及其他癌种转移提供新策略。
引用: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
关键词: 前列腺癌转移, 癌症代谢, cereblon, 6PGD 酶, NADPH 通路