Clear Sky Science · zh
L1TD1通过增强ABCC3 mRNA稳定性促进结直肠黏液腺癌进展
为何这种黏液过多的癌症值得关注
结直肠癌是全球主要的致死性癌症之一。在其中,有一种特殊亚型称为黏液腺癌,其肿瘤充满了占肿瘤体积一半以上的浓稠黏液。这层黏糊屏障可能帮助癌细胞躲避化疗和机体免疫。这项研究提出了一个基础但关键的问题:究竟是什么控制了这些黏液?我们能否关闭这一过程以放慢癌症进展并提高治疗效果?
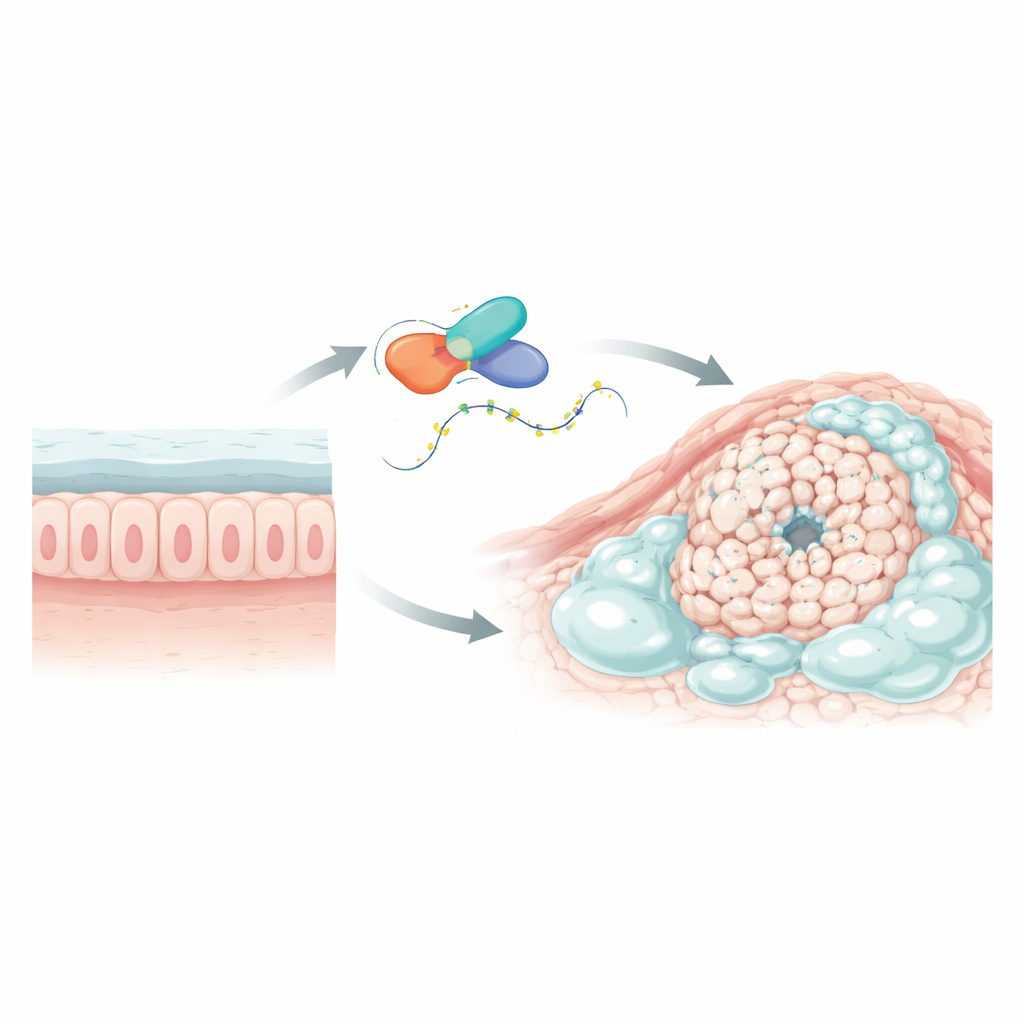
发现一个关键的“麻烦基因”
研究人员首先搜索了大型癌症数据库和单细胞测序数据,找出在黏液丰富的结直肠肿瘤中与普通结直肠癌及邻近健康组织表现不同的基因。有一个基因,称为L1TD1,显著突出。它在黏液型肿瘤中明显上调,但在常规肿瘤中并不高,并且在肿瘤组织中高于周围正常结肠组织。L1TD1编码一种与RNA结合的蛋白质,而RNA是将遗传信息从DNA传递给细胞蛋白合成机器的分子。由于RNA结合蛋白可以微调信息分子的寿命和被阅读的强度,L1TD1因此成为在这些黏液浸润癌症中充当主控因子的有力候选者。
L1TD1如何推动癌症生长和扩散
为测试L1TD1的实际作用,团队使用了结肠癌细胞系和小鼠模型。当他们在癌细胞中提高L1TD1水平时,细胞增殖更快、迁移性更强,并更具侵袭性地穿过类组织屏障。降低L1TD1则产生相反效果,减缓生长并减少侵袭。在注入高L1TD1细胞的小鼠中,肿瘤生长更大并更频繁地转移到肝脏和腹腔。患者样本中高L1TD1的肿瘤也倾向于更大、分化差、分期更晚,将该基因与临床上更差的疾病行为联系起来。
激活黏液产生与药物耐受
黏液本身被证明是L1TD1影响的核心。含有更多L1TD1的细胞产生更多关键黏液形成蛋白,尤其是MUC2和MUC5AC,并显示出类似杯状细胞(肠道正常分泌黏液的细胞)的特征。来自病人和小鼠的三维培养和组织染色证实,L1TD1升高与更厚、更丰富的黏液同时出现。重要的是,这种黏液并非旁观者。当研究者选择性降低MUC2时,由L1TD1驱动的额外增殖、侵袭和化疗耐受性大部分消失。富含L1TD1的细胞对常用药物奥沙利铂更难以被杀死,携带这些细胞的肿瘤在接受治疗的小鼠中缩小较少,强调了L1TD1促成的黏液作为一种保护屏障的作用。
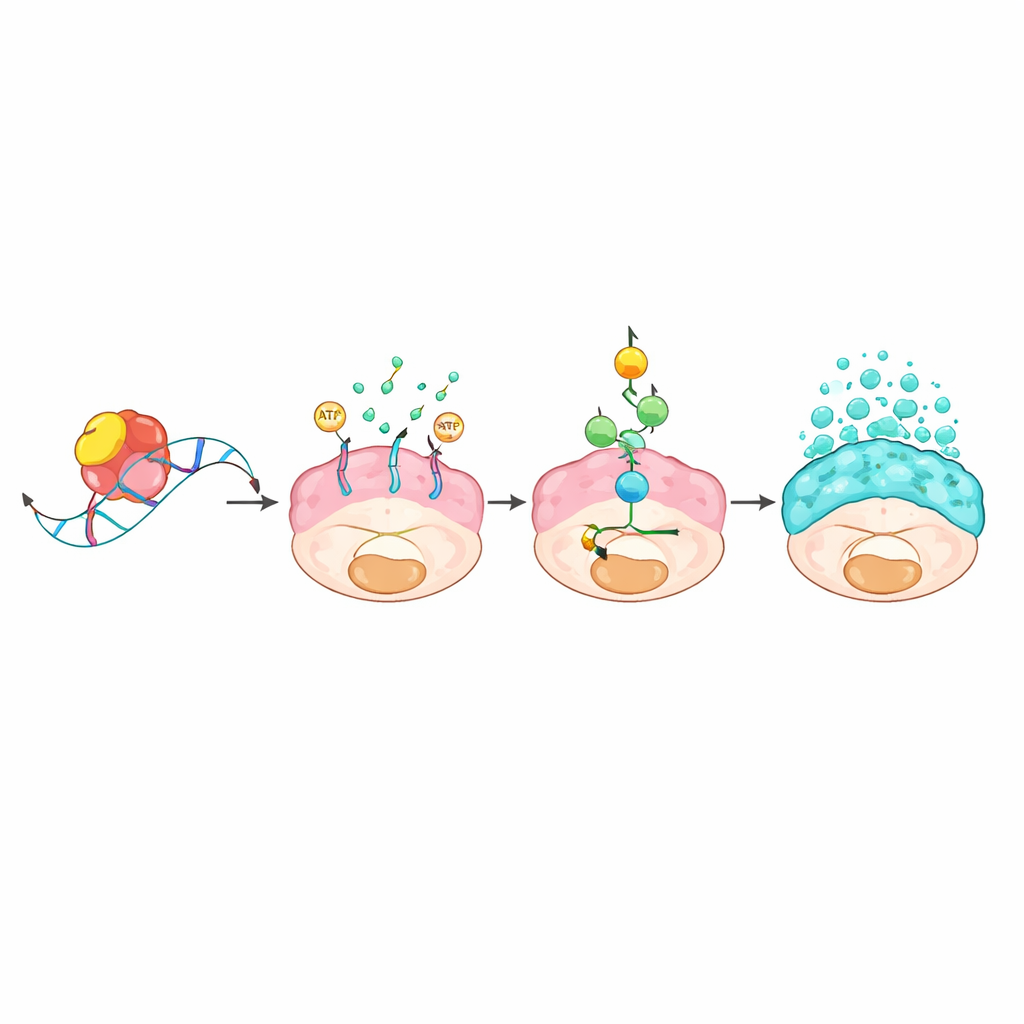
将RNA调控与黏液泛滥连接起来的分子链
团队进一步探寻一种RNA结合蛋白如何引发如此显著的变化。通过捕获物理结合到L1TD1的RNA并比较有无L1TD1时的基因表达,他们确定了一个转运蛋白基因ABCC3为主要靶点。L1TD1附着在ABCC3 mRNA尾端的短“GUGU”基序上,使该信息分子更稳定,从而细胞合成更多被称为MRP3的ABCC3蛋白。该转运体位于细胞膜并消耗能量将物质泵出细胞。由此产生的能量消耗激活了以感应器AMPK为中心的代谢警报系统,进而启动了经典的生长与应激通路MAPK。该级联一旦被激活,就增强了黏液蛋白的合成与分泌,并强化了癌细胞的增殖、迁移和抗药能力。用遗传方法或实验性化合物阻断ABCC3,或抑制MAPK通路,均可降低黏液产生并削弱肿瘤。
对患者意味着什么
总体来看,这项工作揭示了黏液型结直肠癌的分步骤控制机制:L1TD1稳定ABCC3的mRNA,ABCC3消耗细胞能量,AMPK–MAPK通路被激活,肿瘤通过过度产生黏液变得更具侵袭性和耐药。对患者而言,这提示了若干有前景的方向。L1TD1和ABCC3的水平可以帮助识别可能行为更凶险或对标准化疗更具抗性的肿瘤。更重要的是,干扰L1TD1–ABCC3相互作用、阻断MRP3泵功能或靶向下游信号通路的药物,可能削薄黏液屏障、减缓肿瘤生长并提高现有治疗对这一挑战性结直肠癌类型的疗效。
引用: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
关键词: 黏液性结直肠癌, L1TD1, ABCC3 MRP3, 黏液产生, 化疗耐受性