Clear Sky Science · zh
多功能RNA解旋酶DDX39A通过调节WISP1可变剪接驱动胶质母细胞瘤进展并诱导免疫抑制性巨噬细胞极化
这项脑癌研究为何重要
胶质母细胞瘤是最致命的脑癌之一,因治疗后易复发且耐药而臭名昭著。本研究揭示了肿瘤细胞内的一个分子“开关”不仅促进癌细胞生长,还能说服周围免疫细胞停止攻击、转而保护肿瘤。通过追踪这一路径,研究人员还发现了一种可重新利用的现有抗精神病药,可能用于破坏这一有害网络。
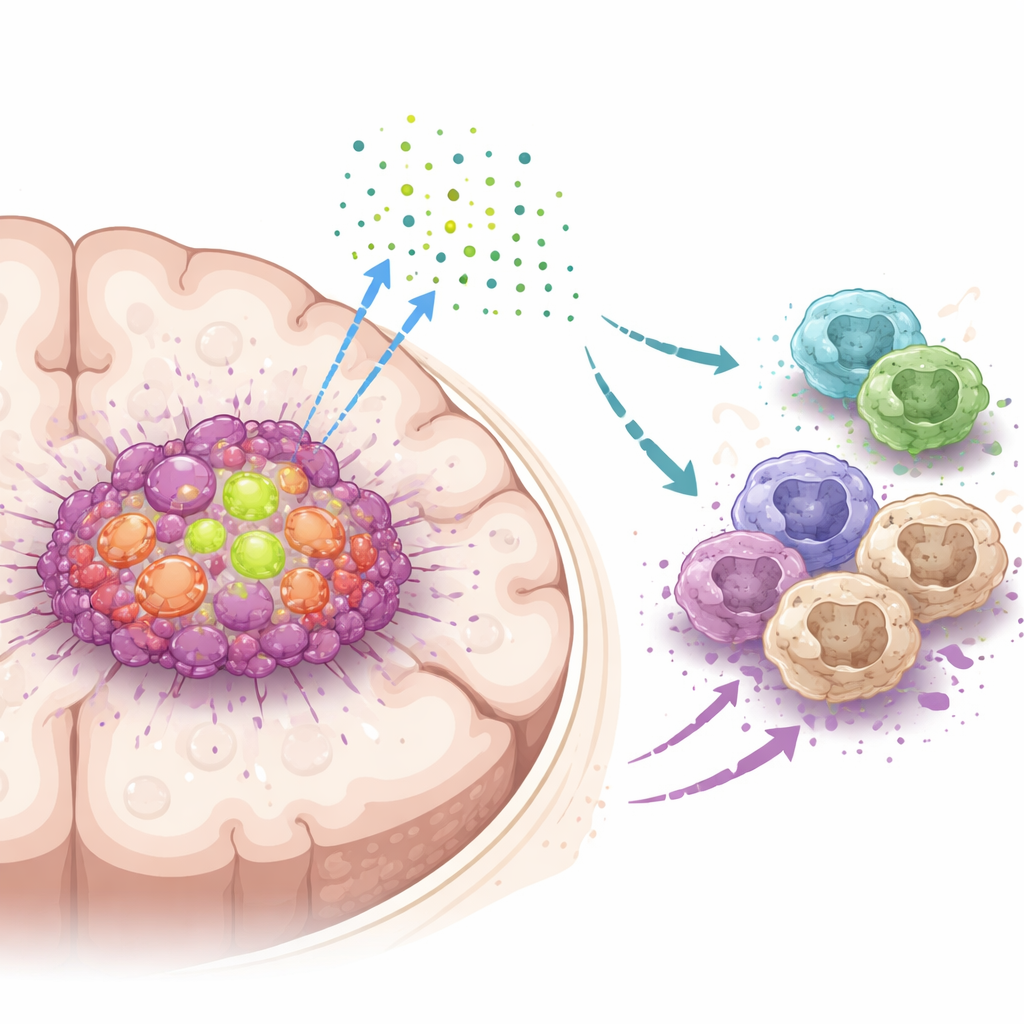
肿瘤细胞内的一个关键助力
研究团队聚焦于一种名为DDX39A的蛋白,它是一台帮助细胞处理RNA(遗传信息工作拷贝)的分子机器。通过分析大规模患者数据集和肿瘤样本,他们发现DDX39A在胶质母细胞瘤中比正常脑组织更为活跃,且其表达水平随肿瘤等级升高。单细胞分析显示,DDX39A在快速分裂的肿瘤细胞以及肿瘤内部某些名为巨噬细胞的免疫细胞中尤其丰富。肿瘤中DDX39A水平较高的患者通常预后更差,表明该蛋白与侵袭性疾病密切相关。
该助力如何促进生长与扩散
为测试DDX39A的实际作用,研究人员在体外培养的胶质母细胞瘤干样细胞和小鼠脑肿瘤模型中使用遗传学工具下调其表达。当DDX39A减少时,肿瘤细胞生长变慢、对周围组织的侵袭性下降,且更容易发生程序性细胞死亡。癌症干样细胞形成新肿瘤球体的能力也大幅下降,显示其自我更新能力受损。在小鼠体内,降低DDX39A的肿瘤更小,动物生存期延长,证实该蛋白积极驱动肿瘤进展,而非仅为被动标记。
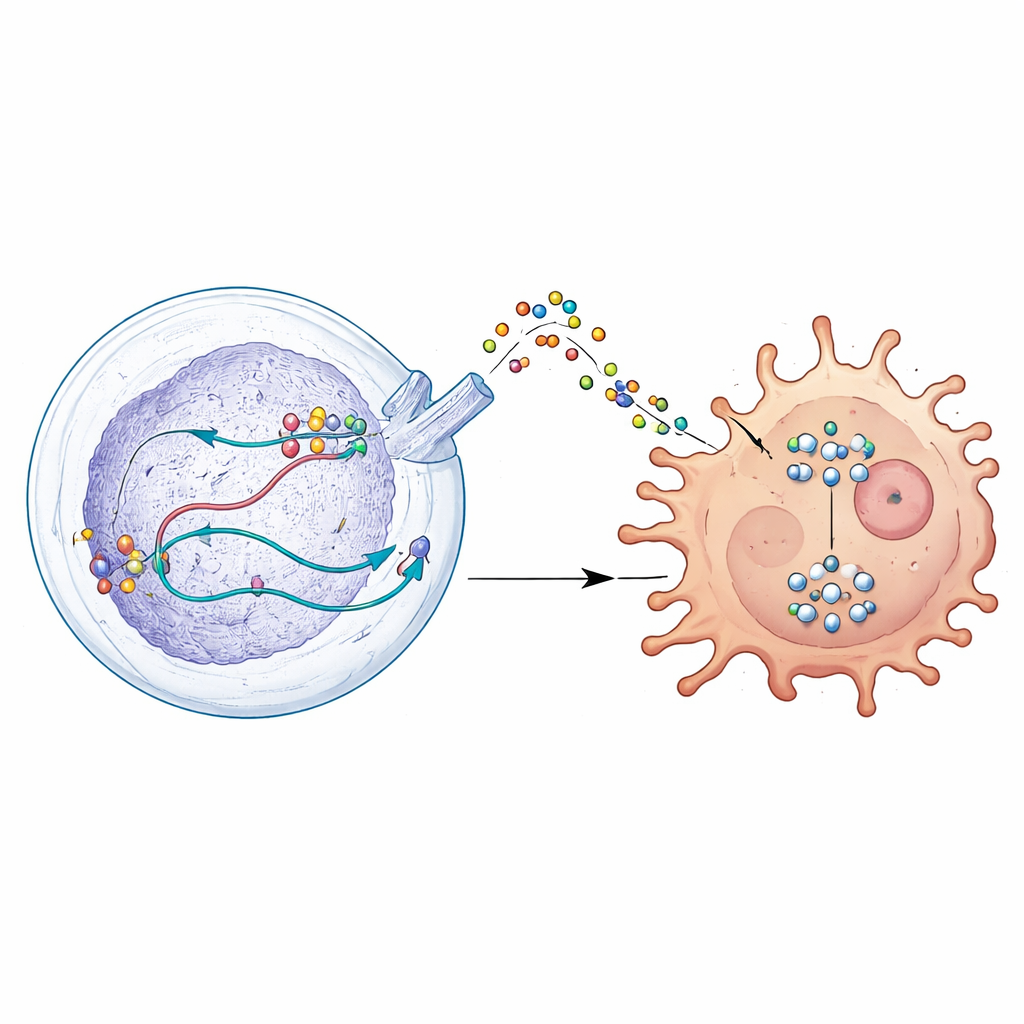
一种使免疫防御失能的秘密信号
进一步研究表明,DDX39A改变了名为WISP1的基因的加工方式。DDX39A并非简单地开启或关闭WISP1,而是帮助塑造其RNA,使信息更加稳定并提高WISP1蛋白的产生。肿瘤细胞随后将WISP1释放到周围环境中,起到一种误导性的信号作用。附近的巨噬细胞——既可攻击肿瘤也可支持肿瘤——对这一信号的反应是转变为免疫抑制、支持肿瘤的状态。这一转变通过细胞内被称为AKT的生长控制通路被驱动。当降低DDX39A或WISP1时,该通路被抑制,肿瘤细胞变得不那么侵袭性,巨噬细胞也更倾向于恢复为抗肿瘤的表型。
把一种精神病药转为抗癌武器
在绘制出这条通路后,研究者在药物数据库中寻找可能干扰DDX39A活性的分子。他们将目光锁定在氟哌啶醇(fluphenazine)上,这是一种使用已久、能进入大脑的抗精神病药。计算建模和结合实验显示,氟哌啶醇可直接与DDX39A结合。在肿瘤细胞中,该药削弱了DDX39A与WISP1 RNA的结合,降低了WISP1水平并抑制了AKT信号。经处理的细胞生长减少、侵袭性下降、形成的肿瘤球体更少且更易死亡。在小鼠模型中,氟哌啶醇减缓了脑肿瘤生长、降低了支持肿瘤的巨噬细胞数量并延长了生存期,且所用剂量与该药在人类治疗其他疾病时的剂量相近。
对未来治疗的意义
通俗地说,这项研究表明胶质母细胞瘤细胞利用DDX39A精细调控一种信息(WISP1),此信息既增强了肿瘤细胞自身的坚韧性,又将周围免疫细胞重编程为护卫而非战士。通过基因或如氟哌啶醇之类的药物阻断这一助力,可在两个层面削弱肿瘤:直接削弱肿瘤细胞及其由免疫抑制性巨噬细胞构成的保护屏障。尽管在这一策略进入临床前仍需大量进一步测试,但这项工作为将一种已知药物再利用以攻击这一顽固脑癌的新暴露弱点开辟了有前景的途径。
引用: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
关键词: 胶质母细胞瘤, RNA剪接, 肿瘤微环境, 巨噬细胞极化, 药物再利用