Clear Sky Science · zh
ULK1在上皮性卵巢癌实验模型中促进转移进展
这项研究为何重要
上皮性卵巢癌常在已经悄然扩散到腹腔后才被发现,因此成为女性中致死率极高的癌症之一。扩散的关键一步是肿瘤细胞形成悬浮在腹腔液中的微小团簇,称为球状体(spheroids);这些球状体能在化疗中存活并播种新的肿瘤。本研究提出一个集中而重要的问题:一种被称为ULK1的细胞“存活开关”是否帮助这些细胞簇存活并扩散?抑制它是否能为晚期卵巢癌开辟新的治疗途径?
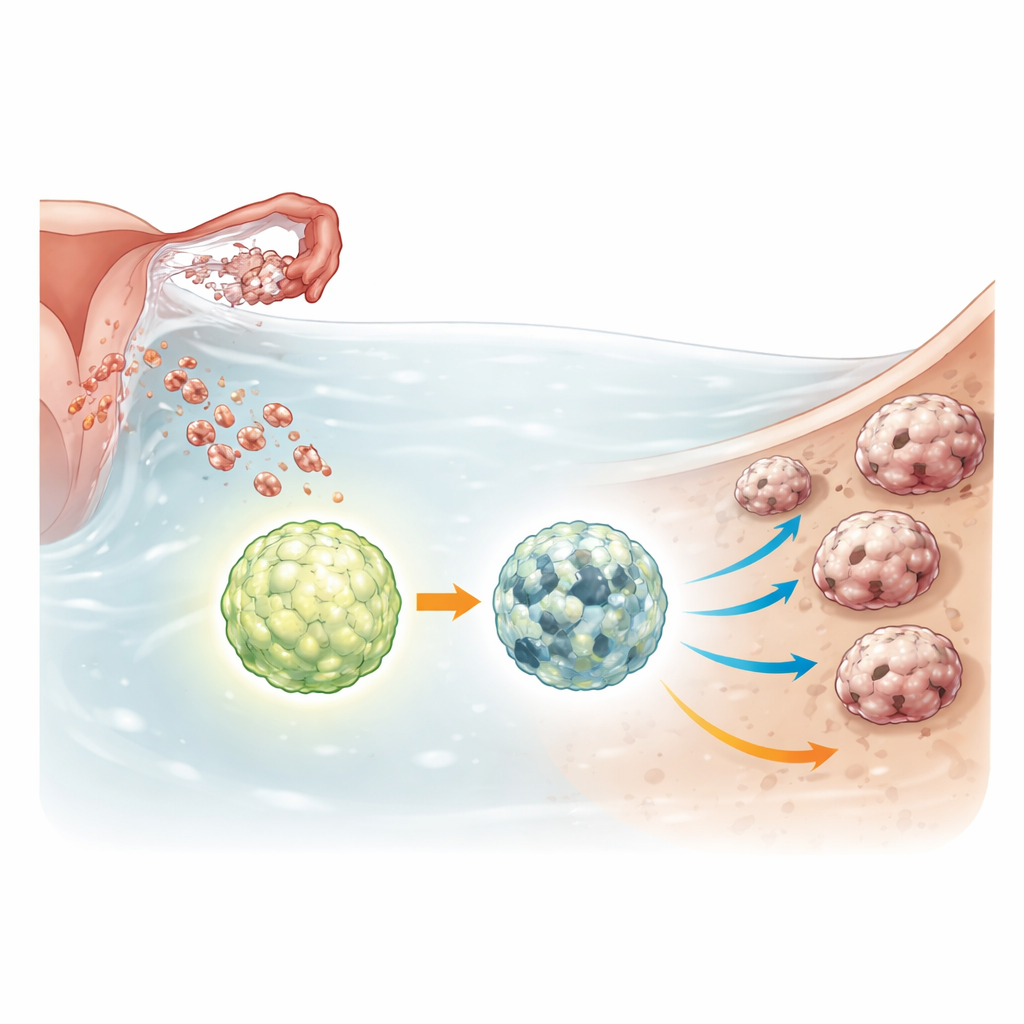
癌细胞簇中的存活开关
卵巢癌球状体要面对严酷环境:营养不足、失去附着以及化疗药物的暴露。为应对这些胁迫,它们会增强一种称为自噬的回收过程,自噬分解并重利用细胞内成分以在压力下维持生存。ULK1是启动这一回收系统的主要开关。研究者利用基因编辑工具在多种卵巢癌细胞系以及代表癌前阶段的非癌性输卵管细胞系中完全删除了ULK1,然后比较正常细胞与缺失ULK1细胞在作为自由悬浮球状体或三维微型肿瘤(类器官)生长时的行为差异。
当开关被关闭会发生什么
在卵巢癌细胞中删除ULK1后,其在球状体内执行自噬的能力受到严重削弱,关键回收蛋白的变化证明了这一点。这些缺失ULK1的球状体含有更少的存活细胞并表现出更多的程序性细胞死亡迹象,表明癌细胞簇不再能有效抵御胁迫。值得注意的是,从非癌性前体细胞中移除ULK1并没有在同等程度上关闭其回收系统,这提示癌细胞比健康细胞更依赖ULK1。这种癌特异性的依赖性使ULK1成为有吸引力的治疗靶点。
减缓扩散并削弱肿瘤据点
除了在悬浮状态下存活,球状体还必须附着并侵入腹腔内壁的光滑衬里才能形成新的肿瘤。使用模拟这一早期转移步骤的体外模型,研究团队表明缺失ULK1的球状体在推开并侵入覆盖内脏的间皮细胞层方面明显受阻。当作为嵌入凝胶基质中的类器官生长时,缺ULK1的癌细胞也形成了更小、更不健壮的肿瘤结构。在将人类卵巢癌细胞注入小鼠腹腔的模型中,失去ULK1导致肿瘤沉积减少和腹腔积液减轻,这些都是晚期疾病的典型特征,尽管动物的总体生存期并未因此改善。
削弱关键信号并增强靶向药物效果
为了解ULK1在自噬之外如何支持癌症,研究者绘制了缺ULK1球状体中的蛋白质变化图谱。他们发现细胞内主要的生长和存活通路,尤其是MEK–MAPK和PI3K–AKT–mTOR通路,受到了扰动。这些通路通常帮助癌细胞抵抗死亡并持续分裂。当研究团队对缺ULK1的球状体使用抑制MEK或mTOR的药物时,癌细胞簇变得更加脆弱,存活率和重新附着能力明显下降。相比之下,删除ULK1并未使常规化疗药物如卡铂、紫杉醇或PARP抑制剂奥拉帕利的疗效增强,在某些条件下反而似乎削弱了这些药物的益处。
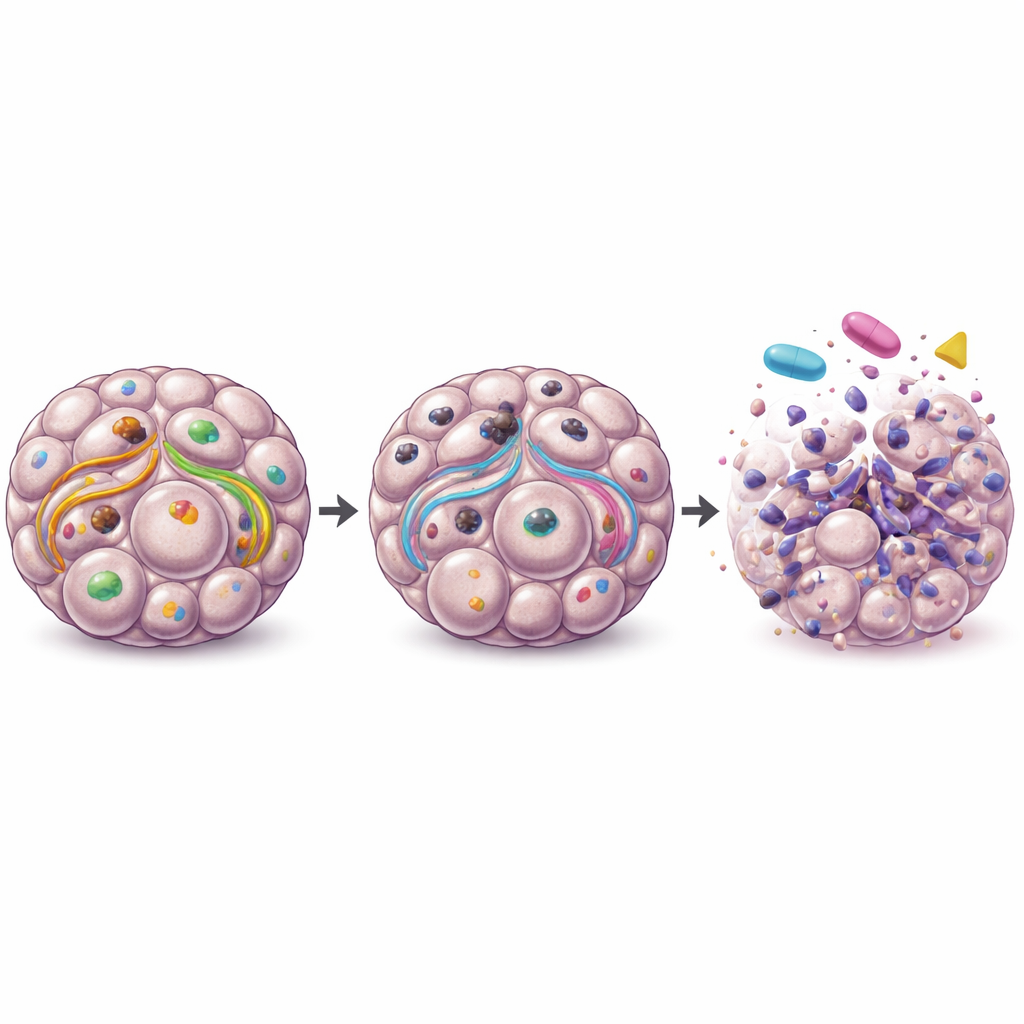
来自患者肿瘤与患者模型的线索
在大规模公开的卵巢肿瘤数据集中,作者发现较高的ULK1基因活性与较差的长期生存相关,并且在转移样本中比原发肿瘤和正常组织更为升高。为更接近临床应用,他们在来自转移肿瘤样本的患者来源类器官上测试了一种临床ULK1口服抑制剂DCC-3116。在一部分患者模型中,单独抑制ULK1或单独使用MEK或mTOR抑制剂都能降低类器官存活,但联合用药并未始终带来额外益处。其他患者来源的类器官对所有处理均表现耐药,强调了卵巢癌的高度异质性以及识别可能受益患者所需生物标志物的重要性。
这对未来治疗意味着什么
综上所述,研究结果将ULK1描绘为卵巢癌扩散的核心助手:它驱动维持球状体存活的细胞内回收过程,支持其侵入新部位的能力,并帮助维系强大的生长信号。关闭ULK1会削弱这些过程,缩小实验性肿瘤,并使癌细胞簇对某些靶向药物更敏感,但对常规化疗并无增强作用。对于患者而言,这项工作表明ULK1可能成为精准医学策略的一部分——尤其针对ULK1高表达的转移性疾病——将ULK1抑制剂与MEK或mTOR抑制剂联合使用以限制肿瘤生长和扩散,前提是能通过严谨检测识别出最有可能获益的肿瘤。
引用: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
关键词: 卵巢癌, 转移, 自噬, ULK1, 靶向治疗