Clear Sky Science · zh
视黄醇类、视黄酸受体与表观遗传学在乳腺癌中的关联
维生素A为何与乳腺癌相关
大多数人把维生素A视为对视力重要的营养素,但它在体内的活性形式——视黄酸,也帮助细胞决定是否增殖、分化或在受损时自我凋亡。本文综述了视黄酸及其细胞“停靠点”在乳腺癌中的改变,探讨为何实验室中令人鼓舞的结果尚未转化为对患者有效的药物,以及对癌细胞“软件”——表观遗传代码——的新认识如何可能重振这一治疗策略。
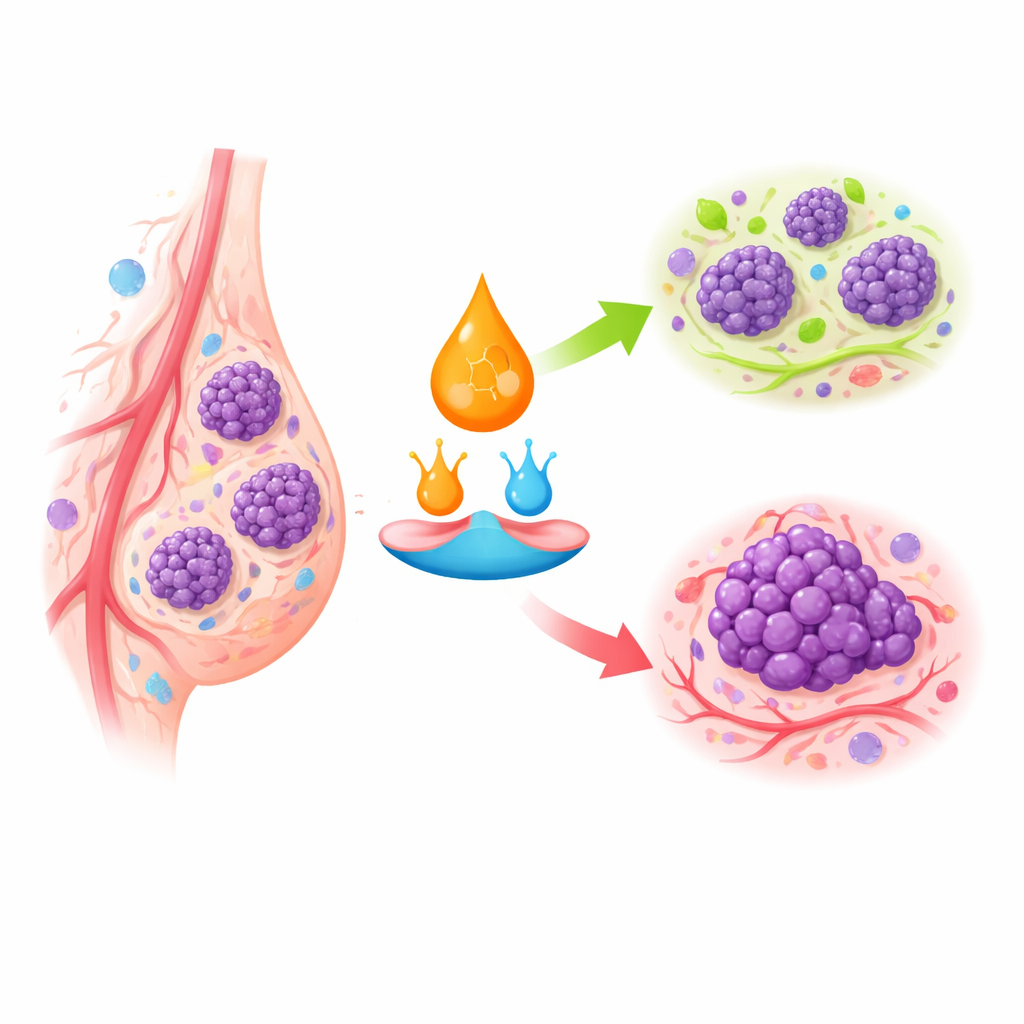
细胞内的生长与自毁交通信号
视黄酸通过结合细胞内特定受体发挥作用,受体随后将整组基因打开或关闭。在健康乳腺组织中,该系统促使细胞停止分裂、成熟为稳定状态,或在异常时走向凋亡。在乳腺癌中,尤其是更具侵袭性的亚型,关键受体丢失或被沉默,视黄酸的细胞内运输路径也被改写。它可能不再被输送到抑制生长的受体处,而是被引导进入促进存活和增殖的通路。这有助于解释为何一些乳腺肿瘤对视黄醇类药物反应甚微,而这些药物在某些血液系统恶性肿瘤中却高度有效。
癌细胞“软件”中的隐性开关
作者关注表观遗传学——附着在DNA及其包装蛋白上的化学标签,像基因组的软件设置那样工作。在许多乳腺癌中,这些标签将重要的视黄酸受体,尤其是称为RARβ2的受体,锁定在“关闭”状态,而不改变基础的DNA序列。DNA上的额外甲基和周围蛋白卷绕的紧缩使该受体失活,同时其他酶重塑染色质格局以利于生长和迁移。非编码RNA虽不翻译成蛋白,但会影响基因活性,进一步将信号偏向于抑制细胞死亡与分化。诸此变化共同赋予癌细胞抵抗治疗和适应压力的灵活性。
重连信号通路
重要的是,这些表观遗传上的“锁”是可逆的。在实验模型中,能去除DNA甲基或放松染色质的药物可以恢复RARβ2及视黄酸通路的其他组成部分。当这些“诱导”试剂与视黄酸本身及标准化疗联合使用时,可更有效地缩小肿瘤并减少被认为驱动复发的干样细胞群体。视黄酸在细胞内的运输方式也很关键:一种载体蛋白将其引导至抑制生长的受体,而另一种则送往促增长的通路。调整这些载体之间的平衡可以使视黄酸从“施肥剂”般的作用转为像刹车一样抑制生长。
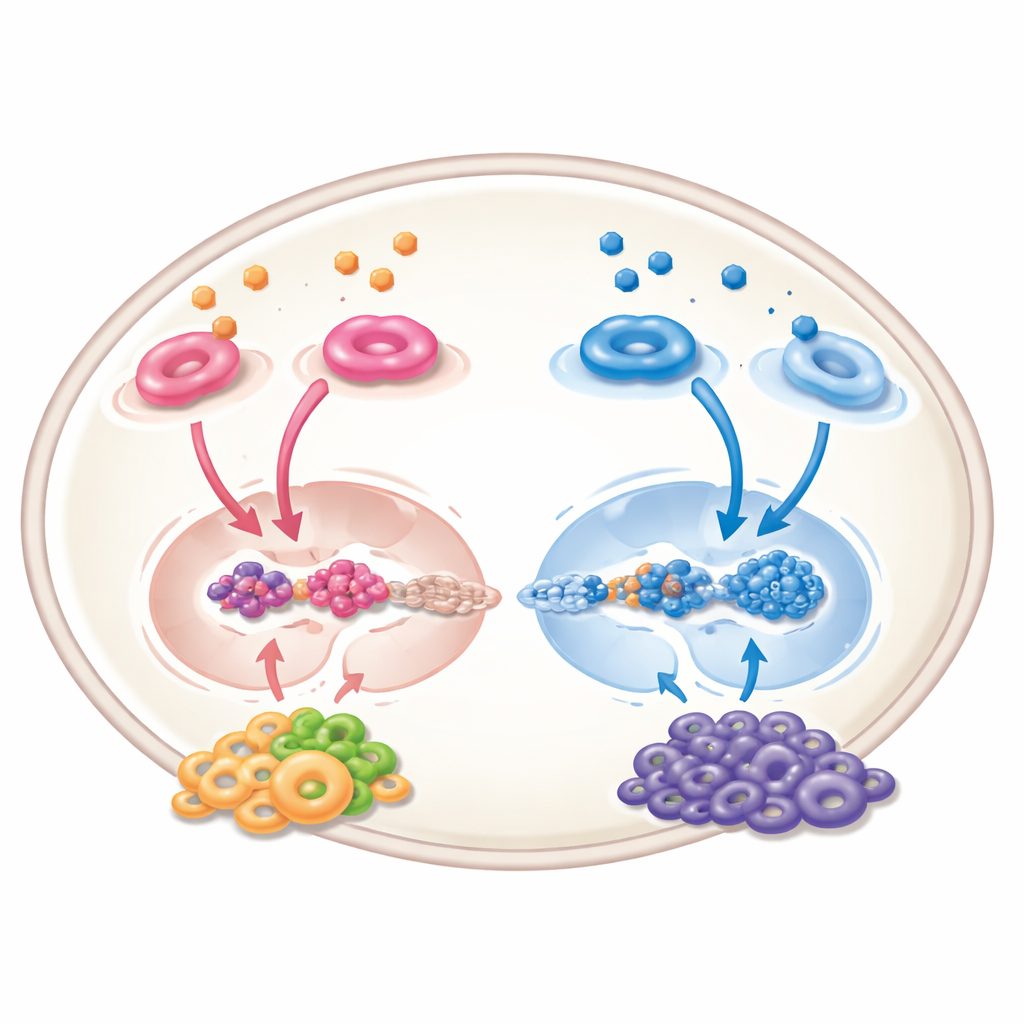
超越肿瘤本身:邻里效应
视黄酸并非只作用于癌细胞;它也重塑肿瘤周围的“邻里”——血管、免疫细胞和支持细胞。在实验系统中,它能减少新血管生成,使免疫细胞转向更活跃、更具有抗肿瘤性的状态,并限制通常抑制机体防御的细胞。然而,情况并非全然有利:在某些包绕肿瘤的基质细胞中,视黄酸信号的激活实际上可能通过强化吸引并支持恶性细胞的化学通讯而促进癌症生长。这些相互矛盾的效应意味着未来的任何治疗都必须谨慎调整,以在正确的细胞类型上以正确的方式发挥作用。
为未来设计更聪明的试验
早期针对乳腺癌的视黄醇类药物临床试验大多失败,但这些试验开展于我们对亚型、生物标志物和复杂药理学认识之前。作者主张新试验应筛选出肿瘤显示视黄醇敏感分子标志的患者,例如保留的受体表达或特定的DNA甲基化模式,并将视黄醇与可解除表观遗传阻滞、靶向生长通路或增强免疫攻击的药物配合使用。改进的制剂以维持体内稳定的药物浓度,并对肿瘤及其周围组织进行密切监测,将至关重要。如果能克服这些障碍,基于视黄酸的治疗或许仍能作为针对特定乳腺癌类型的精准工具找到一席之地。
引用: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
关键词: 视黄酸, 乳腺癌, 表观遗传学, 分化疗法, 肿瘤微环境