Clear Sky Science · zh
模拟脂肪组织与癌症的串话:三维视角
脂肪与癌症比你想的更密切
我们大多数人把体内脂肪看作多余的衬垫或储存能量,但研究现在表明它是一个繁忙且善于“交流”的器官,会以意想不到的方式影响健康。本文综述探讨了脂肪组织与癌细胞如何相互沟通,以及新的三维(3D)实验室模型如何比以往更逼真地模拟这种对话。理解这一隐秘交流有望改善癌症预防、药物检测和治疗,尤其在肥胖日益普遍的背景下。 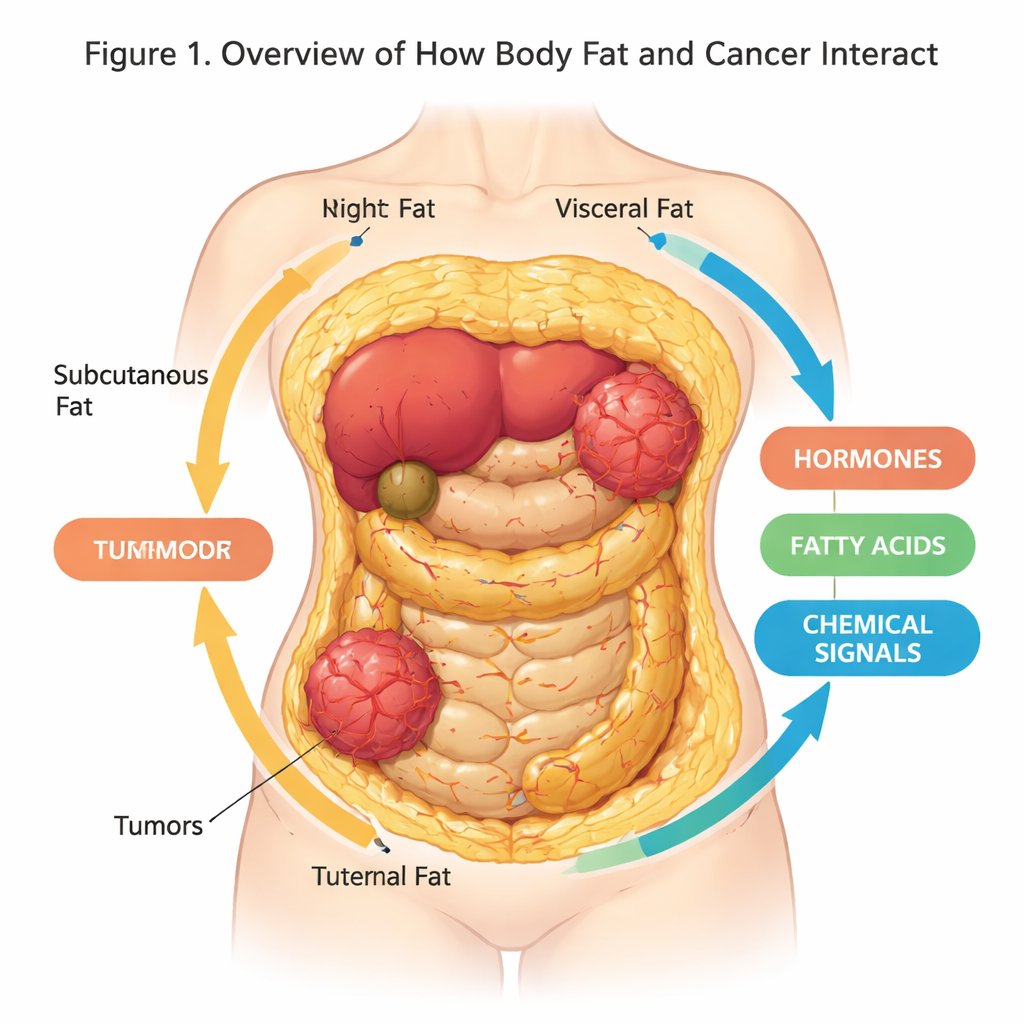
作为有生命、有“对话能力”的器官的脂肪
脂肪组织——我们的体脂并非仅仅是被动的储存场所。它是由脂肪细胞、免疫细胞、血管和支持细胞组成的复杂器官,这些细胞嵌入于被称为细胞外基质的结构性网格中。不同类型的脂肪分布在不同部位:皮下脂肪位于皮肤下,内脏脂肪环绕内脏,还有在能量储存或将其作为热量燃烧方面各异的白色、棕色和米色脂肪细胞。这些细胞不断释放激素、脂肪酸和信号蛋白的混合物,影响代谢、炎症以及我们现在了解到的癌症风险和行为。
肥胖、炎症与癌症风险
当我们体重过重时,白色脂肪细胞在体积和数量上都增长,组织因此承受压力并发生炎症。这种“病态”脂肪释放更多的炎性分子和脂肪酸进入血液,同时对糖和脂质的处理变差。大型流行病学研究已将肥胖与多种癌症(包括乳腺癌、结肠癌、胰腺癌和子宫癌)发病率升高和预后更差联系起来。综述解释了功能失调的脂肪如何为肿瘤提供额外燃料、使周围组织变硬并招募其他细胞类型,从而共同营造更有利于癌症的环境。
脂肪与肿瘤之间的双向对话
现在人们把癌症视为整个生态系统的疾病,而不仅仅是失控的细胞。肿瘤细胞利用邻近的脂肪获取支持,重编程脂肪细胞、免疫细胞和成纤维细胞以助其生长和扩散。作为回馈,脂肪细胞通过分解储存的脂质并释放脂肪酸和激素来响应,癌细胞可以直接利用这些物质。这种串话既可通过循环信号远程发生,也可在肿瘤与脂肪紧邻生长的局部发生,如乳腺或腹部。肿瘤细胞甚至能促使脂肪细胞失去原有身份,转变为更类似瘢痕形成或免疫样的细胞,重塑组织并促进侵袭。 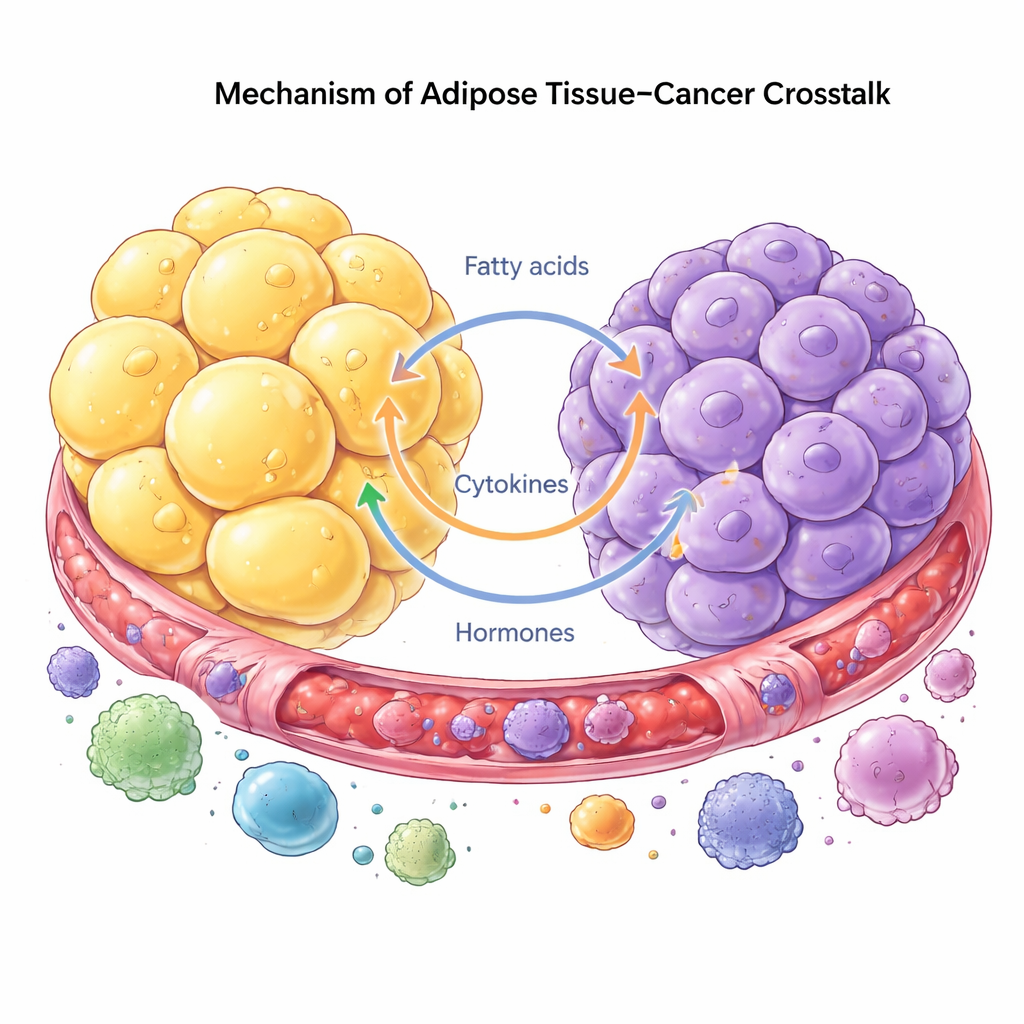
构建三维微型组织
传统的平面(2D)细胞培养和动物模型常常无法捕捉这些复杂相互作用。作者描述了新一代更接近真实组织的3D系统。球体(spheroids)是自组装成微小球状的简单细胞簇;支架(scaffolds)是为细胞生长提供三维支撑的工程材料;类器官(organoids)是组织的微型自组织版本;而组合体(assembloids)将多个类器官或球体合并成复合的“微器官”。研究者目前利用这些3D方法共同培养脂肪细胞与癌细胞,研究类似肥胖的条件如何改变它们的行为,并测试药物如何干扰它们之间有害的对话。
希望与现存差距
每种模型都有权衡。球体成本低、适合高通量但相对简单。支架允许对物理特性(如刚度)进行精细控制,而这些特性可影响癌症扩散,但技术要求更高。类器官和组合体捕捉到最高水平的现实性,包含多种相互作用的细胞类型,然而它们成本高、难以标准化,且常常缺乏完整的血管网络或免疫成分。综述强调,当前的系统仍无法完美再现人体脂肪与肿瘤组织,尤其是在复制完整细胞外基质、成熟脂肪细胞和免疫细胞参与方面存在不足。
这项研究的未来方向
作者总结认为,改进脂肪—癌症相互作用的3D模型对于更准确的药物测试和揭示肥胖如何促进癌症至关重要。随着这些“微型组织”变得更逼真——将真实的脂肪、肿瘤细胞、血管和免疫细胞结合起来——它们可能帮助研究者预测特定患者哪种治疗有效、设计更好地阻断癌症利用体脂作为燃料的策略,并最终指导针对的不仅是肿瘤本身,还有那些助长肿瘤生长的不健康环境的治疗。
引用: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
关键词: 脂肪组织, 肥胖, 癌症微环境, 三维细胞培养, 肿瘤代谢