Clear Sky Science · zh
POM121 的 O-GlcNAc 化通过增强 c-MYC 核进入和重编程细胞外基质促进非小细胞肺癌骨转移
这项研究为何重要
当肺癌转移到骨骼时,会导致剧烈疼痛、骨折并显著缩短生存期,但临床上仍缺乏有效阻止这一致命步骤的手段。本研究深入探究肺癌细胞的内部机制,揭示部分肿瘤细胞如何获得一种特殊优势,使其能够从肺部迁移至骨骼并在其中存活繁衍。通过将这一过程追溯到细胞核边缘单一门控蛋白上的微小修饰,作者识别出一条新的事件链,可能成为更好预测、预防或治疗非小细胞肺癌骨转移的干预靶点。
改变癌细胞行为的一枚糖标记
研究者聚焦于翻译后修饰——蛋白质合成后获得的微小化学改变。其中一种被称为 O-GlcNAc 化的修饰,是将一个小糖分子连接到蛋白质的特定位点。研究团队使用肺癌细胞系和小鼠模型,比对了普通肿瘤细胞与经过重复筛选、具备更强骨定植能力的亚群。他们发现这些趋向骨转移的细胞总体上具有更高的 O-GlcNAc 化水平,这主要由负责添加该糖基的酶 OGT 活性增强所致。在数百种被修饰的蛋白中,一个蛋白尤为突出:POM121——核孔复合体的核心成分,负责控制进出细胞核的运输。
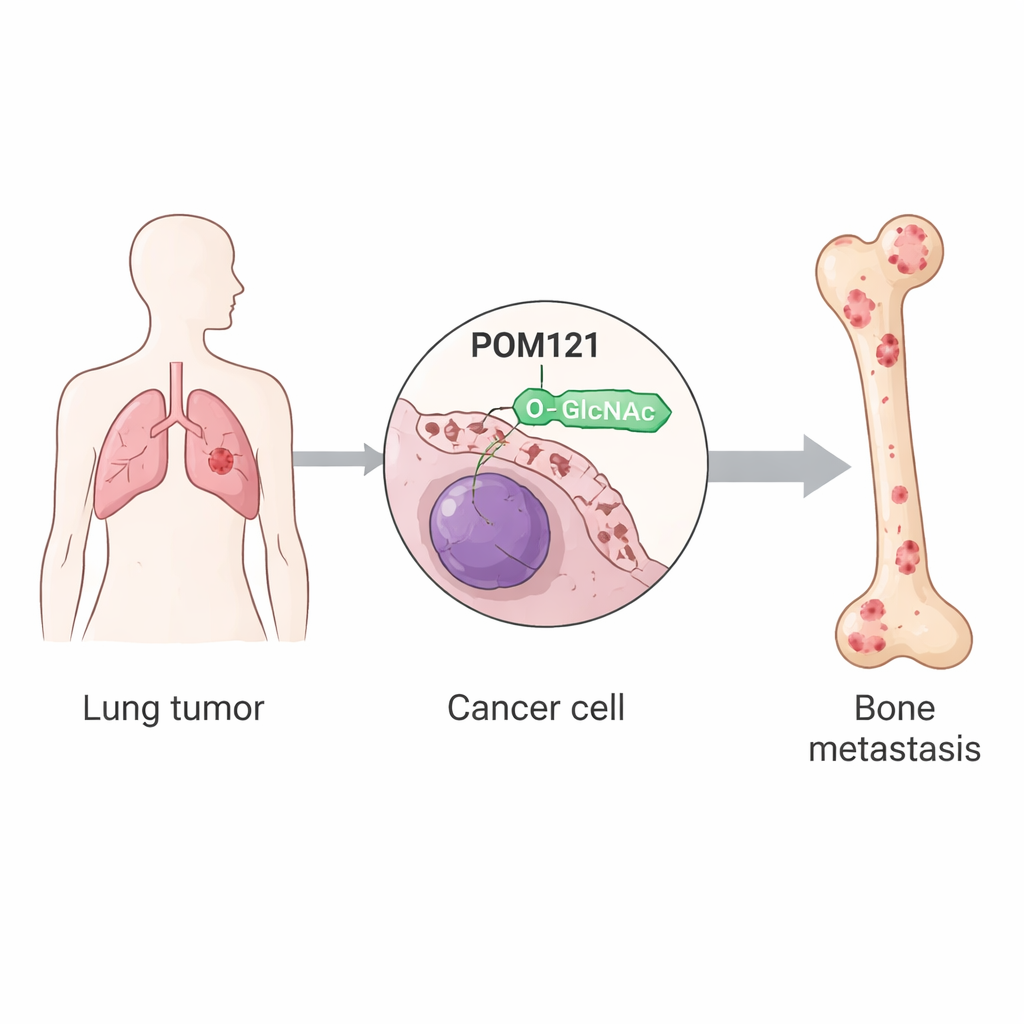
核门控蛋白 POM121 被稳定保存
POM121 嵌入包绕细胞核的膜中,构成许多信号蛋白必须通过的通道部分。在骨转移性肺癌细胞中,POM121 在一个名为丝氨酸199 的位点承载了大量 O-GlcNAc 修饰。当该位点被突变为无法被修饰时,蛋白变得不稳定并被细胞的降解机制迅速清除。研究显示,这枚糖标记保护 POM121 免于被一种名为 TRIM21 的酶标记为降解目标——TRIM21 通常会连接泛素作为“处理”标签。有了 O-GlcNAc,TRIM21 难以有效结合,泛素化减少,POM121 在核孔处积累而位置不变。
为强效致癌因子打开通道
额外稳定的 POM121 会带来什么影响?关键在于一个著名的促癌蛋白——转录因子 c-MYC。c-MYC 必须进入细胞核才能激活基因表达,而它的通过依赖于像 POM121 这样的核孔成分。作者证明,当 POM121 丰富且被 O-GlcNAc 修饰时,细胞核内的 c-MYC 增多;相反,当降低 POM121 水平或去除其糖基时,c-MYC 的核进入显著下降。在小鼠中,携带不可修饰 POM121 突变体的肺癌细胞形成的骨转移数量和体积明显减少,而在 POM121 缺失的细胞中恢复 c-MYC 则部分挽回了其骨定植能力。这把 POM121 放在 c-MYC 之上,成为一条关键转移通路的上游因素。
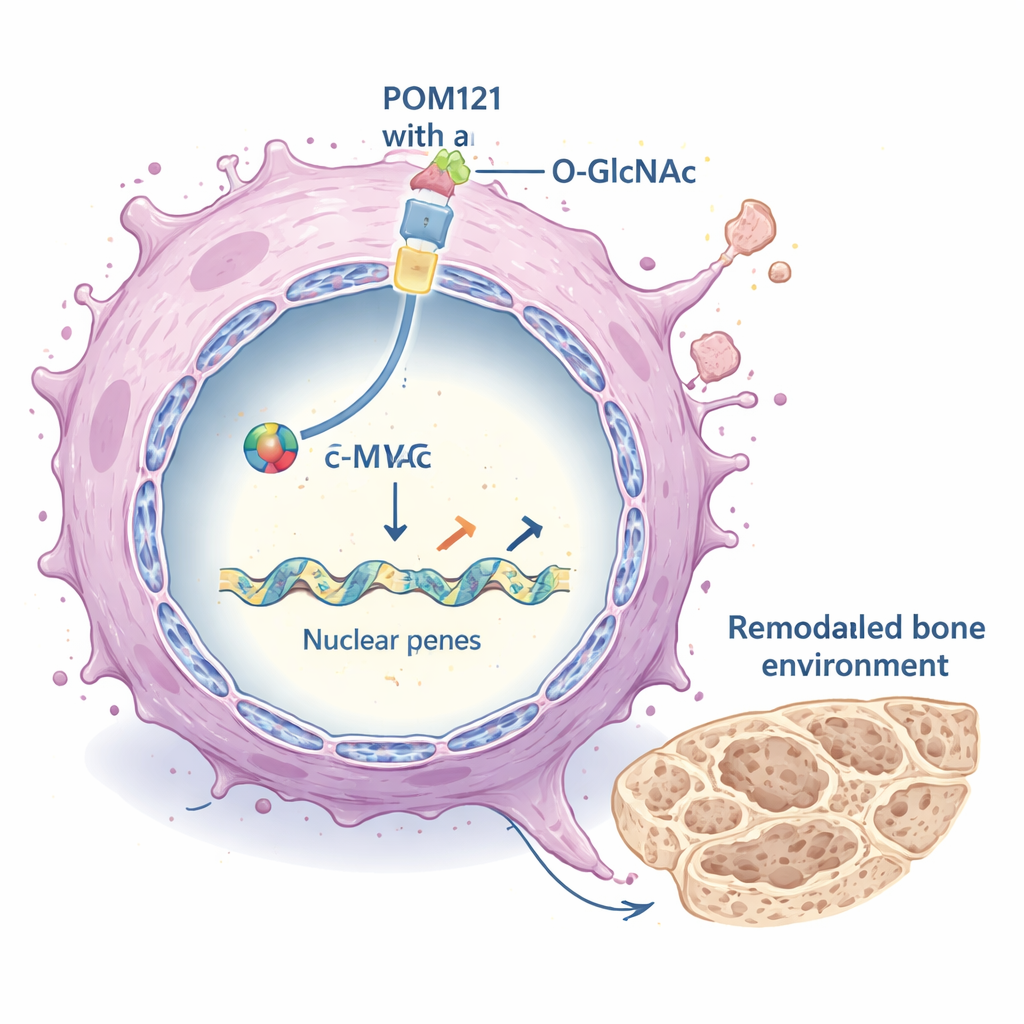
重塑肿瘤微环境
一旦进入细胞核,c-MYC 就像总开关一样控制大量基因。在本研究中,c-MYC 被发现强烈激活一组塑造细胞外基质(ECM)的基因——即包围细胞的支架蛋白。这些 ECM 基因,包括多种胶原蛋白及参与组织重塑的酶,在阻断 POM121 或 c-MYC 时表达下调,而在 O-GlcNAc 化和 POM121 水平升高时表达上调。改变的 ECM 反过来增强了癌细胞内的重要生长通路,尤其是支持生存、增殖与转移的 PI3K–AKT–mTOR 信号级联反应。多种不同的肺癌模型中出现的相似模式提示,这一机制并非局限于单一细胞系。
从实验室发现到患者受益
在患者数据中,研究者发现 OGT、POM121 和 c-MYC 的高表达,以及它们调控的 ECM 基因,与更差的预后和已经发生骨转移的肺肿瘤相关。综合来看,这项工作描绘出一条 OGT–POM121–c-MYC–ECM 轴:增加的 O-GlcNAc 化稳定了核门控蛋白 POM121,使更多 c-MYC 被运入细胞核,进而重编程组织支架与生长信号,促成骨转移。对患者而言,这提示了新的生物标志物以识别易发生骨转移者,以及潜在的治疗策略——从抑制 OGT 或 POM121 功能,到抑制 c-MYC 或干预 ECM 重塑——未来或能帮助阻止肺癌侵及骨骼。
引用: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
关键词: 肺癌 骨转移, POM121, O-GlcNAc 化, c-MYC, 细胞外基质