Clear Sky Science · zh
RNA 结合蛋白 FUS/TLS 通过扰乱雄激素受体-辅因子相互作用改变前列腺癌中的雄激素信号
这项研究为何关系到男性健康
前列腺癌高度依赖男性激素(称为雄激素)及感知这些激素的蛋白——雄激素受体。大多数现代治疗通过切断这些激素或阻断受体来发挥作用。然而许多肿瘤最终会逃避控制,以更难治疗的形式复发。本研究揭示了另一种蛋白 FUS/TLS 如何在早期前列腺癌中充当强有力的雄激素信号“刹车”——以及随着疾病进展该刹车如何失效。
激素信号的交通指挥官
雄激素受体就像一个分子开关。当雄激素与其结合时,受体移入细胞核,结合到 DNA 上,并激活有助于前列腺细胞生长的基因。它并非孤立工作:一类辅因子蛋白可以增强或抑制其活性。作者将注意力集中在 FUS/TLS(简称 FUS)上,这是一种已知参与 RNA 处理和基因调控的蛋白,且先前与肿瘤生长变慢有关。通过培养的前列腺癌细胞,他们发现许多受 FUS 调控的基因与雄激素受体调控的基因重叠,提示 FUS 直接影响激素信号如何被转化为生长指令。
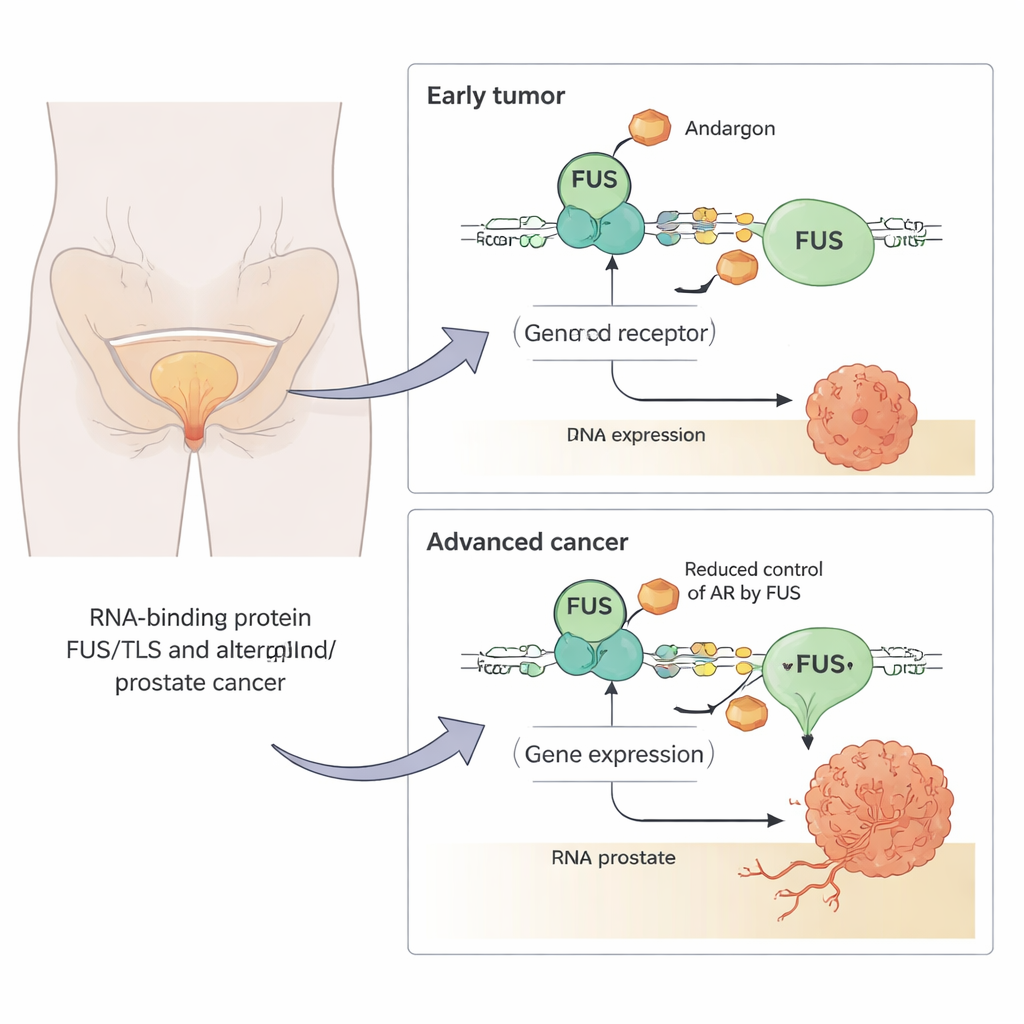
FUS 如何对促肿瘤基因踩刹车
为了弄清 FUS 的作用,研究组在前列腺癌细胞中人为升高或降低其水平,并在处理一种强效类雄激素药物时追踪基因表达变化。他们发现 FUS 可以双向调节雄激素控制的基因,有时增强有时减弱其响应。但主要效应是抑制:经典的雄激素刺激基因如 PSA(KLK3)和 TMPRSS2 在 FUS 水平高时被下调,而在去除 FUS 时则上调。报告基因测试——一种衡量雄激素受体活性的简单读出——证实增加 FUS 会将受体活性在多种细胞类型中大约降低到一半到三分之二左右。
对激素机器的物理封锁
科学家们接着探讨 FUS 如何施加这种控制。显微镜观察和相互作用检测表明 FUS 与雄激素受体在细胞核内相遇并发生物理结合。FUS 通过其 RNA 识别结构域附着于受体的特定区域。它还与若干通常会增强受体活性的关键辅因子结合。对一个著名的雄激素响应基因进行的精细实验显示,FUS 并不阻止受体结合 DNA;相反,它阻止了完整辅因子团队和基础转录机器在该位点的组装。换言之,FUS 将“开关”留在 DNA 上,但剥离了使基因表达完全调高所需的部件。
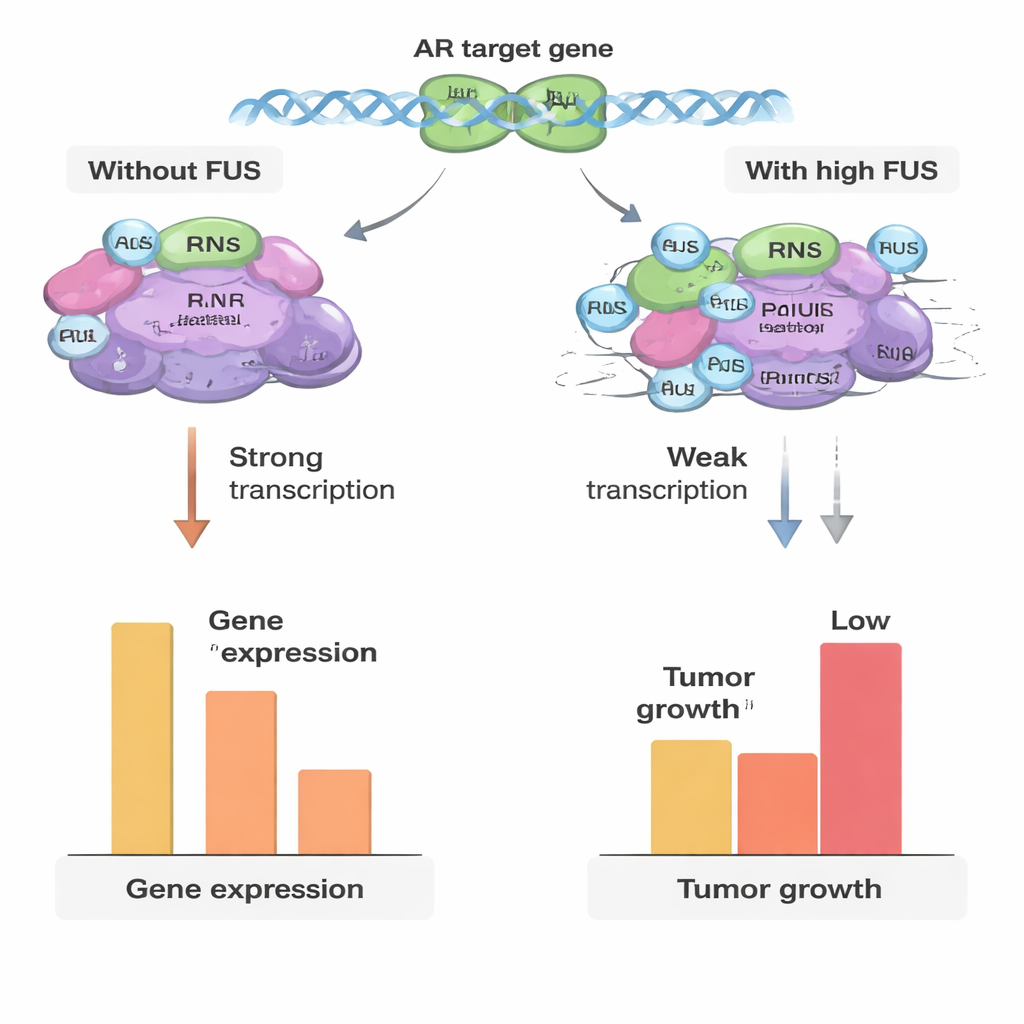
随着癌症进展角色的转变
由于前列腺癌的治疗耐药常涉及这些辅因子的变化,作者在细胞系和涵盖良性组织、原发肿瘤及晚期去势抵抗性前列腺癌(CRPC)的病人样本中检测了 FUS 水平。在早期肿瘤中,FUS 蛋白水平通常低于良性样本,这与肿瘤下调这一天然刹车以更易增长的观点一致。出乎意料的是,在晚期 CRPC 中,FUS 水平再次上升,并高于原发肿瘤。然而在一个拟 CRPC 的细胞模型中,提升 FUS 已不再显著改变依赖雄激素的基因,尽管其仍能减缓总体细胞生长。这提示随着癌症演化,雄激素网络被重塑以致 FUS 对受体的控制大幅减弱,同时 FUS 可能通过其他与生长相关的通路发挥作用。
对未来治疗的意义
对非专业读者而言,关键信息是 FUS 类似于一种内建的安全装置,通常将男性激素信号的驱动控制在不过度水平。在早期癌症中,降低 FUS 有助于肿瘤生长;在晚期疾病中,激素系统发生足够的改变,使得即便 FUS 丰富也不再有效约束雄激素受体。精确理解这一刹车如何工作——以及为何失效——可能启发出新的策略,或恢复其控制,或模拟其解除激素驱动生长的能力,从而有望改善晚期前列腺癌患者的治疗效果。
引用: Brooke, G.N., Leach, D.A., Culley, R.L. et al. Disruption of androgen receptor-cofactor interactions by the RNA-binding protein FUS/TLS alters androgen signalling in prostate cancer. Oncogene 45, 757–773 (2026). https://doi.org/10.1038/s41388-026-03682-3
关键词: 前列腺癌, 雄激素受体, 激素治疗耐药, RNA 结合蛋白, FUS TLS