Clear Sky Science · zh
Sortilin通过限制EGFR的传导功能表现出类肿瘤抑制活性
这对癌症治疗的意义
肺癌是全球范围内致死率最高的癌症,许多现代药物针对一种名为EGFR的分子,该分子驱动肿瘤生长。这些药物在初期常常效果显著,但肿瘤往往会出现耐药。该研究揭示了肺癌细胞内一种天然的“制动器”——一种名为sortilin的蛋白所扮演的意外角色,能够削弱EGFR的促癌信号。理解这种关联有助于解释为何部分患者对EGFR靶向疗法的反应更好,并可能提示保持这些疗法长期有效的新策略。 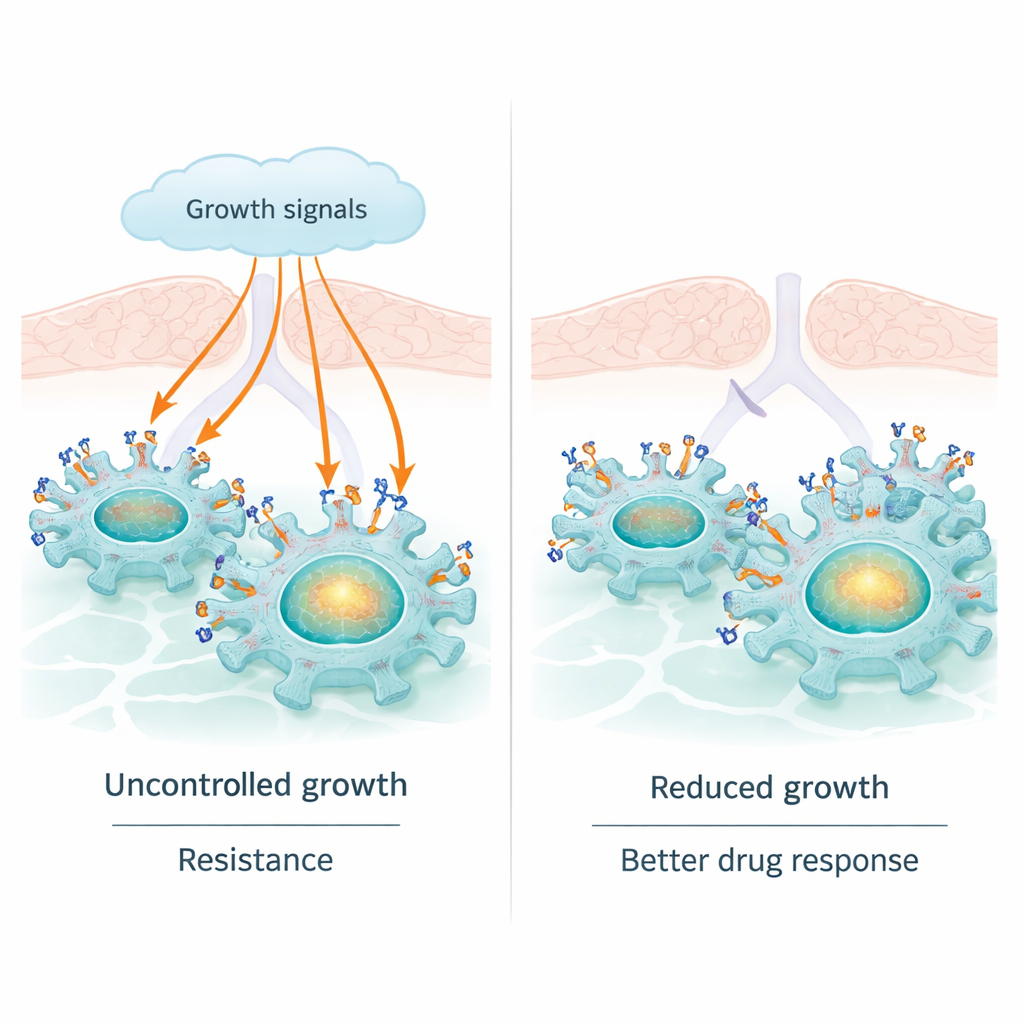
失控的生长开关
EGFR是位于许多细胞表面的受体,负责感知环境中的生长信号。在大量肺腺癌中,EGFR发生改变以致持续被激活。这推动了持续的生长和分裂,也是EGFR抑制药(称为酪氨酸激酶抑制剂)能使肿瘤缩小的原因。但EGFR还有一个较少被重视的面向:它可以进入细胞核并直接作用于DNA,启动诸如cMYC和CCND1等基因,进一步促进生长、生存和治疗耐受性。EGFR的这种核内作用可能帮助肿瘤在其表面活性被化学阻断时仍然逃逸。
Sortilin进入细胞核
此前人们主要将sortilin视为一种参与将EGFR从细胞表面内吞并送往降解通路的分拣蛋白,从而削弱其生长信号。在这项工作中,作者发现sortilin在肺癌细胞受刺激时也会随EGFR一起进入细胞核。通过高分辨率显微镜和生化分馏,他们观察到EGFR与sortilin在激活后不久就在细胞核内形成复合体。重要的是,当EGFR无法进入细胞核时,sortilin也不会进入,这表明EGFR充当了sortilin进入该区室的“通行证”。进入核内后,EGFR–sortilin复合体被发现在靠近关键生长调控基因起始位点的DNA区段上结合,包括cMYC和CCND1。
内置的癌基因刹车
为了解这些复合体的功能,研究者绘制了它们在基因组上的结合分布并测量基因活性变化。他们发现单独的EGFR倾向于促进与生长相关基因的激活,而sortilin出现在相同DNA区段时会削弱这种效应。当人工降低sortilin水平时,EGFR在靶基因处的结合增加,驱动癌症的基因如cMYC和CCND1的活性升高。相反,提升sortilin水平则产生相反的效果:EGFR与DNA的结合减弱,转录机器的招募减少,这些致癌基因的表达下降。在小鼠模型中,工程性过表达sortilin的肺肿瘤生长更慢,且cMYC与CCND1水平降低。 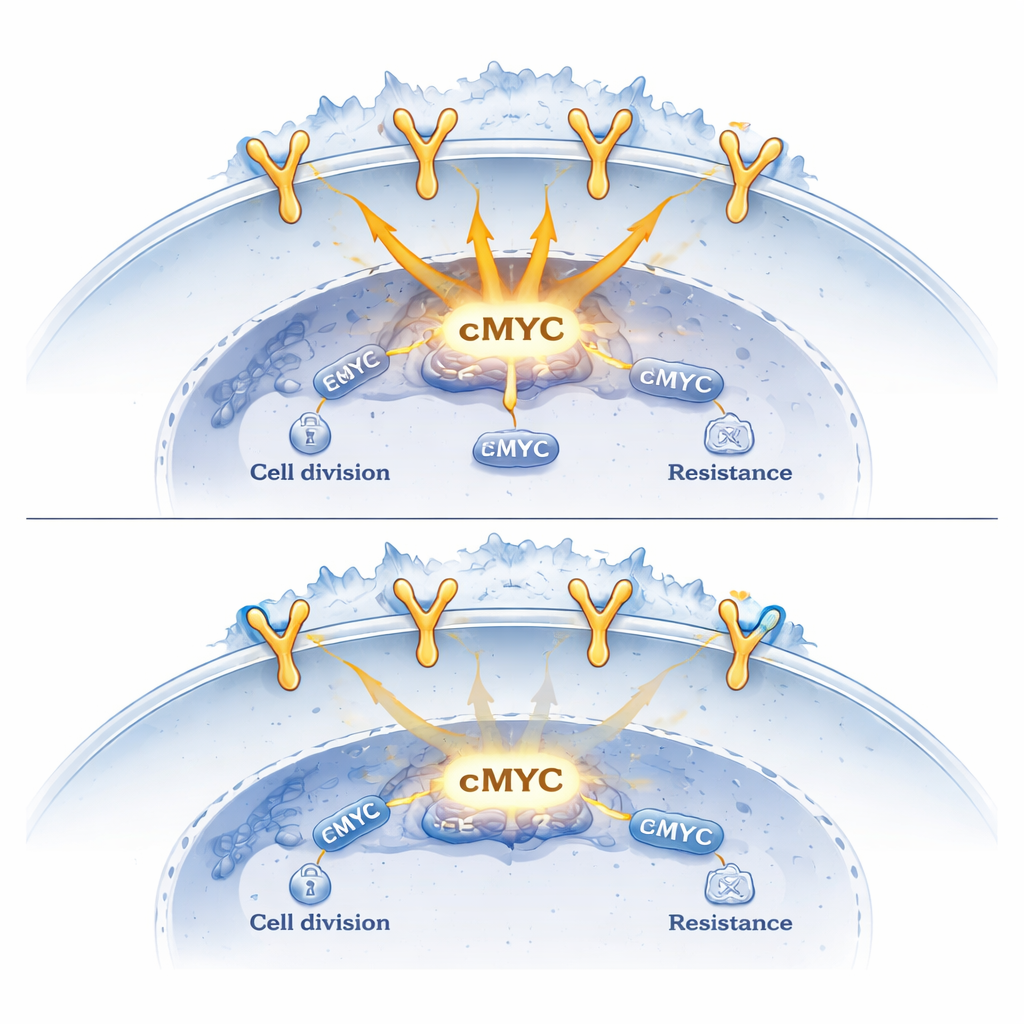
与EGFR药物的相互作用
研究还探讨了该机制与奥希替尼(osimertinib,一种广泛使用的针对EGFR突变的药物)之间的相互作用。令人意外的是,即便奥希替尼关闭了EGFR的酶学活性,该受体仍然迁移到细胞核,并继续结合DNA,尤其是在cMYC基因附近。然而在这些情况下,sortilin也在核内积累。当sortilin丰富时,cMYC在对奥希替尼的反应中下降得更明显,癌细胞存活性减少。对患者肿瘤和大型公共癌症数据库的分析显示,肺腺癌中sortilin的水平常常低于正常肺组织,且较高的sortilin表达一贯与较低的cMYC表达相关。
这对患者意味着什么
综合来看,这些发现将sortilin描绘成一种类肿瘤抑制的伙伴,它随EGFR进入细胞核并对其加以抑制。通过限制EGFR激活像cMYC这样强效生长基因的能力,sortilin可以减缓肿瘤进展并增强EGFR抑制药的疗效。由于许多肺肿瘤的sortilin减少,它们可能缺乏这一内部刹车,这有助于解释为何一些癌症表现得尤其侵袭性或迅速产生药物耐受。测量肿瘤中的sortilin水平可能有助于预测患者对EGFR靶向疗法的反应,而提升sortilin活性的策略或可为长期控制EGFR驱动的癌症提供新途径。
引用: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
关键词: 肺癌, EGFR, sortilin, cMYC, 靶向治疗耐药