Clear Sky Science · zh
白介素-6 对人类 iPSC 衍生多巴胺能神经元的突触影响
为什么炎症与情绪有关
许多抑郁症患者的血液中存在低度炎症的迹象,这些免疫学改变与快感缺失、疲倦和运动迟缓等症状有密切关联。本研究提出一个聚焦问题:一种关键的炎症信号分子——白介素‑6,如何直接影响使用多巴胺的人的脑细胞?多巴胺是推动动机与奖赏的重要化学物质。通过在实验室中将人类多能干细胞培养为产生多巴胺的神经元,研究者可以观察这些细胞如何响应炎症,以及这种反应在女性与男性之间是否不同。
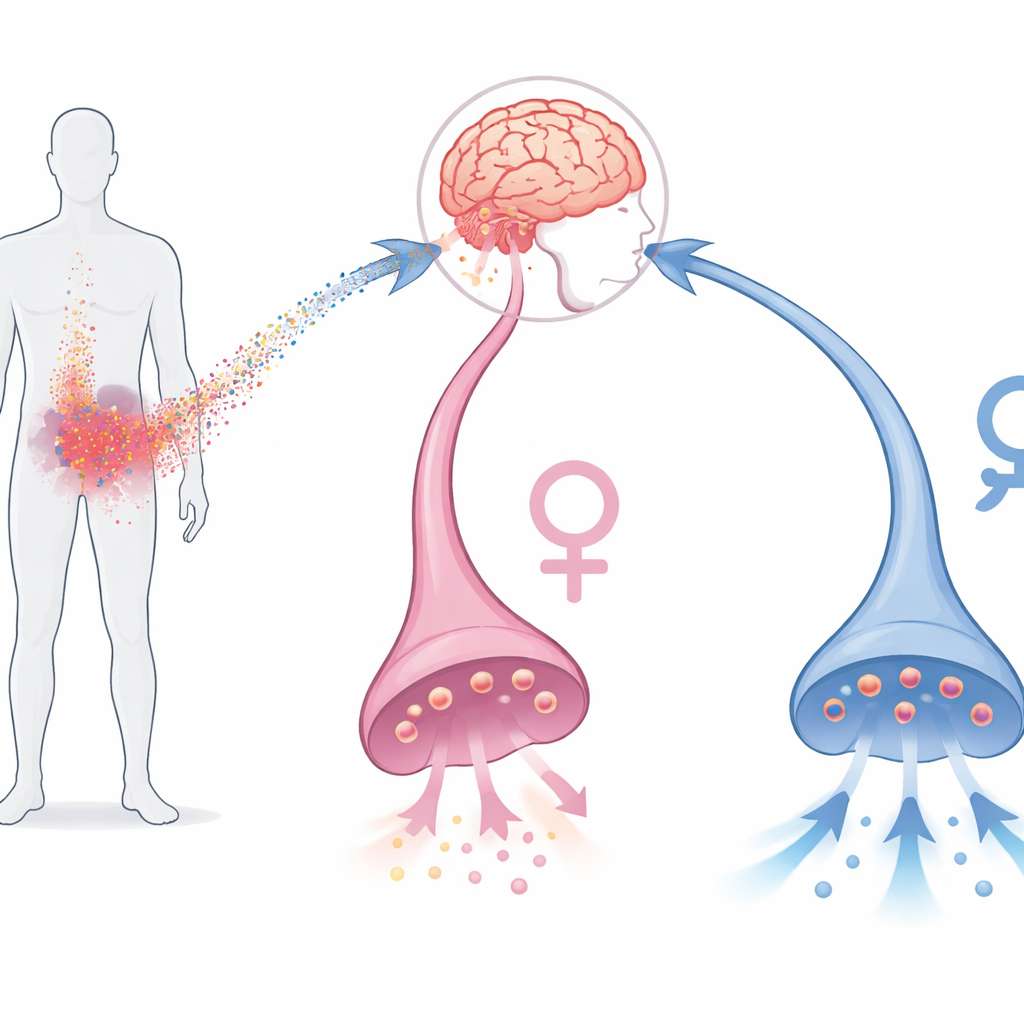
从血液信号到大脑的动机系统
抑郁症普遍存在、致残性强,且在血液炎症水平升高的人群中常对常规抗抑郁药耐受性较差。既往的人类与动物研究表明,炎症触发物会抑制脑内奖赏回路的活动,尤其是依赖多巴胺的腹侧纹状体区域。当炎性分子被实验性升高时,人和动物通常表现出为奖赏努力的动力下降。白介素‑6 就是这样的分子之一,在应激下它可以到达脑中的多巴胺神经元。然而,它如何精确地改变释放多巴胺的细胞仍不清楚,尤其是在人体神经元和不同性别之间的差异上。
在培养皿中构建人类多巴胺神经元
为了解析这些机制,团队将健康男性和女性的皮肤或血细胞重编程为诱导多能干细胞,然后引导它们分化为中脑型多巴胺神经元——即参与动机的那类。经过约八周的成熟,这些神经元表现出预期的标志和电生理活动。随后科学家将细胞暴露于白介素‑6 24 小时,测量三个关键特征:它们释放了多少多巴胺、放电(电脉冲)频率如何,以及装载多巴胺的小囊泡在突触末端移动与停靠以释放其货物的效率如何。
女性与男性细胞的不同表现
结果显示出女性来源与男性来源神经元之间明显的分歧。在女性来源的细胞中,白介素‑6 明确削弱了多巴胺系统:多巴胺释放减少,放电变慢,囊泡移动更迟缓且较少处于准备好释放的停泊状态。在男性来源的细胞中,相同的炎性信号仅引起轻微的减慢,但触发了看似内在的补偿反应。囊泡移动加快并在末端变得更多,突触前接触点数量增加,这些变化可能有助于在炎症下维持多巴胺输出。基因表达分析支持这些功能性差异,显示白介素‑6 在女性神经元中激活了更强的炎症程序,而在男性中则较弱。
一种长链非编码 RNA 作为隐性开关
进一步深入研究时,研究者关注到一种调控分子 MIAT,它是一种不编码蛋白质的长非编码 RNA,可微调基因活动。男性多巴胺神经元起始时的 MIAT 水平高于女性神经元,且白介素‑6 在两性中对 MIAT 的影响方向相反。当团队在男性神经元中通过基因编辑删除 MIAT 时,这些细胞失去了原有的保护性补偿反应。在暴露于白介素‑6 后,缺失 MIAT 的男性神经元表现出多巴胺释放减少、放电变慢和停靠囊泡减少——很像女性神经元。MIAT 还影响控制多巴胺回收和细胞对白介素‑6 敏感性的基因,提示它作为一个分子枢纽,塑造多巴胺神经元应对炎性压力的方式。
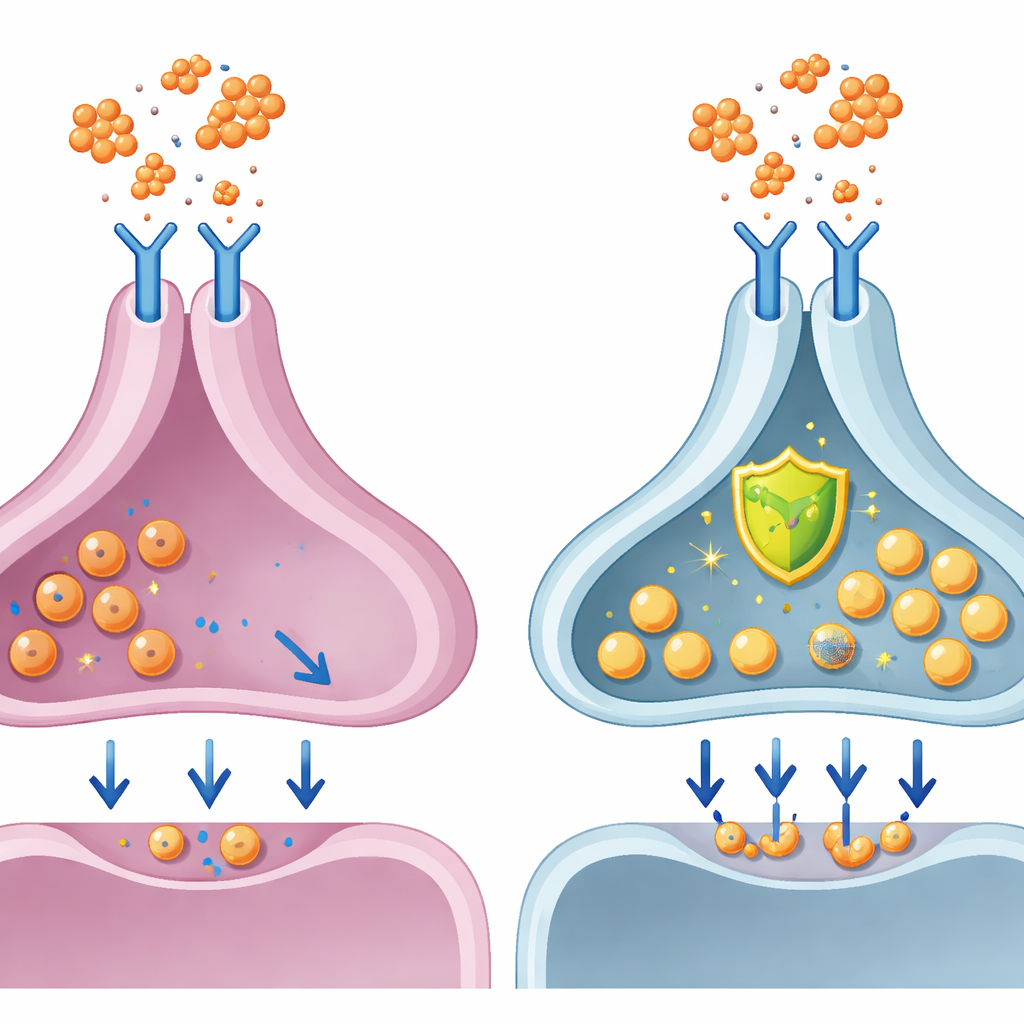
阻断有害通路
鉴于白介素‑6 通过一条已知的蛋白链 JAK‑STAT 通路传导信号,科学家检验了阻断该通路的现有药物是否能保护多巴胺神经元。他们在同时加入白介素‑6 的情况下,使用了已获批用于炎性疾病的 JAK 抑制剂巴瑞替尼(baricitinib)。在女性来源的多巴胺神经元中,巴瑞替尼在很大程度上逆转了多巴胺释放下降、电生理活动变慢和突触囊泡问题。这表明针对该通路可以直接保护体外的人类多巴胺细胞免受炎症诱导的功能障碍,并可能部分解释为何此类药物在某些患者中与情绪和动机的改善相关。
这对抑郁症患者意味着什么
综合来看,这项工作表明炎性信号可以以性别特异的方式削弱人类多巴胺神经元:女性神经元更倾向于在多巴胺释放机制上出现明显损伤,而男性神经元则倾向于产生有助于维持功能的适应性改变。一种非编码 RNA MIAT 似乎是这一差异的重要组成部分,而通过巴瑞替尼阻断下游信号可挽救易受损的细胞。对于患者而言,这些发现支持这样一个观点:针对炎症的治疗可能对血液炎症标志物较高的抑郁患者特别有益,并且在选择此类疗法时,应考虑性别和个体分子特征的差异。
引用: Huang, Y., Michalski, C., Zhou, Y. et al. Synaptic effects of interleukin-6 on human iPSC-derived dopaminergic neurons. Neuropsychopharmacol. 51, 934–945 (2026). https://doi.org/10.1038/s41386-025-02320-y
关键词: 炎症与抑郁, 多巴胺神经元, 性别差异, 白介素-6, 抗炎治疗