Clear Sky Science · zh
RO4938581,一种GABAA-α5负向别构调节剂挽救了Dup15q综合征小鼠模型的行为和脑电表型
这项脑科学研究为何重要
Dup15q综合征是一种罕见的遗传病,常导致自闭症、癫痫和严重的学习困难。家庭能提供的主要是支持性照护,目前没有针对病因的治疗方法。本研究使用携带与Dup15q患者相同多出染色体片段的小鼠,探究大脑中发生了什么异常——并测试一种高度靶向的实验性药物是否能将该异常逆转。该工作突出了某类大脑受体作为未来精准药物的有希望且可检验的靶点。
大脑中过度的“刹车”
我们的大脑依赖于兴奋神经元的“前进”信号和抑制它们的“停止”信号之间的微妙平衡。在Dup15q综合征中,染色体15的一段被重复了。该区域包括构成大脑关键“停止”受体GABAA受体的三个基因,尤其是含有α5亚基的那一种。研究人员构建了具有相同重复片段的小鼠,发现这些动物在海马和皮层等与记忆、情绪和运动相关的大脑区域中,含α5亚基的受体数量增加了约50%。从基因表达到受体成像的多种方法都得出相同结论:在Dup15q模型中,这一特定的刹车系统被过度构建了。
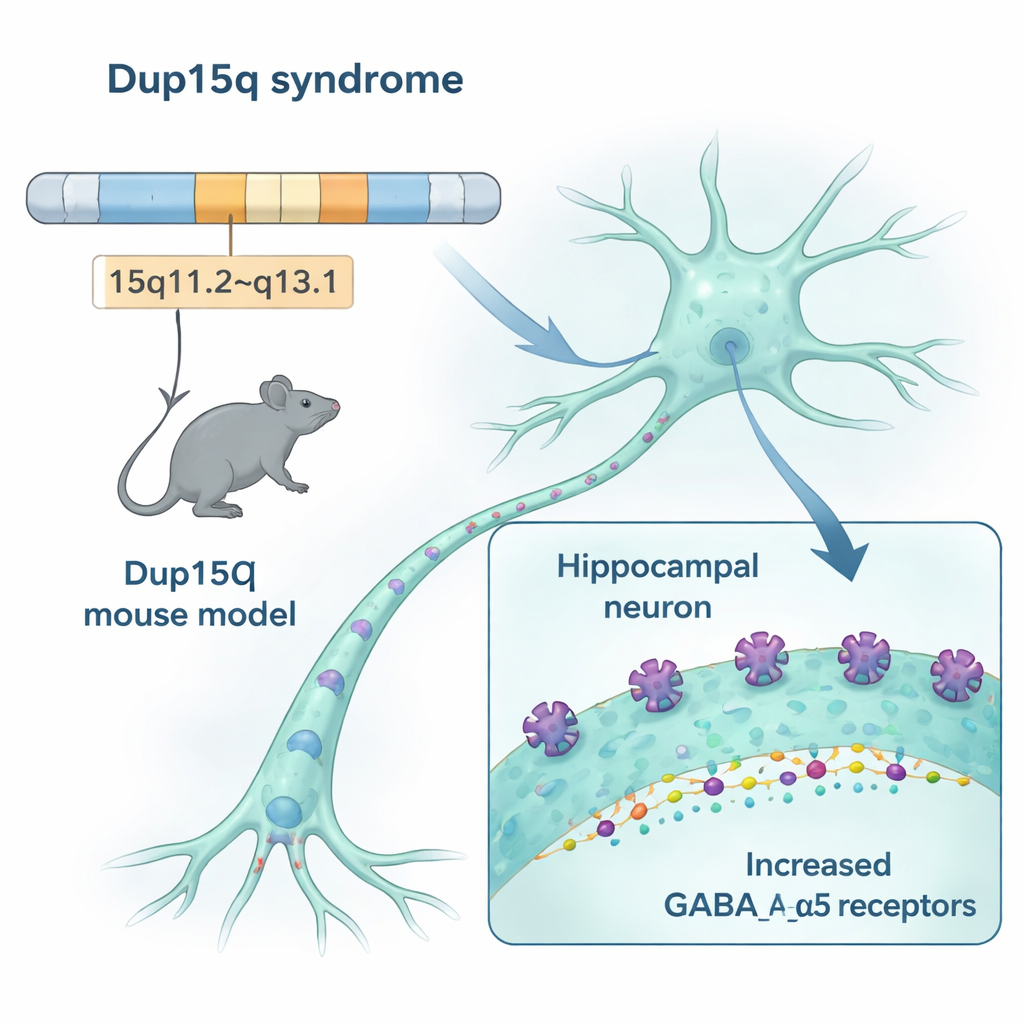
额外受体如何改变脑信号
受体增多只有在确实改变回路放电时才会重要。在来自海马的薄脑切片中,团队测量了抑制性神经元传递给其他细胞的微小电流。在Dup15q小鼠中,这些抑制性电流发生得更频繁,表明神经元持续受到更强的抑制,即便每个信号的幅度并未改变。另一项称为配对脉冲抑制的回路功能检测也显示,这些小鼠的大脑网络比健康同窝鼠更易被抑制。综合这些数据表明,额外的受体使抑制回路更占主导,导致信息处理的灵活性偏离平衡。
受影响小鼠的行为和脑电波
科学家接着询问,这种改变的连线是否转化为类似人类症状的行为。在一系列测试中,Dup15q小鼠表现出社交与交流方面的差异迹象,最明显的是认知灵活性受损。在水迷宫任务中,正常小鼠和Dup15q小鼠都学会了隐藏平台的位置。但当平台被移动后,Dup15q动物迟迟不放弃旧位置、难以适应新位置——这相当于实验室中对自闭症中常见僵化行为的体现。团队还记录了脑电图(EEG)信号,即大量神经元的汇总节律。与Dup15q患者相似,这些小鼠表现出异常增强的β频带活动,这是一种经常被增强GABAA受体的药物所提高的快速节律,进一步支持其抑制系统过度活跃的观点。
一种放松刹车的靶向药物
为了观察是否能将这种过度抑制恢复正常,研究人员使用了RO4938581,这是一种选择性削弱含α5型GABAA受体而不影响其他类型的实验性化合物。在海马切片中,该药物减少了Dup15q神经元中的抑制电荷传递,抵消了多余的抑制作用。口服每日给药数周后,同一化合物改善了动物在水迷宫可逆阶段的表现,使其在平台移动后更像健康小鼠那样调整。它还使其社交互动更接近正常。在脑电记录中,急性给药部分降低了Dup15q小鼠夸大的β波功率,将其脑节律向典型模式推近。
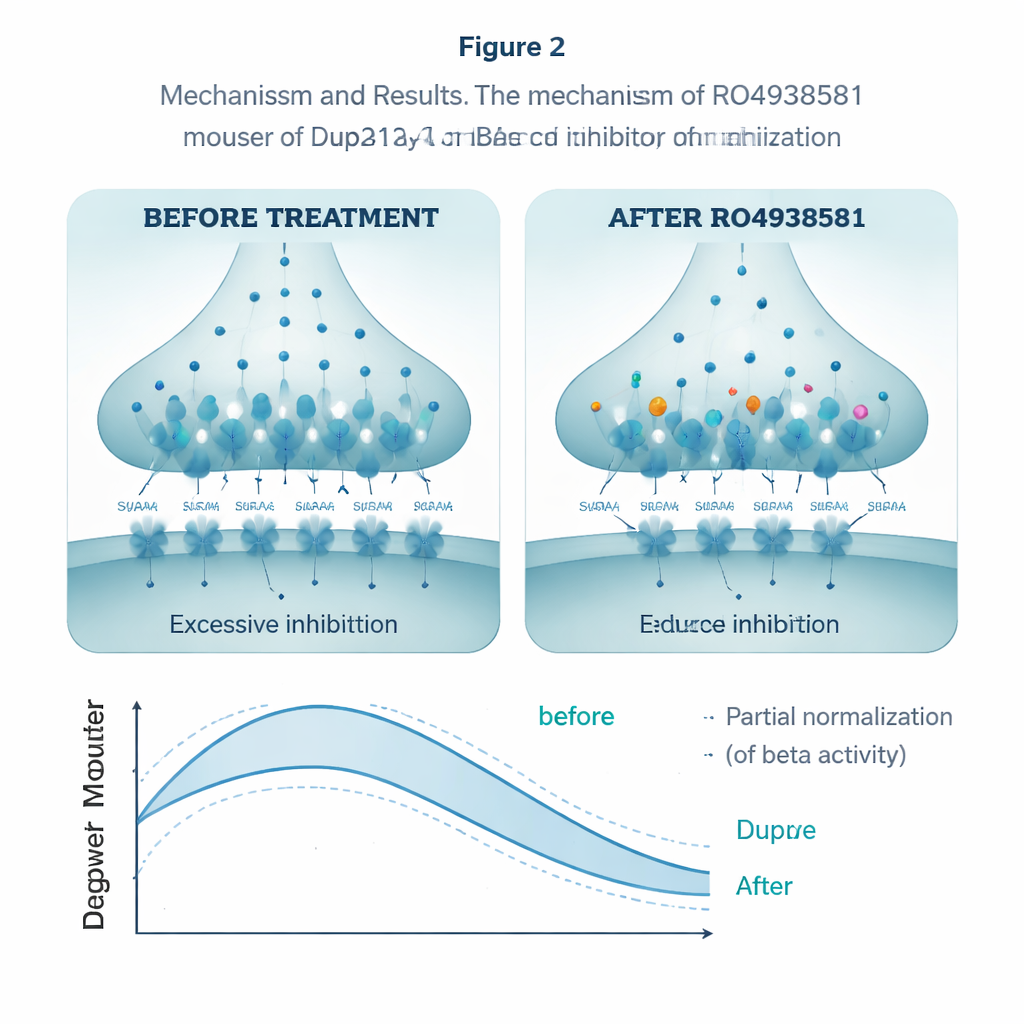
这对未来治疗可能意味着什么
对于生活在Dup15q综合征中的家庭来说,这些发现并不意味着立即的治愈,但确实提供了一个具体的线索。该工作指向了一个特定的受体亚型——含α5亚基的GABAA受体——在相关动物模型中既被过度产生又在功能上重要。用像RO4938581这样的负向调节剂适度抑制该受体并未解决所有问题,但确实改善了灵活性学习、社交行为和一个关键的EEG生物标志物。大脑、行为与生物标志物三方面的变化共同增强了将更安全、适合人体使用的α5靶向药物作为针对Dup15q以及潜在相关神经发育疾病的精准治疗进行测试的理由。
引用: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
关键词: Dup15q综合征, GABAA α5受体, 神经发育障碍, 脑电β波功率, 小鼠模型