Clear Sky Science · zh
级联惰性微流控用于高通量、多尺度富集肿瘤细胞及完整簇以提升恶性诊断
为何在液体中分离癌细胞很重要
当癌症扩散时,肿瘤细胞常常逃逸到包绕器官的体液中。在肺癌患者中,这可能包括积聚在肺周围的液体,即胸腔积液。隐藏在这些液体中的是罕见的单个肿瘤细胞以及紧密相连的细胞簇。研究认为这些簇尤其危险,因为它们与侵袭性疾病和较差预后密切相关。然而,现有的实验室方法难以在不破坏细胞的情况下,从大量患者液体中温和且高效地分离出单个细胞和簇。本研究介绍了一种新的芯片技术,能够快速且细致地从胸腔积液中分选这些细胞,为更可靠的癌症诊断和更好地理解肿瘤转移打开了可能。
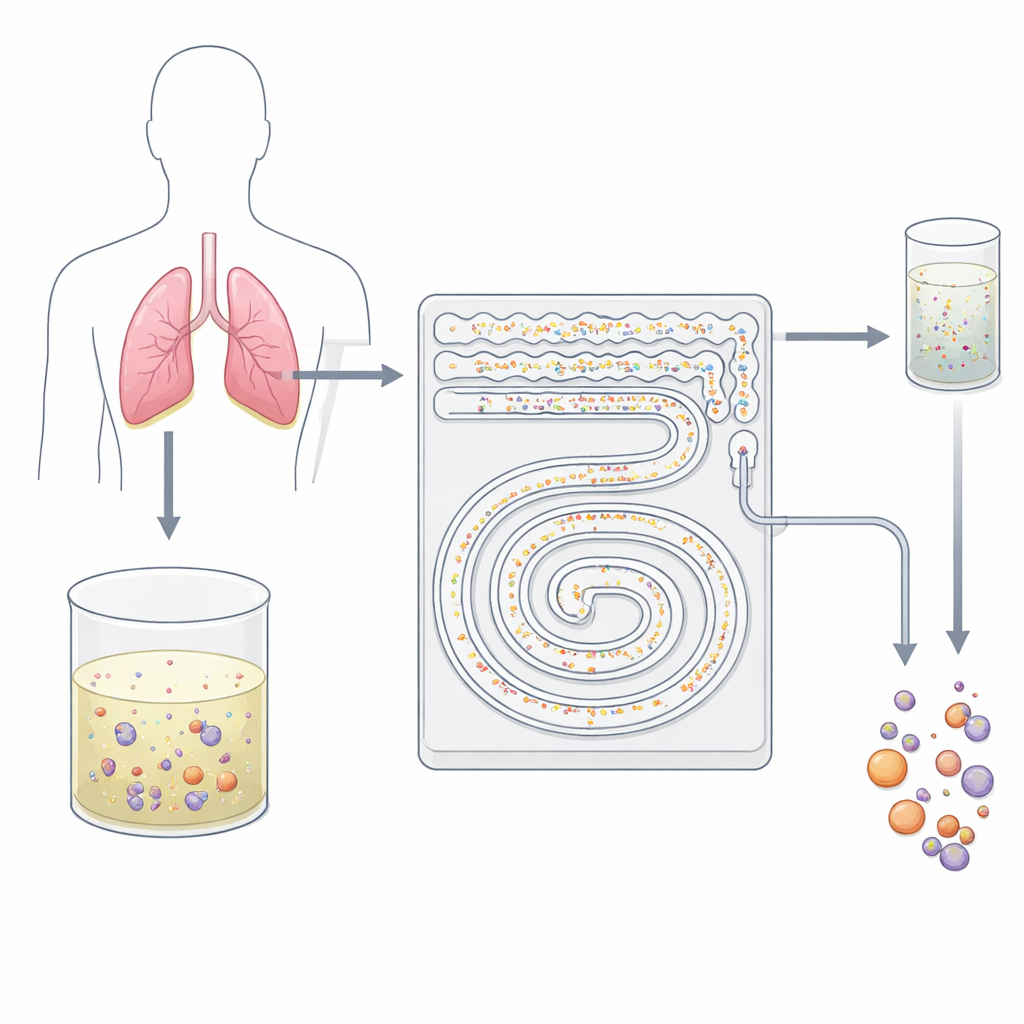
芯片上的温和细胞过滤器
研究者设计了一种手掌大小的塑料装置,刻有微小通道,充当一种智能的两步过滤器。该芯片不依赖粘附性抗体或粗暴的筛分,而是利用细胞在快速流动液体中的行为。当流体通过弯曲的微通道时,隐形的力会将不同大小的颗粒推入不同的流线。团队利用了这一通常称为惰性微流控的效应,将小型背景血细胞与较大的肿瘤细胞及其簇分离开来,无需接触或标记。由于所有过程都在连续、封闭的流动中进行,该装置能够在几分钟内处理数十毫升液体——这是传统载玻片细胞学难以实现的。
第一步:清除背景细胞
在装置的第一阶段,经过去除多余液体并重新悬浮细胞后的胸腔积液被驱动通过一组并行的蛇形通道。在这里,弯曲的涡流将小的白细胞推向通道壁,而较大的肿瘤细胞和簇则保留在流中心。小细胞被引导到废物流出口,从而显著稀释背景成分。该高通量步骤可在约每分钟8毫升的流速下运行,这意味着典型的50毫升临床样本大约可在六分半钟内处理完而不易堵塞。第一阶段的产物流出的是一种更清洁的混合物,富集了潜在的恶性细胞并为更精细的分离做好准备。
第二步:将单细胞与簇分开
部分富集的样品随后进入一个倾斜的螺旋通道,通道中包含窄段与宽段交替重复的结构。在这一阶段,不同大小物体所受的多种流体力呈现不同的平衡,使它们朝螺旋内壁或外壁的不同车道移动。较小的单个肿瘤样细胞会在一个横向位置排队,而体积更大的簇则迁移到更靠近内壁的另一个位置。通过在合适位置设置出口,芯片物理上分流这些流:一个出口主要收集单个肿瘤细胞,另一个收集完整的簇,其他出口则去除剩余的小细胞。重要的是,簇保持完整,避免了传统过滤方法常见的损伤和破裂。
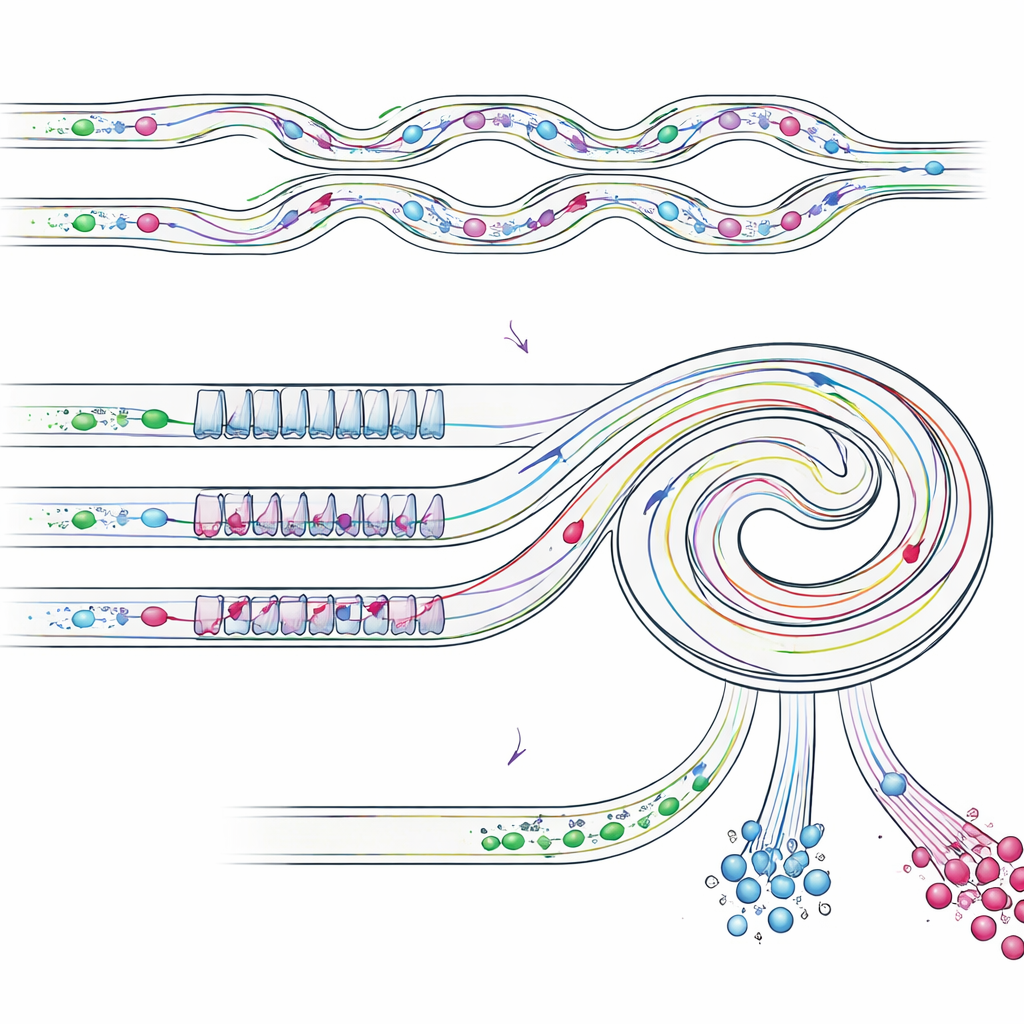
对装置进行测试
为了验证设计的有效性,团队首先使用已知大小的塑料微球模拟血细胞、单个肿瘤细胞和簇。他们证明了级联芯片回收了超过87%的“单细胞”微球和约92%的“簇”微球,同时去除了大多数较小的“血细胞”微球。随后他们进一步测试了与白细胞混合的真实肺癌细胞(A549细胞)。在这些测试中,装置总体回收了约82%的癌细胞,富集部分的纯度约为76%,而细胞簇的纯度接近80%。最后,他们处理了来自三名肺癌患者的实际胸腔积液样本。从肿瘤细胞与簇占所有细胞不到1%的起始液中,芯片在特定出口流中得到了单个恶性细胞约占所有细胞的68%,簇约占该出口中细胞的35%。
这对患者可能意味着什么
通过仅利用流体流动和通道几何形状,该装置可以快速且温和地从大量患者液体中提取单个肿瘤细胞和完整簇,无需化学标记或复杂仪器。富集得到的细胞仍适用于免疫荧光染色和显微镜等常规检测,能够顺利融入现有医院流程。尽管当前研究涉及的患者数量有限,仍需更大规模的临床试验来证明其在诊断和预后中的实际影响,但该工作展示了一个有力的概念:一种快速、无标记的“细胞浓缩器”,可以揭示胸腔积液中肿瘤细胞的数量及其簇态分布。从长远看,此类工具有望提升恶性评估的准确性,为个体化治疗决策提供指导,并为理解癌症转移机制提供更清晰的视角。
引用: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
关键词: 液体活检, 微流控细胞分选, 肿瘤细胞团簇, 胸腔积液, 癌症诊断