Clear Sky Science · zh
基于磁镊用于斑马鱼胚胎的自动化细胞批量显微注射系统的设计
为什么微小的鱼卵很重要
在新药物或基因疗法进入人体之前,科学家常在生长快速且体型小的动物身上进行测试。斑马鱼胚胎因透明且发育迅速而备受青睐,这使研究人员能够实时观察器官的形成。然而,要改变它们的基因或递送药物,必须用显微针对每一个精细的卵进行注射,这一工作通常缓慢、疲劳且高度依赖操作者的技能。本文介绍了一种新的机器人系统,能够自动批量注射斑马鱼胚胎,其速度更快、操作更温和且更可靠,为更大规模、更一致的实验打开了可能。
处理脆弱细胞的新方法
传统的显微注射需要受过训练的操作者在显微镜下操控玻璃针,找到每个胚胎,将其旋转到正确方向,并在不损伤重要结构的情况下刺入。这尤其棘手,因为胚胎是柔软的球体,存在必须避免的关键区域以保证存活。已有的机器人系统在运输和穿刺方面提供了帮助,但通常无法对每个胚胎在三维空间中进行精确旋转。因此,针可能以危险角度进入,降低存活率并限制可可靠处理的胚胎数量。本研究团队致力于构建一个完全集成的平台,能够在无需频繁更换镜头或手动调节的情况下,顺畅地完成胚胎的运输、旋转、注射和释放。
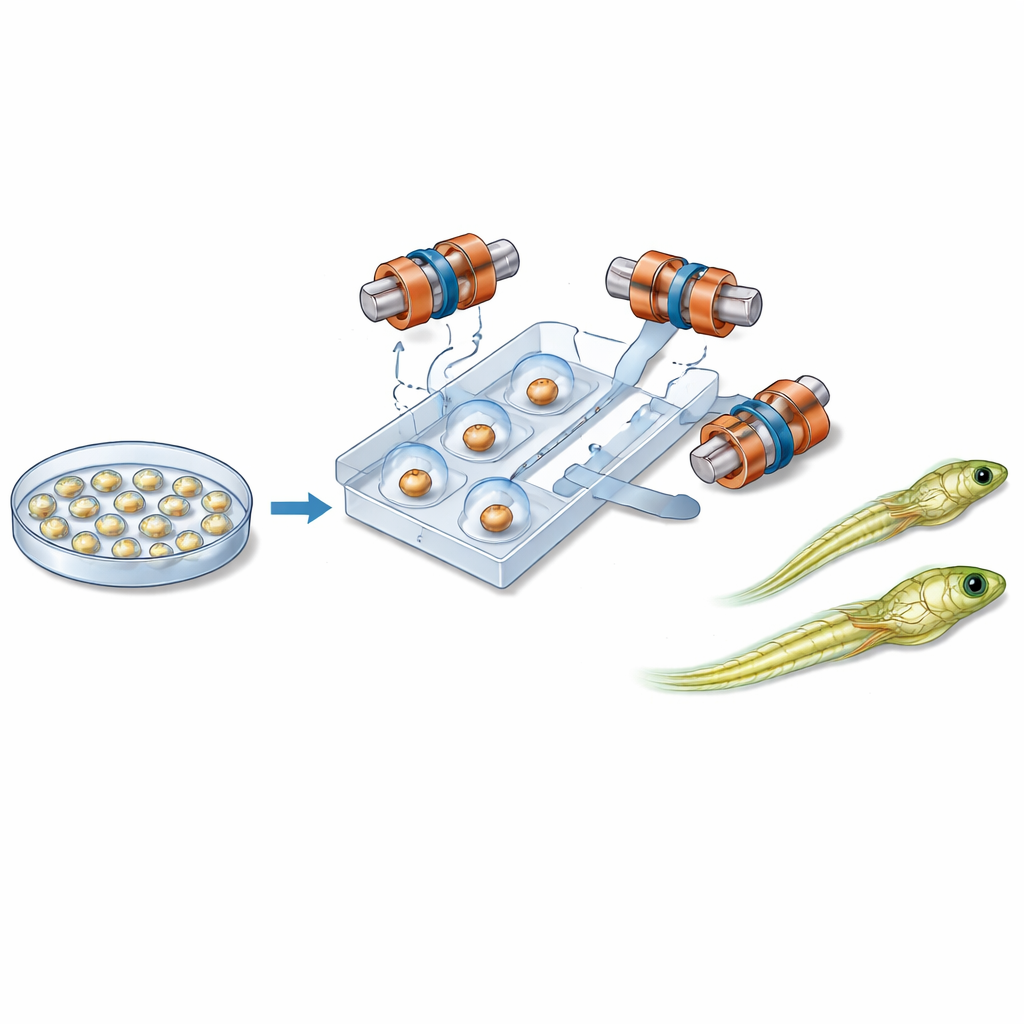
磁铁、微通道与温和控制
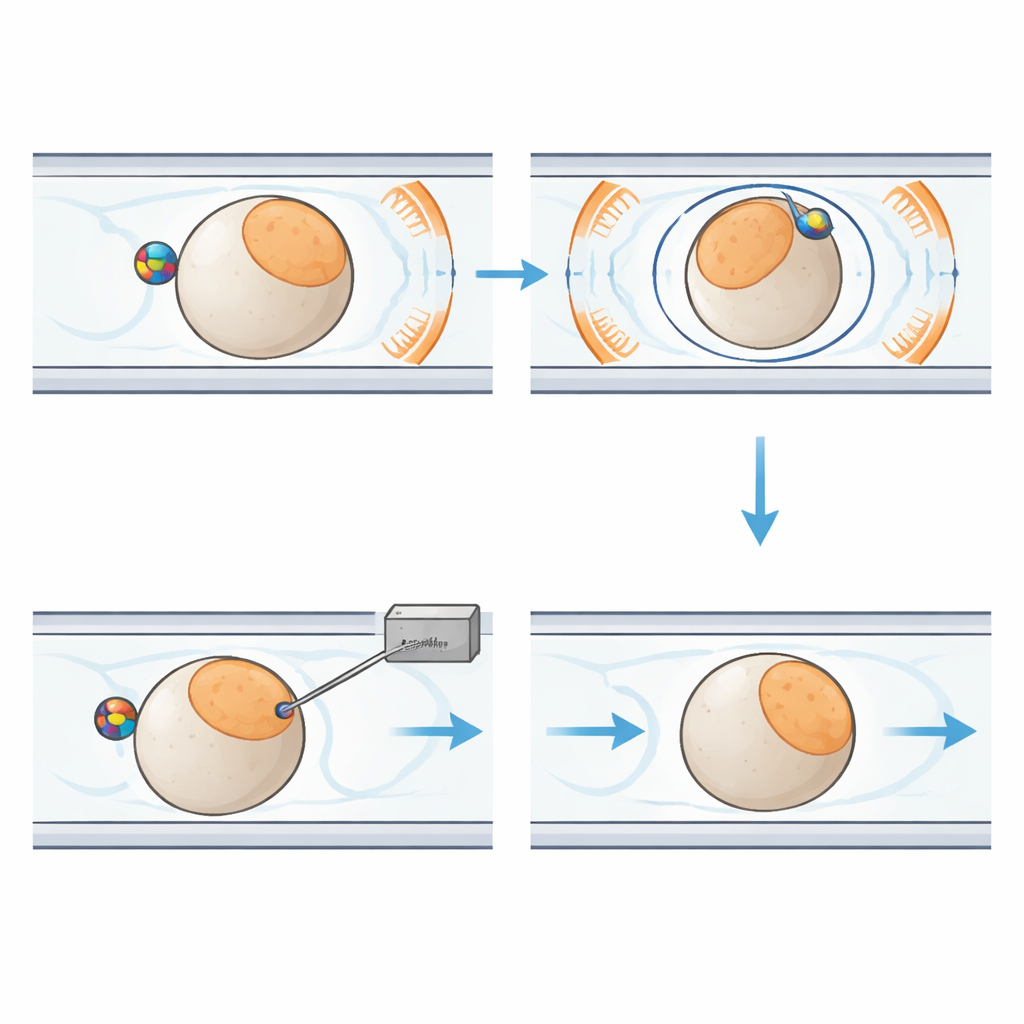
新系统的核心是一块手掌大小的塑料芯片,芯片上有狭窄的通道沿固定路径引导单个胚胎移动。每个胚胎附近放置一个小磁珠。芯片周围布置了六个线圈,能够在三维空间产生均匀的磁场。通过随时间改变磁场方向,系统驱动磁珠旋转。由于磁珠与胚胎表面之间的摩擦,整个细胞随之转动,类似啮合的齿轮。这使机器人能够将胚胎从成像平面倾斜或在平面内旋转,直至将敏感区域安全地置于远离入针方向的位置。液体和温和的气压用于移动并固定胚胎,而单独的模块控制注射针与微量遗传物质的流动。
在微小视野中清晰可见
为了实现这种精确的协同动作,研究人员还设计了一套先进的计算机视觉系统,称为微观操控感知网络。它实时分析显微镜相机图像以定位每个胚胎、检测细小的针尖,并区分胚胎上两端相对的“极区”,这些区域存在关键的发育结构。该网络采用现代深度学习技巧——例如双通路特征提取、突出重要细节的注意力模块以及多尺度图像信息融合——以应对微流控芯片内部杂乱、低光照的环境。在数千张图像的测试中,它对目标的检测与胚胎区域的分割准确率约为98–99%,为磁旋转和针位控制提供了可靠的反馈。
在活体斑马鱼上的验证
团队将其自动化系统与有经验的人类操作者进行了比较,每方各注射100个斑马鱼胚胎。机器人平均每个胚胎用时约33.8秒,速度是人工操作的两倍多,并且成功刺穿了每个细胞。它对每个胚胎的定位平均角误差仅为2.1度,大约是人类操作者误差的一半。更重要的是,机器人注射的胚胎中有88%存活并孵化为幼体,而人工注射存活率为66%。在荧光显微镜下,自动化系统处理的幼体显示出绿色荧光,表明引入的遗传物质被成功摄取并按预期表达。通过用磁力旋转胚胎而不是用机械工具挤压,系统在保持高通量的同时将变形和损伤降到最低。
这对未来研究意味着什么
简而言之,这项工作表明,一种经精心设计的微通道、磁控与智能图像分析相结合的方法,能够比熟练的人工传统操作更快且在更高存活率下完成对脆弱鱼胚的注射。由于斑马鱼是研究发育、疾病和药物作用的重要模型,一台可靠的高通量注射器可以加速大规模基因筛选和长期生物学研究,这些研究曾因人工劳动限制而受阻。通过对芯片和控制参数进行适当的设计调整,同一策略也可适配于其他细胞类型和小型生物体,有助于将精细的细胞“外科”操作从少数专家的手艺,转变为自动化、标准化的流程。
引用: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
关键词: 斑马鱼胚胎, 显微注射, 磁镊, 微流控, 机器人细胞操控